【重磅综述】衰老过程中经典和非经典的细胞间通讯
以下文章来源于老顽童说 ,作者老顽童说

老顽童说
公众号致力于传播衰老相关的前沿科研进展和趣味科普,帮助大家更深入地了解衰老背后的科学故事~

关注我们,获取更多相关资讯
引言
当俞伯牙依水将瑟瑟琴声幽绕山谷的时候,于江之上的钟子期听得如痴如醉,自此传为千古佳话。可见人与人之间除了语言,还可以通过琴乐等多种方式进行交流。那在机体的多种细胞之间是如何进行沟通以满足复杂生命活动的需求呢?衰老过程中这些细胞间通讯方式又会发生怎样的变化呢?今天小编和大家共同学习来自伦敦玛丽女王大学Ana O’Loghlen教授团队,于2020年8月发表在Trends in Cell Biology杂志,题为“Classical and Nonclassical Intercellular Communication in Senescence and Ageing”的综述文章,文章对细胞衰老和机体衰老过程中的经典和非经典细胞间通讯进行了回顾和综述。
通讯作者:Ana O’Loghlen(图源于网络)
摘要
细胞间通讯是指细胞之间相互通讯和传递各种信息的不同方式。这些交流方式包括许多不同的过程,而这些过程可以单独或同时发生,并且随着生理或病理环境的变化而改变。细胞间通讯的典型特征是释放可溶性因子,并影响邻近细胞的功能。然而,细胞之间还可以通过许多其他方式进行互相交流。在此,作者回顾了不同的细胞间通讯方式,包括在细胞衰老、机体衰老和衰老相关疾病中可溶性因子的作用。
要点
(1)细胞间通讯是生理和病理条件下的一个关键特征,目前假设几种细胞间通讯手段可同时发生或连续发生;
(2)通过可溶性因子进行细胞间通讯是目前研究最多的方式,然而重要的替代方式也逐渐被发现;
(3)衰老细胞会主动通过各种细胞间通讯手段与邻近细胞沟通,包括但不限于衰老相关分泌表型(SASP);
(4)大多数关于阻止可溶性因子释放的药理学药物的研究都忽视了这些药物对其他细胞通讯方式的影响。
词汇表
(1)Ferroptosis:铁死亡,指铁在细胞中积累引起的细胞死亡。
(2)Inflammaging:炎性衰老,指以慢性、低度炎症为特征的衰老。
(3)Inflammasome:炎症小体,指能够激活caspase-1并诱导先天炎症反应的免疫系统受体的聚集体。
(4)Senescence:衰老,指以一种或几种生物标志物(包括稳定的细胞周期阻滞和主动分泌体)为特征的表型的激活。
(5)Senescence-associated secretory phenotype (SASP):衰老相关分泌表型,指衰老细胞分泌的可溶性因子、生长因子和基质重塑酶。
(6)Senolytic drugs:延缓衰老药物,靶向杀死衰老细胞的药物。
(7)Senomorphics:抑制SASP的化学物质或药物。
(8)Syncytiotrophoblast:合胞体滋养层,滋养层细胞融合形成的胎盘外层。
(9)Trans-stable-isotope labelling of amino acids in cell culture (SILAC):细胞培养中氨基酸的跨稳态同位素标记,利用SILAC在细胞间转移蛋白质。
正文
一、细胞衰老:一个复杂和异质的表型
20世纪60年代,Moorehead和Hayflflick首次鉴定了一种称为衰老的细胞表型。在体外培养从人类供体中分离出的原代成纤维细胞时,他们观察到这些细胞会出现增殖停滞现象,并将这种表型称为细胞衰老。他们假设这种表型可以模拟衰老,并将其称为“培养皿中的衰老”。在体外发现了一种诱导提前衰老的现象,称为癌基因诱导的衰老,后来证实这种现象在体内抑制肿瘤进展方面发挥了作用。然而,直到2011年,Van Deusen实验室才在细胞衰老和个体衰老激活之间建立了因果关系。作者在BubR1(有丝分裂检查点蛋白)缺失的早衰小鼠模型中发现某些器官中p16Ink4a的积累触发了早衰中常见的自然特征。有趣的是,他们首次发现p16Ink4a基因失活可以改善衰老。现在已经证实,细胞衰老是机体衰老的一个标志。此外,细胞衰老不仅是机体衰老的驱动因素,也是某些年龄相关疾病的驱动因素,如癌症、骨关节炎、动脉粥样硬化、阿尔茨海默病、慢性阻塞性肺病(COPD)和特发性肺纤维化(IPF)等。
虽然衰老的主要特征是细胞周期抑制剂p16INK4A和p21CIP的表达导致稳定的细胞周期阻滞,但细胞衰老对组织稳态的影响源于其高度主动的分泌特征。衰老相关分泌表型(SASP)被认为是细胞衰老的“灵魂”,因为它是高度主动的过程,并随着时间推移而改变其组分。它将产生有利的或不利的影响,而这取决于引发衰老的触发因素和背景。然而,由于在非常具体的情况下只确定了一些因素,SASP的特征还没有很好地被描述出来。还需要注意,衰老是一个复杂的异质细胞表型,能够在许多不同的环境中影响组织稳态,需要谨慎的将它标准化到某些标记(Box 1)。
Box 1
体外鉴定衰老细胞的指南
细胞衰老可由多种触发因素引起,包括端粒缩短、致癌应激、ROS和DNA损伤。进入衰老进程的原代细胞的主要表现是通过表达细胞周期抑制剂CDKN2A、CDKN2B和/或CDKN1A(分别编码p16INK4A、p15INK4B和/或p21CIP蛋白)诱导稳定的细胞周期阻滞,并缺乏增殖相关标记,如Ki67、BrdU或EdU(图1)。然而,由于这些标记不仅限于衰老细胞,也存在于未分化的体细胞中,因此应使用额外的标记来确认衰老表型。推荐鉴定三种以上的生物标志物,以证实衰老的激活。 另一个用于识别衰老的标记是衰老相关的β-半乳糖苷酶(SA-β-Gal)活性。SA-β-Gal的增加是由于衰老细胞中较高的溶酶体活性,这可能是由于衰老中溶酶体数量的增加或溶酶体活性的增加,并且可以通过特定的染色来检测。最后,还应检测其他标记,如DNA损伤、SASP的特定分泌体的释放或特定信号通路的激活,但这些标记更具争议,因为一些触发因素能够同时诱导这些标记的出现,如癌基因通过诱导H-RasG12V表达而诱导衰老。相反,其他触发因素,如发育衰老或αvβ3增加,不会引起一直被认为是衰老关键生物标志物的DNA损伤反应。这证实了并非所有的生物标志物都会在诱导衰老时同时表达,增加了衰老鉴定的复杂性。
需要注意的是,衰老是一种极其复杂和异质的细胞表型,在许多不同的背景环境中影响组织的稳态,标准化标记的推广可能是不利的,因为它很可能存在着与背景相关的、尚未被揭示的衰老特征。
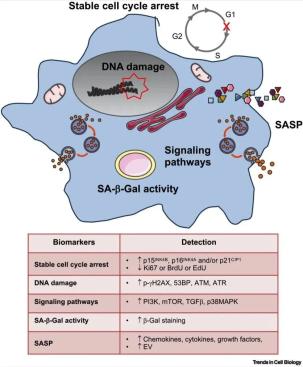
图1 衰老的生物学标记物。(EV,胞外囊泡;mTOR,哺乳动物雷帕霉素靶蛋白;SA-β-Gal,衰老相关β-半乳糖苷酶;SASP,衰老相关分泌表型;TGF-β,转化生长因子β。)
目前有两种主要的治疗策略来处理机体衰老和年龄相关疾病中的衰老细胞。第一个是通过选择性杀死衰老细胞(使用称为“senolytics”的药理学化合物)。第二个是通过使用senomorphics药物来消除细胞间通讯的有害影响,特别是SASP。在此,本文作者回顾了衰老细胞的不同细胞间通讯方式及其与机体衰老和一些年龄相关疾病的关系,将它们分为经典的、新发现的和非经典的细胞间通讯方式,包括可溶性因子和细胞外基质(ECM)重塑蛋白,也描述了细胞通讯的其他方式。文章重点关注了在不同的生物学背景和年龄相关的病理背景下,细胞间通讯是如何调节的及其功能。
二、SASP:经典和非经典细胞间通讯
SASP是一种衰老细胞特有的细胞间通讯手段。经典的SASP以衰老细胞分泌可溶性因子、生长因子和ECM重构酶为特征。然而,新发现的SASP和其他被称为非经典的细胞间通讯手段也在机体衰老和细胞衰老中被描述。在这里,作者回顾了经典、新发现的和非经典SASP的现有知识。
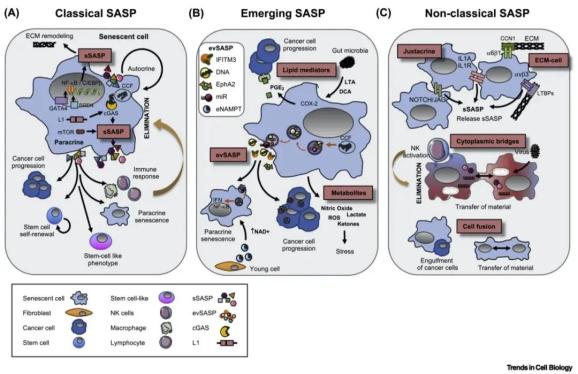
图2 细胞衰老和机体衰老过程中的细胞间通讯。(A)可溶性因子、生长因子和基质重构酶在经典可溶性衰老相关分泌表型(sSASP)模型中被释放。然而,sSASP需要受到严格的调控。在转录水平:BRD4和GATA4调控SASP的两个主要调控因子:NF-κB和C/EBPβ。sSASP也可以被LINE-1(L1)的逆转录转座元件驱动,这些逆转录转座元件在衰老过程中解脱抑制,而细胞质染色质片段(CCFs)通过活化环状GMP-AMP合成酶(cGAS)来驱动。哺乳动物雷帕霉素靶蛋白(mTOR)和下游信号通路也对该sSASP进行转录后调控。分泌的sSASP在微环境中起着多种作用,一方面,它改变了细胞外基质(ECM),可以通过自分泌信号增强衰老。另一方面,通过旁分泌信号也发挥许多功能。它可以促进癌症进展、干细胞自我更新和受损细胞中的干细胞样特征。同时还具有将衰老传递给邻近细胞的能力。重要的是,sSASP可以刺激先天和适应性免疫反应,有利于衰老细胞的消除。(B)新发现的SASP因子包括胞外囊泡(EVs)(evSASP)。由于胞外囊泡在衰老过程中包含物的高度异质性和多样性,新的功能不断涌现。一些因子逐渐被重视,如干扰素(IFN)和ephrin相关的抗氧化蛋白。此外,miRNAs(miRs)和CCF DNA片段可以装载到evSASPs中。evSASPs还发挥旁分泌功能,促进癌症进展和诱导旁分泌引起的衰老。此外,已经发现代谢产物和脂质介质可以诱导氧化微环境或促进肿瘤进展。肠道微生物释放脂磷胆酸(LTA)和脱氧胆酸(DCA),它们通过COX-2和前列腺素E2 (PGE2)的释放驱动sSASP反应。(C)非经典SASP是指不受释放因子驱动的衰老过程中的细胞间通讯。细胞间通讯可以通过受体相互作用来介导,如白细胞介素-1受体(IL-1R)和白细胞介素-1 (IL-1A)或NOTCH1/JAG相互作用,两者均可诱导sSASP。此外,cell-ECM相互作用已被描述在衰老过程中发生。例如, 在αvβ3诱发sSASP时整合素α6β1可以与CCN1 (cysteine-rich蛋白1)相互作用进而通过活性氧(ROS)来诱导衰老。另外,称为细胞质桥的细胞质延伸也发生在细胞衰老过程中。有趣的是,衰老细胞和自然杀伤(NK)细胞之间发生的细胞质桥促进了衰老细胞的清除。细胞的融合也可以诱导细胞衰老,使融合细胞之间的物质交换成为可能。此外,衰老细胞可以吞噬癌细胞作为能量来源,维持衰老细胞的高代谢需求。(eNAMPT,胞外烟酰胺磷酸核糖转移酶;EphA2,肝配蛋白A;;IFITM3,干扰素诱导的跨膜蛋白3;LTBP,潜活相关的TGF-β结合蛋白。)
(一)经典SASP:可溶性因子或sSASP
sSASP对组织稳态既有利又有害。因此,需要对sSASP进行严格调控。sSASP的主要驱动因素之一是持续的DNA损伤反应。两个主要调控SASP的因素是:NF-κB和C/EBPβ,而NF-κB受转录因子GATA4的调控(图2A)。然而,独立于p38 MAPK和胞质染色质片段(CCFs)的非典型DNA损伤反应也可以诱导sSASP。这些DNA片段可以在衰老过程中从细胞核中释放出来,激活干扰素基因(STING)通路的抗病毒环状GMP-AMP合酶(cGAS)刺激因子。不过,p38 MAPK和CCF激活sSASP需要通过NF-κB信号。
奇怪的是,炎症小体的激活也可以调控sSASP。这是由白介素(IL)-1的信号转导和表达介导的,主要参与旁分泌衰老信号。此外,IL-1A受到哺乳动物雷帕霉素(mTOR)抑制靶点的调控。mTOR选择性地通过IL-1A转录后调控多个sSASP因子,也通过蛋白合成因子4EBP1调控MK2[丝裂原活化蛋白激酶激活蛋白激酶2(MAPKAPK2)]来调控sSASP。
另外,表观遗传改变也可以调节sSASP。最近的一项研究发现,在细胞衰老和衰老过程中逆转录转座因子LINE-1(L1)的抑制。这进而激活了cGAS/STING,从而激活了sSASP。此外,sSASP还受到染色质重塑以及BRD4向sSASP基因附近超增强子的招募的调控。总的来说,由于功能异常的表达和释放可以导致病理状态,因此sSASP要受到严格的调控。
长期以来,人们认为sSASP的成分会随着时间的推移而改变。直到最近,一项全面的研究才发现sSASP包含两种不同的功能。第一是富含抗炎转化生长因子(TGF)-β的sSASP。这种特殊的sSASP由膜结合蛋白NOTCH1调控,NOTCH1的表达在衰老的初始阶段增加,并介导C/EBP抑制。第二是随着时间的推移,NOTCH1表达降低,导致C/EBP蛋白的活化,进而诱导促炎sSASP产生。
在过去的几十年里,人们对sSASP的了解逐渐深入。一方面,sSASP通过IL-8和IL-6及其相应受体以自分泌方式来加强细胞周期阻滞的稳定进行(图2A)。另一方面,它以旁分泌方式影响多种细胞类型。它可以诱导原代成纤维细胞和上皮细胞的衰老,同时促进癌细胞的肿瘤发生。重要的是,sSASP还通过介导先天和适应性组织反应来发挥旁分泌作用,这有利于将衰老细胞从组织中去除,对维持组织稳态至关重要。最近,SASP被证明是通过IL-6进行组织再生的关键,以及对细胞可塑性和干性维持都十分重要。尽管在sSASP的新功能和调控方面有许多新的进展,但也有如下所述的其他新发现的功能。
(二)新发现的经典型SASP
虽然经典的SASP被定义为衰老细胞释放的分泌体,但目前的大多数研究主要集中于研究衰老细胞分泌的可溶性因子、生长因子和细胞外基质重塑酶。而在这一部分,本文作者主要对文章中所报道的包括胞外囊泡(EVs)、非细胞代谢物、离子等在内的一些“新发现的”SASP的组分进行了总结(图2B)。
EVs是一种脂膜囊泡,可由所有细胞释放产生,因此存在于绝大多数生物体中。在最初的认识中认为EVs主要作为细胞内非必需物质或代谢废物的一种“排泄”方式,但是目前发现其是一种成熟的细胞间通讯方式。尽管如此,衰老细胞还是会通过EVs清除有毒的细胞质DNA,以维持细胞内环境的稳定。事实上,衰老细胞比增殖细胞释放更多的EVs(evSASP)。有趣的是,已经证明这些EVs可以诱导健康细胞旁分泌衰老,这突出了它们作为细胞间通讯媒介的重要性(图2B)。虽然其诱导旁分泌衰老的机制目前尚不清楚,但在衰老细胞分泌的EVs中发现了几种miRNAs、干扰素相关蛋白和抗凋亡蛋白。相反,EphA2介导的来自衰老细胞的EVs具有促肿瘤作用,为evSASP增加了一层额外的复杂性。有趣的是,从老年健康捐赠者中提取的血浆中富集了几种与肾上腺素相关的蛋白,尽管它们是否是游离蛋白或EV相关蛋白仍有待确定,但在一定程度上也提示了evSASP的功能重要性。
代谢物是细胞和组织中具有代谢活性的小化学分子的代谢副产物,代表了细胞的生化代谢活性。因此,几种代谢物目前也已成为细胞衰老、成体衰老和衰老相关疾病的生物标志物。目前有研究发现EVs内部也含有代谢物调控因子,这也证明EVs也具有生物活性。例如,有研究发现EVs中存在NAD+的调节因子细胞外烟酰胺磷酸核糖转移酶(eNAMPT),且在小鼠和人类中随着年龄的增长而减少。此外,含有eNAMPT的EV可增加受体细胞中的NAD+水平,延缓小鼠的衰老并延长寿命。有趣的是,NAMPT已经被证明可以调节SASP,因此NAMPT和EV两者可以相互作用、调控衰老。
年轻人和老年人的胞外代谢物谱不同。对老年献血者(> 74 岁)的血液分析发现,与抗氧化剂、氧化还原和肌肉维持相关的代谢物减少。在衰老期间,包括血浆在内的各种组织中抗氧化分子NAD+的水平降低,而这也与相对NAD+的降低有关:即NADH比值的降低有关线粒体功能障碍相关的衰老中发现的NADH比值。此外,在衰老细胞中发现柠檬酸和参与氧化应激的代谢物增加。总而言之,这些发现均与衰老细胞的细胞外代谢谱有关,然而,柠檬酸盐与血液中的铁有关。在衰老和阿尔茨海默氏症和帕金森氏症等与年龄相关的疾病中,铁的水平通常会增加,从而导致活性氧(ROS)的产生。活性氧、乳酸、酮、谷氨酰胺和一氧化氮(NO) 都是衰老细胞释放的高能代谢物,会在其周围产生有毒的微环境。鉴于离子和代谢物在细胞衰老和个体衰老方面的特征不清楚,进一步了解它们怎样作为SASP新发现的组成部分发挥作用将是至关重要意义。
脂质介质包含一系列分子,这些分子与抗炎和促炎机制有关,也能促进微生物的清除。最近的一项研究发现,与肥胖相关的肠道微生物组分脂磷壁酸(LTA)和脱氧胆酸(DCA)可诱导肝星状细胞(HSCs)衰老,促进肝细胞癌(HCC)的发生与发展。有趣的是,LTA通过COX-2诱导脂质代谢产物前列腺素E2(PGE2)的释放,并抑制抗肿瘤免疫。作为一部分“新发现的”的SASP,确定其他脂质介质是否与维持组织内稳态有关将是一件有趣的事。
(三)非经典细胞间通讯
在这一部分,本文作者主要对细胞衰老和个体衰老中存在的可溶性和新发现的SASP以外的其他细胞间通讯方式进行了总结,并将其称之为细胞间通讯的非经典(或非分泌)机制(图2C)。
近分泌信号(Juxtacrine signaling)是一种依赖受体与配体结合的一种细胞间通讯方式。衰老细胞间也通过细胞与细胞或近分泌方式与邻近细胞进行“交流”。例如,IL-1A被认为是可溶性因子旁分泌衰老的主要调节因子,也调节近分泌衰老。衰老细胞表达具有膜结合能力的IL-1A,它与IL-1R相互作用来调控IL-6和IL-8的水平;因此,使用RNA干扰或阻断抗体下调IL-1R或IL-1α可防止IL-6和IL-8在衰老过程中上调(图2C)。此外, Hoare等人的一项杰出的研究表明,他们发现SASP的组成是高度动态的,膜具有膜结合能力的NOTCH1的表达可调控SASP的组成。虽然NOTCH1最初通过驱动一个典型的富含转化生长因子β的分泌体的典型的细胞间通讯方式进行调控,但它也通过侧向诱导方式通过近分泌缺口/JAG途径促进细胞间接触而促进衰老,这被定义为继发性近分泌衰老,其中NOTCH1对于通过细胞间信号传递衰老是必不可少的,但对于由可溶性因子或细胞自主衰老介导的旁分泌衰老来说不是必需的。
目前的研究表明,sSASP可以诱导ECM重塑和硬化,这将导致衰老过程中免疫细胞的募集发生改变。虽然公认衰老细胞向细胞外基质分泌多种细胞外基质重塑蛋白,但衰老细胞与细胞外基质的相互作用还不是很清楚。在伤口愈合、炎症、纤维化、心脏再生和癌症过程中,整合素α6β1和细胞蛋白CCN1之间的相互作用可以诱导衰老,激活ROS。此外,整合素αvβ3也被证明通过以细胞自主和非细胞自主的方式激活转化生长因子-β通路来诱导衰老。然而,虽然细胞外基质诱导了ROS的释放,但并没有引起DNA损伤,提示细胞外基质与细胞间的相互作用可能通过不同的机制诱导细胞衰老。
细胞与细胞融合是一种细胞间通讯方式,融合蛋白的异常表达或病毒感染(如麻疹或ERVWE1表达)可诱导该方式产生。它不仅可以诱导原代细胞衰老,而且在癌细胞中也介导免疫反应。虽然所涉及的机制仍有待阐明,但目前发现在癌细胞中通过融合诱导衰老在一定程度上需要p53的表达。目前观察到细胞融合的病理条件之一是癌症。化疗激活癌细胞的衰老,刺激它们“吞噬”邻近的细胞,并通过溶酶体进行处理,这为这些细胞提供了物质和能量,以维持衰老细胞所需的高代谢能力。然而,这背后的机制以及这是否是一种细胞融合形式还需要进一步研究。
除了细胞融合,细胞质桥也允许细胞之间进行生物物质交换,包括RNA、蛋白质,甚至细胞器,如线粒体和溶酶体。细胞质桥是允许相邻细胞间时空相互作用的膜延伸。目前已在多种细胞类型中发现细胞之间存在物质转移,如神经元、癌细胞和免疫细胞,也有衰老细胞。Biran等人通过对细胞培养中的氨基酸进行反式稳定同位素标记(SILAC),发现衰老细胞通过细胞质桥梁将蛋白质物质转移到自然杀伤(NK)细胞,介导其激活并增加细胞毒性。转移的蛋白主要参与肌动蛋白的细胞骨架重组和抗原提呈,并且依赖于GTPase Cdc42,但也发现了一些对NK细胞活化有重要作用的蛋白,如HSPA5和CALR。此外,蛋白质转移也发生在体内,但需要明确这种转移是通过细胞质桥还是通过额外的细胞间通讯机制来介导的。
三、生理学和病理学中的细胞间通讯
总之,已有的研究表明了在衰老和衰老过程中所发生的经典的、新发现的和非经典的细胞间通讯方式的重要性。虽然作者已经将细胞间通讯的方式分别进行了阐述,但一些细胞通讯方式在体内极有可能不是同时发生的,这将进一步取决于生物学或病理学背景。在这里,作者回顾了在特定的生理或病理情况下,哪些通讯方式是已知的衰老中存在的。此外,作者还讨论了在特定衰老背景中不同的细胞间通讯类型的作用。
(一) 细胞间通讯有助于组织稳态维持
在胎儿的发育过程中胎盘的发育尤为重要。胎盘外层之一是合体滋养层,由滋养层细胞融合形成。这种融合诱导了体外衰老的激活,并在体内的相似结构中观察到了多种衰老标记。目前没有完全研究清楚合体滋养层中的衰老机制,只能推测是防止细胞凋亡或促进胎盘母体和胚胎运输的机制。来自于滋养层细胞的细胞外囊泡可以将富含miRNA 的外囊泡转运到非滋养层细胞,通过诱导细胞自噬来抵御病毒的侵扰,这种机制在发育的过程中明显加强了细胞间的物质交流(图3A)。
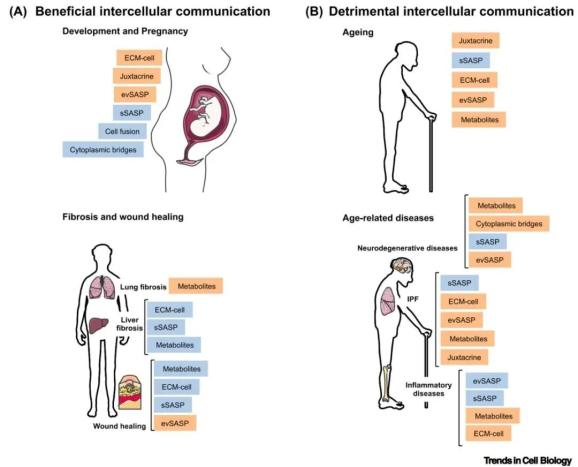
图3 生理学和衰老相关病理学中的细胞通讯。(A,B)描述了不同类型的细胞通讯方式,(A)有益于或(B)有害于组织稳态和机体健康的维持。蓝色框表明有明确的文献证据表明衰老与细胞间通讯之间的相互关联。橙色框表明有明确的文献证据表明与病理学之间的关系,而并没有显示与衰老的相互联系。(ECM,细胞外基质;evSASP,细胞外囊泡衰老相关的分泌表型;sSASP,可溶性衰老相关的分泌表型。)
衰老是发育过程中的自然现象,其中sSASP在介导巨噬细胞清除这些细胞以确保胚胎的正确形成中起着关键作用。细胞融合在sSASP诱导组织重塑及再生中起到至关重要的作用。有趣的是,TGF-β作为SASP的一部分似乎是发育衰老的关键。由于整合素和NOTCH信号调节衰老过程中的TGF-β,并且在发育中都起着关键作用,因此了解此时衰老细胞中是否发生近分泌以及ECM-细胞间通讯将是有趣的。
在特定的生理活动比如伤口愈合和纤维化的过程,衰老会抑制细胞的过度增殖以及疤痕的形成。通过整合素α6β1与ECM蛋白CCN1的相互作用,细胞在伤口愈合和肝纤维化的过程中引起ROS来诱导衰老(图2A)。再者,衰老细胞分泌出来的sSASP因子-血小板源生长因子AA(PDGF-AA)可以加速伤口的愈合。同时,肝HSCs起始衰老会招募NK 细胞以及肿瘤抑制M1 细胞可以促进组织的分解。有趣的是,在动物模型中,EVs同样可以加速伤口愈合以及疤痕的形成,同时上调NAD+保护细胞防止博莱霉素诱导的肺纤维化。总体来说,可溶性因子、生长因子、EVs以及代谢产物与ECM相互作用组成了在伤口愈合和纤维化过程中的细胞间通讯,但需要更多的实验来验证它们在衰老中的存在以及其作用。
(二) 在衰老和衰老相关疾病中细胞间通讯的有害影响
虽然癌症的发病率随着年龄的增长而增加,但已经有许多综述文章描述了癌症中的细胞间通讯,本文不再赘述。本文作者主要针对衰老和年龄相关的神经退行性疾病和炎症性疾病中的细胞间通讯进行总结。
衰老过程中发生的重要变化之一是功能失调的炎症反应,称之为“炎性衰老”,其中很多炎症因子都是sSASP中的因子。在衰老的过程中,衰老的细胞会不断的积累同时不断的释放sSASP因子,加上有缺陷的免疫系统在消除衰老细胞方面效率低下,共同导致了衰老过程中的炎症以及组织损伤。更何况不仅仅是sSASP可以导致衰老相关的功能障碍。同时衰老的组织中的细胞间基质的变化改变了ECM从而导致免疫细胞无法有效的接近并清除衰老细胞,进而导致了衰老细胞与ECM之间的相互作用,影响体内细胞的稳态,例如增殖、凋亡和迁移过程。有趣的是,根据对癌症细胞的研究类比衰老过程,发现细胞通过C/EBPβ激活的慢性促炎SASP的机制导致了NOTCH1的表达量随着年龄的增长而降低。
在衰老过程中,下丘脑干/祖细胞的衰竭是诱发小鼠衰老的重要原因。然而,使用来源于年轻祖细胞的EV治疗老年小鼠,可通过防止含miR的EV减少而缓解这些细胞数量的减少,从而改善下丘脑的相关功能。同样,用来自于年轻小鼠中富含eNAMPT囊泡处理的老年小鼠也表现出来出延迟衰老的表型,这表明EVs可能靶向衰老受体细胞中的多种通路。这是源于EVs异质性还是其他原因,亦或者是其他机制,这还需要进一步研究,EVs在老化过程中的作用仍然没有被很好的诠释。
尽管可以在EVs中找到代谢物和离子,但他们同时可以以胞外分子的形式存在。在衰老的过程中,氧化性分子(NO和ROS)的释放增加,伴随着还原因子(例如NAD+)的释放减少。总体来说,这些生物学过程导致了氧化应激的增加,这也是许多生理性衰老和复制性衰老的标志(图3B)。
衰老细胞的积累以及活跃的细胞间交流是衰老和衰老相关疾病的严重后果之一。如senolytics药物的应用可以改善多种神经退行性疾病的症状,例如阿尔兹海默症、帕金森氏症。如前所述,在衰老的过程中涉及许多不同的细胞间通讯方式,其中炎症性sSASP最典型。像阿尔茨海默氏症和帕金森氏症这样的神经退行性疾病与慢性炎症有关,但ROS和活性氮的释放以及抗氧化剂的减少也极大地促进了这些病理过程,可以增加阿尔茨海默氏症中的Aβ 沉积、帕金森氏症中的α-突触核蛋白截短和聚集。有趣的是,Aβ 和α-突触核蛋白可以通过EVs或在α-突触核蛋白存在的情况下通过细胞质桥传播到邻近的细胞。离子(如铁离子)的释放与错误折叠的蛋白质的转移会导致这些神经退行性病变。在多种神经退行性疾病刺激了小胶质细胞的、NF-κB激活的和促炎细胞因子释放的脑区均可出现铁积聚。相反,铁离子功能障碍会导致某种形式的细胞死亡,称为铁死亡。有趣的是,衰老细胞会积聚铁并改变铁的代谢。由于已经在EV中发现了转铁蛋白受体(铁的转运蛋白),因此尽管缺乏更多的实验证据,但是EV在衰老过程伴随的铁运输中的作用似乎呼之欲出。
在许多与年龄有关的炎症性疾病(如IPF、骨关节炎和动脉粥样硬化)中已发现衰老的作用,其中慢性炎症的作用已经得到了很好的阐述。在这个过程中伴随发生的是氧化物的释放以及还原物的消减。已知动脉粥样硬化、神经变性和肌肉减少症中NAD +水平降低。Jeon及其同事在最近的一项研究中发现,从衰老的软骨细胞释放出的EVs 将这种表型传递到增殖的软骨细胞中,抑制了软骨的形成并促进了骨关节炎的炎性环境。EVs 在炎症性疾病中的作用非常重要,这是由于其应激激活或诱导免疫抑制而具有免疫调节潜力。例如,从类风湿性关节炎患者的滑膜液中分离出的EVs 会引起关节发炎,而肿瘤衍生的EVs 已显示出通过CD95 配体(CD95L)肿瘤坏死因子(TNF)相关的凋亡诱导配体(TRIAL)或半乳凝素9诱导T细胞凋亡而诱导产生肿瘤抑制环境。
结语与展望
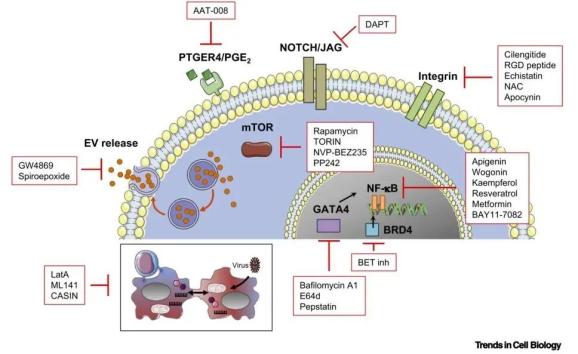
图4。药物调控细胞间通讯。已发现用来防治衰老和衰老中细胞间通讯的各种药理学抑制剂。最具代表性的药理学药物是针对可溶性衰老相关分泌表型(sSASP)的药物。通过抑制上游主调节因子(如GATA4,NF-κB或BRD4)来中和sSASP。抑制剂可以靶向与sSASP 的释放或加工有关的其他途径,例如哺乳动物的雷帕霉素(mTOR)途径靶点。另外,可以使用特定的药理学药物来阻止SASP 的各个成分,这些药物可以阻止例如细胞外囊泡SASP(evSASP)的释放或前列腺素E受体4(PTGER4)与前列腺素E2(PGE2)的结合。非经典的SASP 也可以通过阻止NOTCH / JAG途径,整联蛋白信号传导或细胞质桥的形成来抑制。(BET,溴结构域和末端外抑制剂;DAPT,N-[(3,5-二氟苯基)乙酰基] -L-丙氨酰基-2-苯基甘氨酸-1,1-二甲基乙基酯; LatA,2-噻唑烷酮大环内酯;NAC,N-乙酰半胱氨酸。)
在最近的小鼠实验中证实了衰老细胞在多种疾病中的致病性以及消极影响。通过各种延缓衰老药物选择性地去除衰老细胞的治疗已经表明,衰老细胞的消除改善了组织稳态和疾病状态。在这些病理情况下,衰老细胞的病理效应的罪魁祸首被认为是SASP。然而在正常的生理状态下,衰老细胞对组织的稳态也起到重要的作用,所以针对衰老细胞的用药要谨慎一点。另外一种可以阻止衰老细胞对环境产生消极影响的方法是控制或者中和SASP(图4)。sSASP 可以通过不同的方式进行阻断,例如抑制主要的上游调控因子(如GATA4,NF-κB和BRD4)。另外还可以通过靶向药物(例如靶向mTOR 途径的药物)抑制sSASP 的分泌和加工。最后,防止单个SASP因子的信号传递被认为是可以阻止SASP 发挥功能的另一种策略。但是,如前所述,衰老中的细胞间通讯要比最初想象的复杂很多,并不完全依赖可溶性因子。因此,很有可能存在其他尚未确定的通讯方式,这也凸显了系统识别和分析衰老和衰老中细胞通讯的迫切需求。
悬而未决的问题
(1)细胞间通讯在衰老中是否发挥着其他重要的、未知的生理作用?
(2)除了延缓衰老药物,还有什么其他抑制细胞间通讯的手段?
(3)延缓衰老药物如何影响正常生理状态下的细胞间通讯?
(4)延缓衰老药物应该在疾病过程的哪个时间节点使用?

来源:老顽童说

1980-2020
喜欢此内容的人还喜欢
原标题:《【重磅综述】衰老过程中经典和非经典的细胞间通讯》

