是时候和阿司匹林说再见了吗?

阿司匹林的一级预防,尘埃落定
对于阿司匹林用于一级预防的治疗方案,从20世纪中后期就有很多研究涌现。至2009年,ATTC协作组荟萃分析[1]提示,阿司匹林一级预防可以降低严重血管事件。但随着他汀的广泛使用和生活方式的加强管理,近期的临床研究如POPADAD[2]、ARRIVE[3]、ASCEND[4]、ASPREE[5]研究提示在未经获益和出血风险比评估的人群中,阿司匹林一级预防获益不明显。
基于以上研究,《2019 AHA/ACC心血管病一级预防指南》[6]进一步下调了无动脉粥样硬化性心血管疾病患者中应用阿司匹林的推荐力度:仅推荐对于心血管事件风险较高且不具有出血高危因素的 40~70 岁患者,可以考虑应用小剂量阿司匹林(75~100 mg/d),但仅为 IIb 级推荐(即可用、可不用但倾向于不用)。
PCI术后患者长期抗栓,阿司匹林尽早停用
近年多项研究探索PCI术后长期抗栓治疗模式,近年来逐渐明朗。今年欧洲心脏病学会科学年会(ESC2020)上,新发布的《2020 ESC 非持续性ST段抬高型急性冠脉综合征(NSTE-ACS)患者管理指南》[7]对于行经皮冠状动脉介入(PCI)术后患者单药抗栓策略参考TWILIGHT研究后作出了更新,即:综合评估缺血和出血风险后,支架术后接受DAPT治疗的患者应当考虑在3-6个月后停用阿司匹林。(IIa/A)
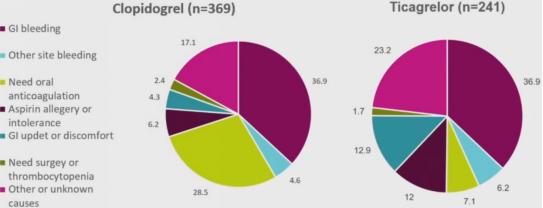
同时,ESC大会上公布的一项台湾真实世界研究[8]进一步说明了ACS患者PCI术后短期DAPT继之P2Y12受体抑制剂(氯吡格雷或替格瑞洛)长期单抗在真实世界中的现状。该研究纳入了610名ACS患者,探索该种治疗模式的疗效和安全性。
该真实世界研究探索了选择短期DAPT后停用阿司匹林的时间和原因:有69.3%的患者在PCl术后1个月内停用阿司匹林,16.1%在1-3个月内停用阿司匹林,主要原因是消化道出血。
随访12个月后观察到,相比氯吡格雷组,替格瑞洛组主要终点事件(全因死亡、再发ACS或计划外血运重建的复合终点)大幅降低(HR 0.67,95% CI 0.49-0.93;P=0.018),而两组患者的大出血(BARC 3和5型)风险无差异(HR 0.71,95% CI 0.35-1.45;P=0.345)。
从临床研究到指南推荐,再到真实世界研究,对于PCI术后患者进行短期DAPT后停用阿司匹林,进行长期P2Y12抑制剂单药抗血小板治疗方案,是基于患者综合获益的选择。阿司匹林成为可被替代的选择已是一种成熟的治疗模式。
ASCVD长期二级预防,阿司匹林依然是基石
基于ATTC协作组[1,9]荟萃分析,阿司匹林在二级预防中长期抗栓的基石地位无可撼动,指南推荐长期阿司匹林治疗。然而临床实践中,长期使用阿司匹林会有一定比例患者存在阿司匹林不耐受:20%患者存在消化道不适症状[10],60%的患者存在内镜下胃肠道损伤[11]。正如上文真实世界研究所证实:短期DAPT后停用阿司匹林的原因多为消化道安全性的问题,不利于患者长期抗栓治疗。
那对于阿司匹林无法耐受的患者,如何制定抗栓策略?
今年《柳叶刀》上一项荟萃分析[12]比较了长期抗栓时阿司匹林和P2Y12受体抑制剂的有效性和安全性:纳入9项研究、共42018例ASCVD(冠心病、脑血管疾病、外周血管疾病)患者,P2Y12受体抑制剂单药与阿司匹林单药相比,可以降低心梗事件发生风险,两者任意出血(OR 1.08,95%CI 0.91-1.29)与主要出血(OR 0.9,95%CI 0.74-1.1)并没有差异,然而在消化道出血方面,P2Y12受体抑制剂消化出血风险更低(OR 0.59,95%CI 0.39-0.89),较阿司匹林降低消化道出血相对风险41%。这样的结果在三类P2Y12受体抑制剂(氯吡格雷、替格瑞洛及噻氯吡啶)没有异质性,均保持一致。
这一结果和既往认知相同:阿司匹林会通过破坏磷脂层等方式直接损伤胃肠道粘膜,而对于循环COX酶的抑制会导致胃黏膜保护作用减少,即使剂型为肠溶片也无法完全缓解消化道损伤。
其实近年来对于阿司匹林不耐受患者的抗栓治疗,陆续有指南和共识对其进行推荐:
2016年《稳定型冠心病口服抗血小板药物治疗中国专家共识》[13]提出无禁忌症者,阿司匹林75-100 mg/长期治疗;若不能耐受阿司匹林,建议服用氯吡格雷75 mg/d,或替格瑞洛60-90 mg 2次/天。
对于阿司匹林不耐受的ASCVD患者的长期抗栓治疗中,如何选用P2Y12受体抑制剂?
这里需要注意的是,氯吡格雷存在抵抗风险。由于氯吡格雷的代谢受到ABCB1、CES1、CYP2C19、PON1及其他基因多态性影响。有数据显示[14],基因多态性导致10%-63%患者使用氯吡格雷后对抗血小板无反应或反应较差。并且,在有氯吡格雷抵抗的患者[15]中,40%发生了缺血性心血管事件。
相比之下,快速、优效、可逆且不存在药物抵抗的新型P2Y12受体抑制剂——替格瑞洛展示出了更大的优势,开始广泛受到临床的认可。
此外,一项纳入了37019名行PCI术的ACS患者进行不同P2Y12受体抑制剂联合阿司匹林治疗的研究[16],对P2Y12受体抑制剂的消化道安全性进行比较:替格瑞洛较氯吡格雷在总体ACS人群、NSTE-ACS人群和STEMI人群中的消化道出血相对风险分别降低34%、34%和37%。
且陆续有多项大型临床研究都证实,在安全性方面,替格瑞洛单药治疗总体出血发生率很低:纳入非重型急性缺血性卒中或高危TIA患者的SOCRATES研究[17]中证实替格瑞洛单药的安全性良好,主要出血发生率仅为0.5%,与阿司匹林相当(HR 0.83,95%Cl 0.52-1.34;P=0.45);纳入行PCI的ACS或稳定型冠心病患者的GlOBAL LEADERS研究[18]的12-24个月界标分析提示替格瑞洛单药治疗主要出血(BARC 3或5型)发生率仅为0.58%,与阿司匹林相当(RR 1.40,95%CI 0.89-2.19;P=0.14)。
此外,还有一项DECAB-GI研究[19]纳入了272名18-80岁、有择期冠状动脉旁路移植术(CABG)适应症的患者,旨在对比CABG后1年,替格瑞洛联用阿司匹林、单用替格瑞洛或单用阿司匹林对于上消化道黏膜的损伤。
结果显示,CABG术后1年,替格瑞洛单药治疗组严重上消化道黏膜溃疡发生率为8.8%,消化道出血发生率仅为1.3%,阿司匹林单药治疗组为14.3%和2.5%。以上结果提示,替格瑞洛消化道安全性优于阿司匹林。
总 结
综上所述,关于“是时候和阿司匹林说再见了吗”这个问题还是需要区分不同患者来看:
(1)一级预防:阿司匹林推荐降级,在ACC/AHA指南中仅推荐对于心血管事件风险较高且不具有出血高危因素的 40~70 岁患者,可以考虑应用小剂量阿司匹林(75~100 mg/d),仅为IIb级推荐
(2)对于PCI术后患者的长期抗栓:建议PCI术后3-6个月停用阿司匹林,保留P2Y12受体抑制剂进行长期抗栓治疗
(3)ASCVD患者长期二级预防:
阿司匹林仍然是基石;
但在一些特殊情况,如阿司匹林不能耐受时,可考虑使用替格瑞洛替代。
参考文献:
[1]Antithrombotic Trialists' (ATT)Collaboration. Aspirin in the Primary and Secondary Prevention of VascularDisease: Collaborative Meta-Analysis of Individual Participant Data FromRandomised Trials. Lancet. 2009; 373(9678): 1849-60.
[2]Belch J, MacCuish A, Campbell I, et al.The prevention of progression of arterial disease and diabetes (POPADAD) trial:factorial randomised placebo controlled trial of aspirin and antioxidants inpatients with diabetes and asymptomatic peripheral arterial disease. BMJ. 2008;337: a1840.
[3]Gaziano JM, Brotons C, Coppolecchia R,et al. Use of aspirin to reduce risk of initial vascular events in patients atmoderate risk of cardiovascular disease (ARRIVE): a randomised, double-blind,placebo-controlled trial. Lancet. 2018; 392(10152): 1036-1046.
[4]ASCEND Study Collaborative Group,Bowman L, Mafham M, et al. Effects of Aspirin for Primary Prevention in Personswith Diabetes Mellitus. N Engl J Med. 2018; 379(16): 1529-1539.
[5]McNeil JJ, Wolfe R, Woods RL, et al.Effect of Aspirin on Cardiovascular Events and Bleeding in the Healthy Elderly.N Engl J Med. 2018; 379(16): 1509-1518.
[6]Circulation. 2019 Sep 10;140(11):e596-e646. doi: 10.1161/CIR.0000000000000678. Epub 2019 Mar 17.
[7]Collet JP, Thiele H, Barbato E, Barthélémy O, Bauersachs J, Bhatt DL, Dendale P, Dorobantu M, Edvardsen T, Folliguet T, Gale CP, Gilard M, Jobs A, Jüni P, Lambrinou E, Lewis BS, Mehilli J, Meliga E, Merkely B, Mueller C, Roffi M, Rutten FH, Sibbing D, Siontis GCM; ESC Scientific Document Group. 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J. 2020 Aug 29:ehaa575.
[8]Wen-Han Feng,Po-Wei Chen,Ming-Yun Ho, et al. Ticagrelor Monotherapy vs Clopidogrel Monotherapy in Patients With Acute Coronary Syndrome Undergoin
[9]BMJ. 2002 Jan 12;324(7329):71-86. doi: 10.1136/bmj.324.7329.71.
[10]Yeomans ND, Lanas AI, Talley NJ, Thomson AB, Daneshjoo R, Eriksson B, Appelman-Eszczuk S, Långström G, Naesdal J, Serrano P, Singh M, Skelly MM, Hawkey CJ. Prevalence and incidence of gastroduodenal ulcers during treatment with vascular protective doses of aspirin. Aliment Pharmacol Ther. 2005 Nov 1;22(9):795-801.
[11]Aliment Pharmacol Ther. 2005 Nov 1;22(9):795-801. doi: 10.1111/j.1365-2036.2005.02649.x.
[12]Chiarito M, Sanz-Sánchez J, Cannata F, Cao D, Sturla M, Panico C, Godino C, Regazzoli D, Reimers B, De Caterina R, Condorelli G, Ferrante G, Stefanini GG. Monotherapy with a P2Y12 inhibitor or aspirin for secondary prevention in patients with established atherosclerosis: a systematic review and meta-analysis. Lancet. 2020 May 9;395(10235):1487-1495.
[13]稳定性冠心病口服抗血小板药物治疗中国专家共识[J]. 中华心血管病杂志, 2016, 44(002):104-111.
[14]Simon T, Verstuyft C, Mary-Krause M, Quteineh L, Drouet E, Méneveau N, Steg PG, Ferrières J, Danchin N, Becquemont L; French Registry of Acute ST-Elevation and Non-ST-Elevation Myocardial Infarction (FAST-MI) Investigators. Genetic determinants of response to clopidogrel and cardiovascular events. N Engl J Med. 2009 Jan 22;360(4):363-75.
[15]Matetzky, S. (2004). Clopidogrel Resistance Is Associated With Increased Risk of Recurrent Atherothrombotic Events in Patients With Acute Myocardial Infarction. Circulation, 109(25), 3171–3175.
[16]Aliment Pharmacol Ther. 2020 Jul 13. doi: 10.1111/apt.15790.
[17]Johnston SC, Amarenco P, Albers GW, Denison H, Easton JD, Evans SR, Held P, Jonasson J, Minematsu K, Molina CA, Wang Y, Wong KS; SOCRATES Steering Committee and Investigators. Ticagrelor versus Aspirin in Acute Stroke or Transient Ischemic Attack. N Engl J Med. 2016 Jul 7;375(1):35-43.
[18]Vranckx P, Valgimigli M, Jüni P, et al; GLOBAL LEADERS Investigators. Ticagrelor plus aspirin for 1 month, followed by ticagrelor monotherapy for 23 months vs aspirin plus clopidogrel or ticagrelor for 12 months, followed by aspirin monotherapy for 12 months after implantation of a drug-eluting stent: a multicentre, open-label, randomised superiority trial. Lancet. 2018 Sep 15;392(10151):940-949.
[19]Tang C, Zhu Y, Yang X, Xu B, Ye C, Yang Y, Zhong J, Zhao Q, Yu L. Upper gastrointestinal mucosal injury associated with ticagrelor plus aspirin, ticagrelor alone, or aspirin alone at 1-year after coronary artery bypass grafting. J Gastroenterol Hepatol. 2020 Oct;35(10):1720-1730.
专家简介

所带领的心血管疾病团队,在临床工作上卓有成绩,创建了目前国内设备先进、技术一流的大型心血管介入治疗中心。他在山东省率先开展心室再同步化治疗严重心力衰竭、起搏预防治疗心房纤颤等疾病,填补了山东省空白;在山东省首家急性心肌梗死绿色通道基础上建立了济南市首家国家级胸痛中心,开展了各类心脏介入手术万余例;并且创立中国房颤中心、中国心力衰竭中心等。苏国海教授在国内心血管领域有很高的知名度,近年参与了国内多部重要指南和专家共识的制定,在国内外大型学术会议授课、讲座或学术报告500余次。先后承担国家自然科学基金面上项目、国家博士后基金、山东省自然科学基金等各类科研项目20余项。带领的团队获得“济南市委济南市政府优秀创新团队”称号,获得120 万元的资助,在全球ISS竞标中成功竞标,获得260万的支持。目前作为第一主研人参与国家重大科技专项“国际规范的肿瘤免疫治疗和药物性心脏损伤临床试验关键技术平台建设”;是山东第一医科大学学术提升计划“心血管重构发生机制和干预策略研究”的骨干研究人员。获得山东省科技进步奖、山东医学科技奖、济南市科技进步奖等各类科技奖励10余项。近五年来共发表论文54篇,其中SCI收录期刊论文24篇;核心期刊发表论文30篇,参编专著1部。
主要研究方向为心肌重构及冠脉不稳定斑块的基础及临床研究,发现心肌重构的新机制及可能干预方法,不同冠脉斑块稳定性的鉴别,以及不同抗栓策略对预后的影响等。作为山东大学等高校博士及硕士研究生带教导师,共带教博士及硕士研究生40 余人。
- End -

