Cell子刊封面论文:王宗杰/陈康富等通过代谢编程促进细胞摄取细胞外囊泡,增强体内治疗效果

撰文丨王聪
编辑丨王多鱼
排版丨水成文
纳米颗粒,例如细胞外囊泡(EV),已成为癌症和炎症治疗药物的强大递送载体。尽管它们在体外表现出显著的效力,但在体内的应用却显示出有限的治疗效果。诸如细胞摄取率低和细胞特异性差等关键挑战,继续阻碍着纳米颗粒介导的递送系统的有效性。因此,要实现治疗效果,需要极高的剂量(5-50 万亿个颗粒),这在实际应用中是不切实际的。
近日,陈-扎克伯格生物研究中心、西北大学王宗杰团队(陈康富为论文第一作者),在 Cell 子刊 Cell Biomaterials 上发表了题为:Metabolic programming promotes cellular uptake of extracellular vesicles and boosts in vivotherapeutic efficacy 的研究论文,该论文还被选为期刊封面论文。论文第一作者陈康富现为北京理工大学集成电路与电子学院准聘教授。
该研究通过全面的多组学分析,确定了能增强细胞外囊泡(EV)摄取的关键代谢物和代谢途径,并配制了一种由丙酮酸和甲硫氨酸组成的代谢物混合物,将其作为“代谢物佐剂”以调控细胞代谢,从而大幅提高 EV 摄取量,增强 EV 递送的阿霉素效力并控制肿瘤。这种代谢物佐剂为提高体内纳米颗粒的递送效率提供了一种经济实惠且易于使用的解决方案。

该研究揭示了细胞代谢状态是细胞外囊泡(EV)摄取的可调门控因子,为改善体内纳米颗粒递送提供了一个实用杠杆。封面图片中,一个载有药物的 EV 沿着细胞“递送高速公路”疾驰,驶向一个发光的细胞“入口”,象征着 EV 进入目标细胞。两个标有丙酮酸和甲硫氨酸的聚光灯状球体代表通过多组学分析鉴定出的简单“代谢物佐剂”,它能在体内恢复 EV 摄取能力。通过增强细胞膜上脂筏介导的内吞作用,这种“代谢物佐剂”使 EV 摄取量提高约 150%,并增强了 EV 递送的阿霉素的抗肿瘤效果。
下一代疗法,包括基因和细胞疗法(CGT),依赖于将治疗载荷高效递送至特定细胞类型。纳米颗粒,例如细胞外囊泡(EV),已被广泛探索作为递送载体,大多数研究都集中在优化其生物物理和生化特性上,但其体内递送效率仍有限。
鉴于 EV 的摄取是 EV 与细胞之间的交互过程,研究团队推测,调控细胞状态能够增强载药 EV 的摄取和治疗效果。
在这项最新研究中,研究团队探索了细胞代谢组如何影响神经母细胞瘤细胞对 EV 的摄取。研究结果表明,EV 摄取量因细胞的代谢状况而显著不同。通过多组学分析,研究团队发现,由丙酮酸和甲硫氨酸组成的代谢物混合物可使 EV 摄取量提高 150%。在动物癌症模型中,联合使用这些代谢物佐剂,显著缩小了肿瘤体积。
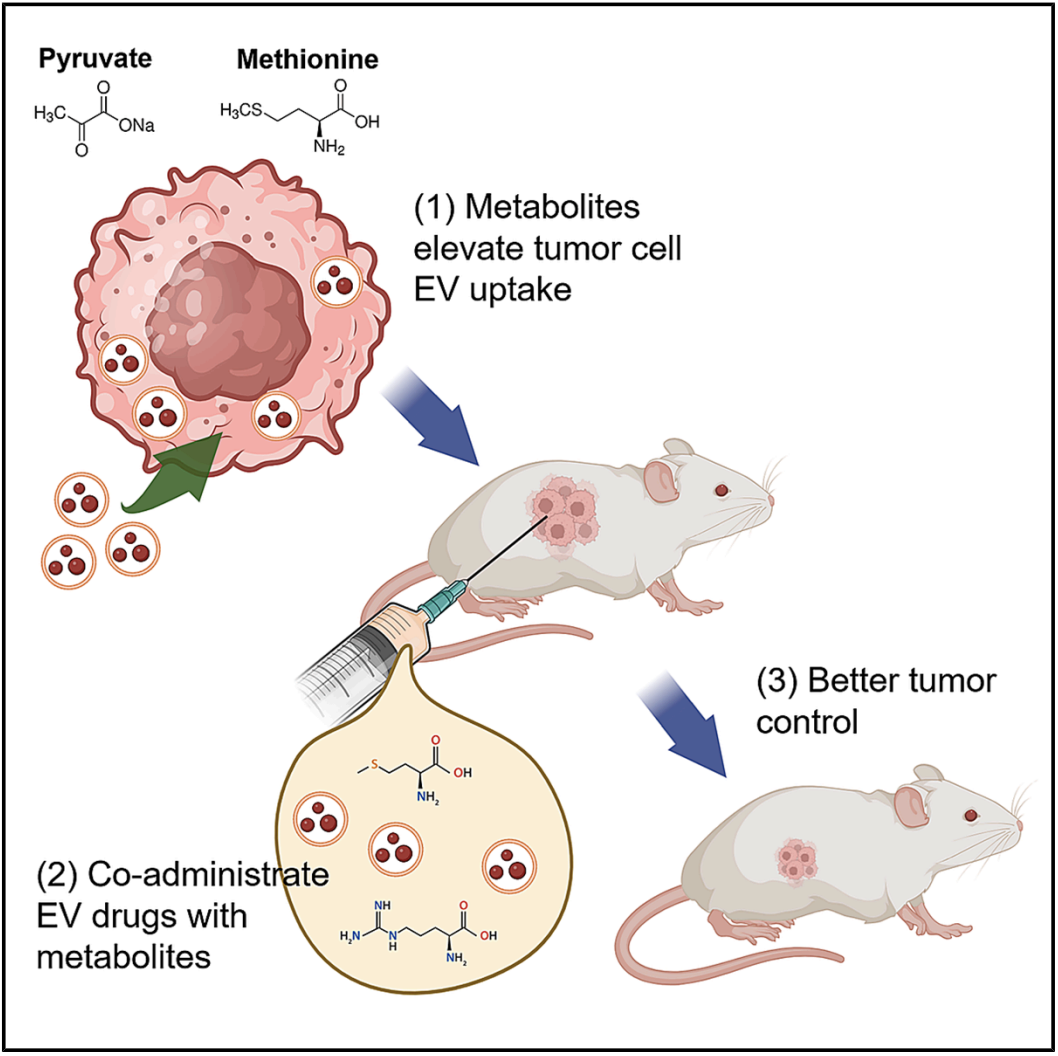
该研究的核心发现:
代谢状态是细胞外囊泡(EV)摄取的可调门控因子;
丙酮酸和甲硫氨酸代谢物佐剂使体外培养基中 EV 的摄取量增加约 150%;
代谢物佐剂可增强 EV 递送的阿霉素效力并控制肿瘤;
增强的 EV 摄取主要是由细胞膜上脂筏介导的内吞作用所驱动的。
总的来说,这项工作突显了靶向细胞代谢组以优化药物递送的潜力,并引入了一种简单直接的佐剂策略以提高纳米颗粒的体内递送效率。除了转化潜力外,这项研究还强调了在设计递送载体的同时考虑细胞行为和状态对于充分发挥基于纳米颗粒递送载体的治疗潜力至关重要。
论文链接:
https://www.cell.com/cell-biomaterials/fulltext/S3050-5623(26)00065-6
原标题:《Cell子刊封面论文:王宗杰/陈康富等通过代谢编程促进细胞摄取细胞外囊泡,增强体内治疗效果》

