浙大一院团队揭示脑结构-功能耦合异常的难治性抑郁症全新神经影像表型
难治性抑郁症(treatment-resistant depression, TRD)是精神科最棘手的临床难题之一,具有高复发率、高疾病负担和高自杀风险的特点。现有抗抑郁药物对约三分之一的抑郁障碍患者无效,而传统诊断依赖临床症状和治疗试错,缺乏早期客观识别指标,导致患者错失最佳干预时机。
近日,浙江大学医学院附属第一医院黄满丽教授联合山东第一医科大学崔栋副教授团队与浙江大学滨江研究院林博团队在npj Mental Health Research(Nature子刊)发表题为Impaired regional structure-function coupling as novel neurophenotype: mechanistic insights and diagnostic exploration in treatment-resistant depression的研究论文。该研究首次整合多模态磁共振成像技术,系统揭示了难治性抑郁症患者脑结构 - 功能耦合(structure–function coupling, SFC)的特异性异常模式,并基于机器学习构建了高精度鉴别诊断模型,为 TRD 的早期识别和个体化治疗提供了全新的神经影像学标志物。

研究背景:突破单模态研究局限,聚焦脑结构 - 功能协同
既往神经影像学研究多单独分析脑结构或功能改变,忽视了两者之间的动态交互作用。近年来研究表明,大脑功能活动并非简单映射于解剖结构,而是依赖于结构与功能的精准耦合 —— 这种耦合关系的破坏与多种神经精神疾病的发生发展密切相关。
然而,难治性抑郁症患者的脑结构 - 功能耦合特征及其与临床症状的关联仍不明确。本研究旨在验证三大核心假设:1、与健康对照相比,TRD 和非难治性抑郁症(non treatment-resistant depression, nTRD)患者存在显著的区域性 SFC 异常;2、异常 SFC 与患者的临床症状严重程度相关;3、基于 SFC 特征的机器学习模型可有效区分 TRD 与 nTRD。
研究方法:多模态 MRI 结合机器学习的严谨设计
本研究为横断面研究,经浙江大学医学院附属第一医院医学伦理委员会批准,共纳入 2023 年 1 月至 2024 年 6 月期间的 308 名受试者,包括 72 例 TRD 患者、152 例 nTRD 患者和 84 名健康对照。所有患者均符合 DSM-5 抑郁障碍诊断标准,TRD 定义为经过至少两种足量足疗程抗抑郁药物治疗后应答不佳。
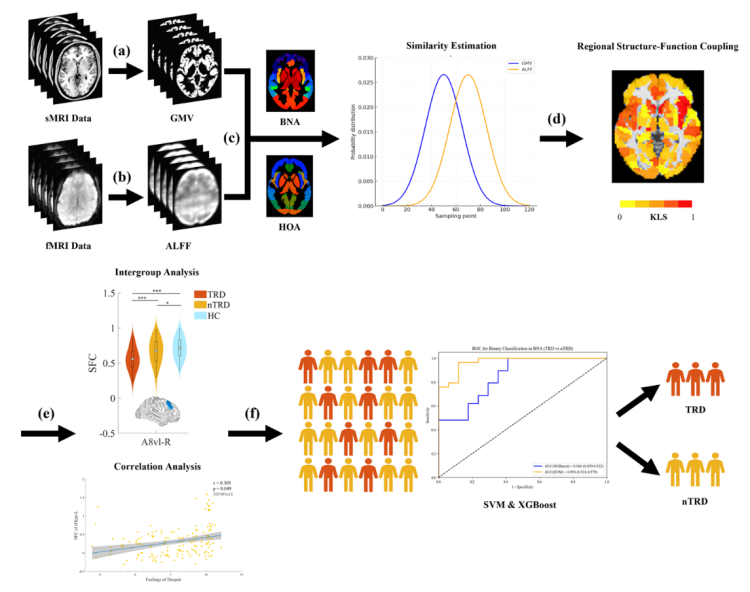
研究采用 GE 3.0T MRI 系统采集高分辨率结构像和静息态功能像数据,通过以下步骤进行分析:1、数据预处理:使用 SPM12、CAT12 和 DPARSF 软件完成头动校正、空间标准化、平滑等步骤;2、SFC 计算:提取每个脑区的灰质体积(grey matter volume, GMV, 结构指标)和低频振幅(amplitude of low frequency fluctuation, ALFF, 功能指标),基于 Kullback-Leibler 散度计算两者分布的相似性,得到区域性 SFC 值;3、统计分析:采用协方差分析比较三组间 SFC 差异,偏相关分析探索 SFC 与临床症状的关联;4、机器学习分类:使用 XGBoost 和支持向量机(Support Vector Machine, SVM)构建分类模型,通过随机划分训练集 / 测试集验证模型稳定性。
核心发现:三大突破性成果
1. TRD 患者存在特异性脑区 SFC 显著解耦
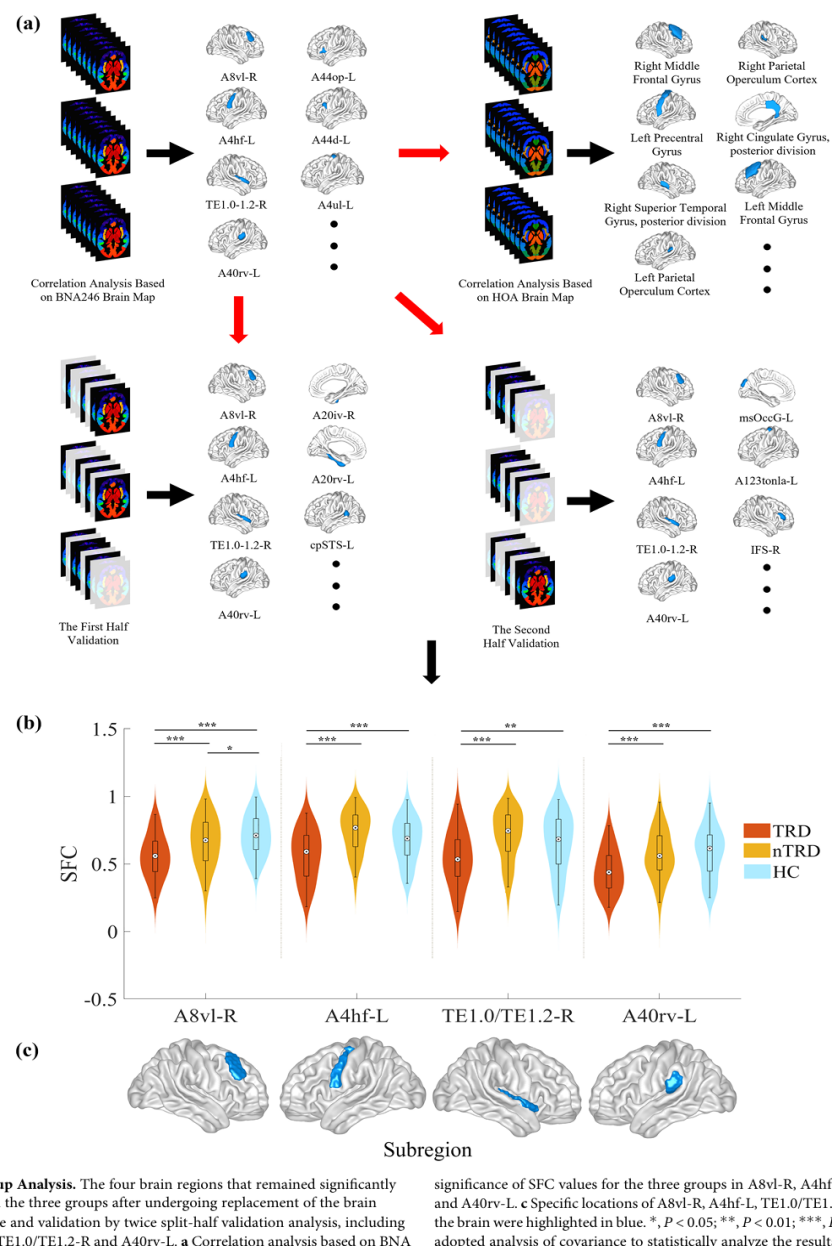
研究发现,与 nTRD 和健康对照相比,TRD 患者在以下四个关键脑区表现出显著的结构 - 功能解耦(SFC 值降低):
右侧额中回(A8vl-R):属于额顶网络,负责认知控制和目标导向行为;
左侧顶下小叶(A40rv-L):属于感觉运动网络,参与躯体感觉整合和注意力分配;
左侧中央前回(A4hf-L):属于感觉运动网络,调控运动执行和躯体表征;
右侧颞上回(TE1.0/TE1.2-R):属于感觉运动网络,参与听觉加工和社会认知。
这些结果通过替换图谱验证(BNA246与HOA脑图谱)和两次半数检验得到了重复确认,表明 TRD 患者存在认知控制和躯体加工相关脑区的结构 - 功能整合障碍。
2. nTRD 患者海马 SFC 与自杀风险密切相关
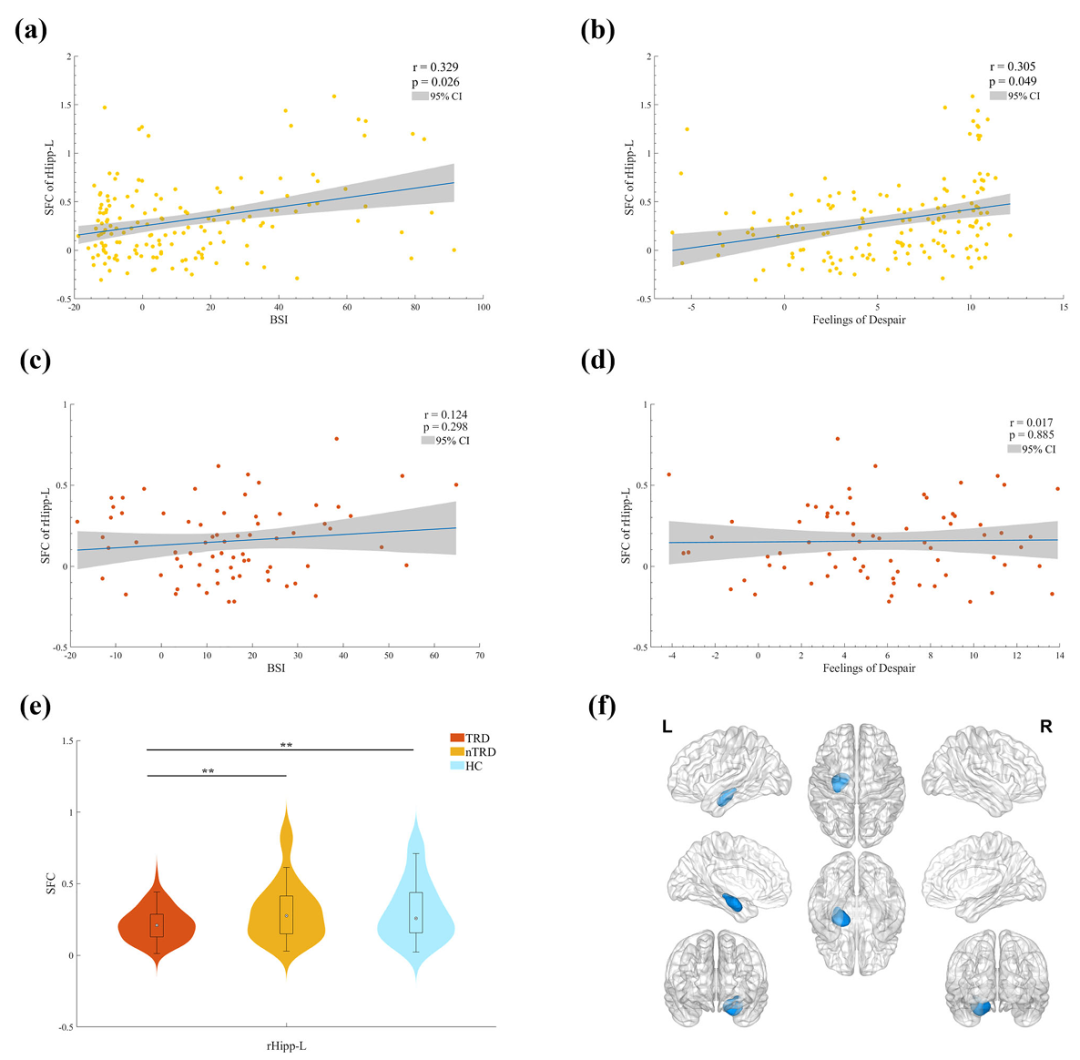
亚组分析显示,在 nTRD 患者中,左侧喙部海马(rHipp-L)的 SFC 值与自杀意念评分和绝望感评分呈显著正相关—— 即海马结构 - 功能耦合越强,患者的自杀意念和绝望感越严重。而在 TRD 患者中,这种关联完全消失。这提示抑郁症不同阶段存在不同的神经适应机制:nTRD 患者的海马 SFC 增强可能是一种代偿性反应,而 TRD 患者的广泛解耦则反映了脑网络功能的彻底崩溃,这可能是其治疗抵抗的核心神经病理基础。
3. 基于 SFC 的机器学习模型实现高精度鉴别诊断
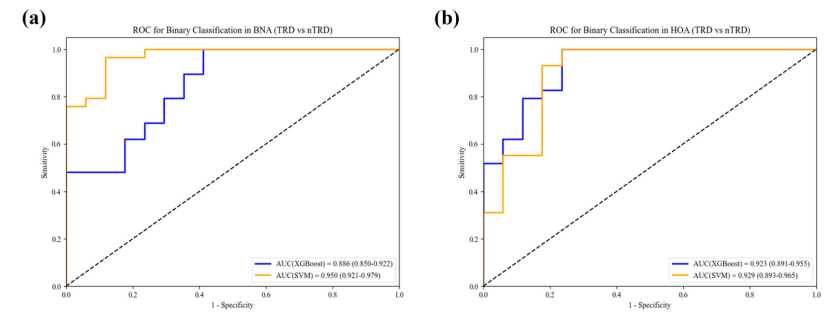
研究利用差异显著的 SFC 特征构建分类模型,结果显示:基于 BNA 脑图谱的 SVM 模型 AUC 高达0.950,XGBoost 模型 AUC 为 0.886;基于 HOA 脑图谱的两个模型 AUC 均超过 0.92;该性能显著优于既往基于临床数据或单模态影像的诊断模型。这表明脑结构 - 功能耦合特征可作为 TRD 的有效神经影像学标志物,为临床早期鉴别诊断提供了客观依据。
临床意义与未来展望
本研究首次将脑结构 - 功能耦合作为难治性抑郁症的全新神经表型,揭示了其与治疗抵抗和临床症状的内在关联,具有重要的临床转化价值。基于 SFC 的生物标志物可帮助临床医生在治疗早期识别 TRD 高风险患者,避免无效的药物试错。此外,异常 SFC 脑区(如右侧额中回)可作为经颅磁刺激等神经调控治疗的精准靶点。最后,结构 - 功能解耦的发现为理解 TRD 的病理生理机制提供了新视角,提示未来研究应关注脑网络的动态整合而非单一模态改变。
研究局限性
诚然,研究仍存在一些局限性。首先,横断面设计无法揭示 SFC 异常与疾病进展的因果关系,需进一步开展纵向随访研究。其次,研究对象均为汉族人群,结果的普适性需在其他种族中验证。第三,认知功能数据不够完整,未来可探索 SFC 与认知损害的关联。最后,样本量限制了机器学习模型的优化,未来需在更大样本中整合多组学数据提升预测性能。
作者与资助信息
浙大一院精卫中心23级八年制博士生叶欣怡和23级硕士生叶绍永为共同第一作者,黄满丽教授和崔栋副教授为共同通讯作者。本研究得到国家自然科学基金(No. 82271562)、浙江省重点研发计划(No. 2023C03077)和山东省自然科学基金(No. ZR2023MH319)的资助。研究得到了浙江省精神障碍精准诊疗重点实验室、浙江大学滨江研究院等平台的大力支持。
论文链接:https://doi.org/10.1038/s44184-026-00206-5
原标题:《【Nature子刊】浙大一院团队揭示脑结构-功能耦合异常的难治性抑郁症全新神经影像表型》

