江西省科学院王启宇/吴永明等iScience:从脂肪肝到肝纤维化,环境暴露的“加速键”被按下

交叉学科
环境暴露对健康的影响并非孤立的“有或无”事件,而是一个与机体代谢状态深度耦合、逐步加剧的动态过程。化学污染物在环境中的浓度只是风险的一面;真正决定损伤轨迹的,是个体既有的健康基础,尤其是代谢状态。当前环境毒理学的研究边界正在不断拓展。一方面,研究重点从单一污染物毒性评估,转向污染物与慢性疾病之间的协同致病效应;另一方面,研究也在深入分子层面,解析污染物在病态组织中的富集规律及其关键转运蛋白,为早期干预提供新靶点。
近日,江西省科学院(医药与健康研究所、资源与环境研究所)牵头,联合南昌大学等多家单位,在Cell Press细胞出版社旗下期刊iScience发表最新研究“F-53B exposure accelerates progression from preexisting fatty liver to non-alcoholic steatohepatitis and hepatic fibrosis”。该研究以高脂饮食诱导的MASLD(代谢功能障碍相关脂肪性肝病)雄性斑马鱼模型为对象,首次揭示:当机体已存在MASLD时,即使环境相关浓度的F-53B(一种广泛使用的PFOS替代品)也足以加速疾病向脂肪性肝炎和肝纤维化进展;机制上,MASLD导致肝脏中F-53B总负荷显著升高,而敲低肝脏型脂肪酸结合蛋白(L-FABP)可有效减轻F-53B诱导的脂质蓄积、炎症和纤维化反应。这一发现打破了“安全浓度”的静态认知,强调了代谢状态与环境暴露的强互作效应,为面向易感人群的环境健康风险评估提供了关键科学依据。
长按图片识别二维码阅读原文
研究背景
F-53B是我国电镀行业中广泛使用的PFOS替代品,在工业废水、地表水乃至人体血清中均有检出,具有极强的环境持久性和生物富集性。已有研究表明,F-53B可诱导健康动物发生肝脏脂肪变性。然而,现实世界中,全球约四分之一至三分之一的成年人患有代谢功能障碍相关脂肪性肝病(MASLD)。当已存在的MASLD再遭遇F-53B暴露,损伤是否会“火上浇油”、加速向更严重的脂肪性肝炎和肝纤维化进展?这一问题此前尚无答案。
核心发现
1、MASLD显著增加肝脏中F-53B的总负荷量
F-53B在肝脏中的生物富集浓度在正常鱼和MASLD鱼之间无显著差异,但MASLD导致肝脏体积显著增大。计算肝脏总负荷量后发现:暴露于100 μg/L F-53B时,MASLD鱼肝脏中的F-53B总量高达3623.9 ng,是正常鱼的5.8倍;即使在0.25 μg/L低浓度下,MASLD鱼的负荷量也达到正常鱼的4倍以上。更多的污染物蓄积,为后续更严重的肝损伤埋下伏笔。
2、环境相关浓度的F-53B在MASLD状态下即可诱发显著肝损伤
在正常饮食鱼中,仅最高浓度(100 μg/L)的F-53B才能显著升高血清ALT和AST水平,并诱发肝损伤。而在MASLD鱼中,低至0.25 μg/L(环境相关浓度)的F-53B即可显著加重肝脏损伤,表现为肝索结构破坏、空泡融合等病理改变,而正常鱼在同等浓度下几乎无变化。这表明,既有的MASLD使F-53B的肝毒性阈值降低了至少400倍。
3、F-53B暴露推动MASLD向肝炎和纤维化进展
F-53B暴露不仅加重肝脏脂肪变性,还促使MASLD进展为肝炎和纤维化。在MASLD鱼中,即使肝脏甘油三酯和游离脂肪酸水平不再进一步升高(已达代谢平台期),F-53B仍显著诱导:①淋巴细胞浸润密度大幅增加;②促炎因子TNF-α和IL-1β显著上调;③Masson染色显示胶原纤维沉积,纤维化标志物ColIAI、HA和PT/FII在肝组织匀浆中反而下降,这反映了可溶性前体被大量聚合成不溶性纤维基质。F-53B将病理从“量变”的脂肪堆积,推向了“质变”的炎症和纤维化。
4、敲低L-FABP可有效减轻F-53B诱导的肝损伤
肝脏型脂肪酸结合蛋白(L-FABP)是F-53B进入肝细胞的关键转运蛋白。在HepG2细胞中敲低L-FABP(效率达89%)后,F-53B诱导的甘油三酯蓄积增幅从65%降至29%,降幅超过一半;炎症因子IL-6的上升幅度从127%收窄至61%,促纤维化因子TGF-β1的上升幅度从90%收窄至22%。拦截污染物入胞,可有效缓解下游的脂质蓄积、炎症和纤维化反应,为干预策略提供了明确靶点。
总结与展望
本研究首次揭示了F-53B暴露与既有MASLD之间的“恶性协同”效应:MASLD状态下,肝脏因体积增大导致F-53B总负荷量飙升数倍,进而将肝毒性阈值降低至少400倍,使得环境相关浓度的污染物也能加速MASLD向脂肪性肝炎和纤维化进展;机制上,L-FABP是F-53B入胞的关键转运蛋白,敲低该蛋白可显著缓解脂质蓄积、炎症和纤维化反应(图1)。
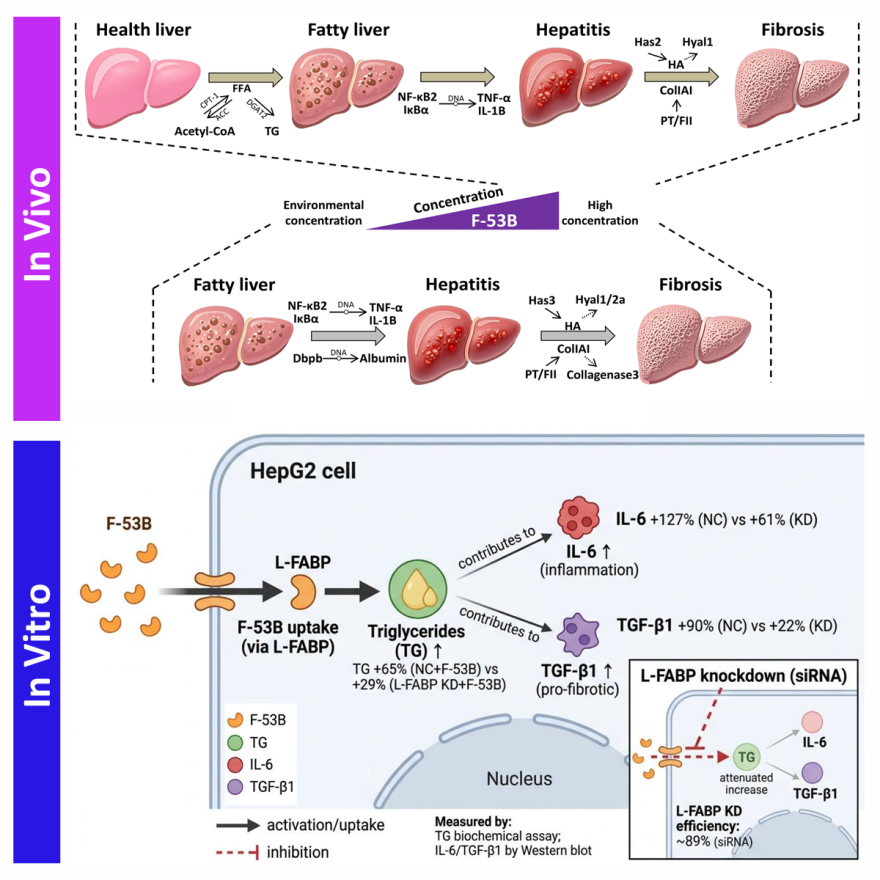
图1. 研究内容示意图
本研究为环境污染物风险评估提供了新视角——必须将人群既有的代谢性疾病状态纳入毒性评估框架。同时,L-FABP有望成为干预F-53B肝毒性的潜在靶点。后续研究应进一步在哺乳动物模型中验证这一机制,并探索真实世界混合暴露场景下的健康风险。

相关论文信息
研究成果发表在Cell Press旗下期刊iScience上
▌论文标题:
F-53B exposure accelerates progression from preexisting fatty liver to non-alcoholic steatohepatitis and hepatic fibrosis
▌论文网址:
https://www.sciencedirect.com/science/article/pii/S2589004226010503
▌DOI:
https://doi.org/10.1016/j.isci.2026.115675
原标题:《江西省科学院王启宇/吴永明等iScience:从脂肪肝到肝纤维化,环境暴露的“加速键”被按下 | Cell Press论文速递》

