抗精神病药越吃越呆?徐州医科大学发现肠菌代谢物或可挽救
生命科学
Life science
全球每年开具近7000万张抗精神病药物处方,这些药物虽能有效控制精神分裂症患者的幻觉和妄想,却常带来一个令人困扰的副作用——认知功能下降。患者和家属经常发现,服药后虽然疾病症状减轻了,但反应变慢、记忆力减退、注意力不集中等问题随之而来。长期以来,学界将这些认知损害归因于疾病本身进展或药物对神经递质的直接作用,却忽视了一个关键事实:这些药物在穿越血脑屏障之前,首先经过的是肠道,而肠道微生物是否以及在其中扮演着怎样的角色尚不清楚。
2026年4月20日,徐州医科大学于英华、黄旭枫、郑葵阳团队合作在Cell Press细胞出版社旗下期刊Cell Host &Microbe上发表了题为“Gut microbiota-derived ergothioneine alleviates antipsychotic-induced synaptic and cognitive impairments”的研究论文,该研究揭示了抗精神病药物通过耗竭肠道微生物产生的麦角硫因(强大的抗氧化剂),进而导致认知障碍,而补充这种天然抗氧化物可有效逆转药物引起的突触损伤和记忆缺陷。
从现有认知来看,精神分裂症患者本身存在肠道微生物群失调,抗精神病药物又具有抗菌活性,两者叠加使得区分疾病所致和药物所致的认知损害变得困难。但研究团队注意到一个关键线索:长期服用奥氮平等药物的患者,其肠道屏障功能明显受损,血浆脂多糖(lipopolysaccharide, LPS)水平升高,这提示系统性炎症可能是连接肠道与脑功能损伤的桥梁。更关键的是,这些肠道改变在用药早期就已出现,远早于认知损害的完全显现。
肠道屏障率先报警:药物损伤的起点不在大脑
为了厘清因果关系,研究团队设计了一套严格的实验体系。在接受持续8周的奥氮平处理后,小鼠肠道微生物组成发生显著改变:蓝细菌门显著耗竭,而变形菌门和放线菌门丰度却出现扩张。进一步的宏基因组学分析显示,谷胱甘肽代谢和组氨酸代谢通路受到严重抑制。肠道屏障功能指标全面恶化:结肠粘液层厚度减少45%,紧密连接蛋白Occludin和ZO1下调近一半,细菌与肠上皮距离缩短,血浆脂多糖水平升高。这些结果表明,慢性药物暴露不仅改变微生物生态,更破坏了肠道物理屏障。
但真正揭示因果关系的是粪菌移植实验。研究团队将奥氮平处理小鼠的粪便菌群移植到无菌健康小鼠体内,发现接受移植的小鼠不仅重现了肠道屏障缺陷,更出现了认知功能障碍,其在Y迷宫和新物体位置识别测试中表现显著下降。反之,将健康小鼠的粪便菌群移植给奥氮平治疗小鼠,则能显著改善其肠道屏障功能和认知表现。这一因果闭环实验结果证实,微生物菌群的改变是药物诱导认知损害的充分且必要条件。
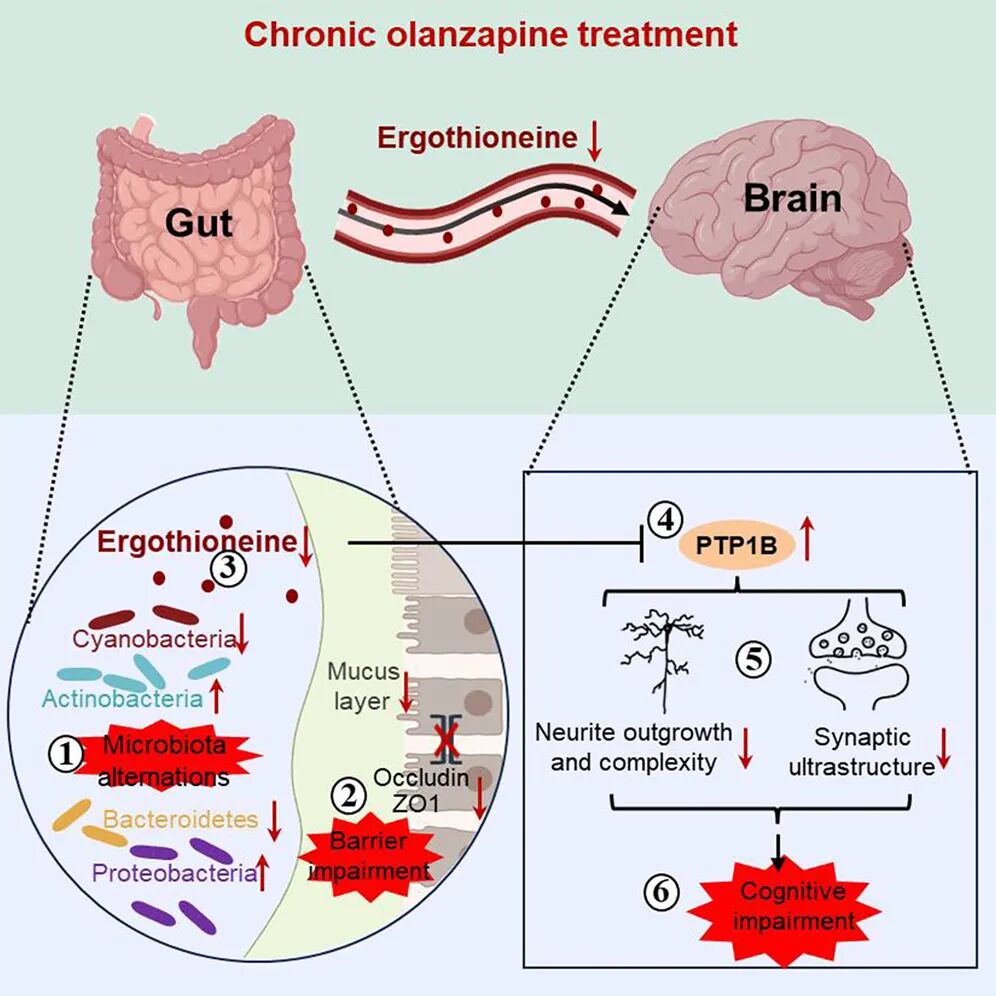
图1. 研究内容示意图
粪菌移植锁定因果:菌群改变是认知损害的条件
接下来的多组学分析将焦点锁定在一种此前被忽视的小分子——麦角硫因(ergothioneine, ET),这是一种含硫组氨酸衍生物,由特定肠道微生物通过egtBD操纵子合成,无法被人体自身合成,完全依赖饮食和微生物来源。非靶向代谢组学显示,ET是奥氮平处理后脑组织中下调最显著的代谢物。宏基因组学进一步证实,产麦角硫因的蓝细菌及其相关酶(EgtA-E、Ggt)明显减少。更加重要的是,在首次发病、未用药的精神分裂症患者中,其血液ET水平显著高于长期服用奥氮平的患者,且ET水平与认知评分呈正相关趋势。
进一步的实验结果表明,ET的神经保护机制是多层次的。他们发现,麦角硫因的缺乏会加重海马区的氧化应激,主要表现为丙二醛升高、超氧化物歧化酶活性降低,同时激活氧化还原敏感性的蛋白酪氨酸磷酸酶1B(PTP1B),而活化的PTP1B则可抑制转录因子NRF2的活性,削弱其介导的抗氧化防御,最终导致海马神经元突触结构损伤:突触后致密区变薄、突触间隙增宽、树突棘成熟度下降和认知功能障碍。不过,补充麦角硫因或神经元特异性敲除PTP1B均可有效阻断上述病理过程,提示麦角硫因-PTP1B-NRF2轴是抗精神病药物导致认知副作用的关键分子通路。体内治疗实验带来了更令人振奋的结果,补充麦角硫因可显著逆转由奥氮平等抗精神病药物诱导的认知和突触损伤。具体而言,补充麦角硫因后,小鼠在Y迷宫和新物体位置识别测试中明显改善空间记忆与物体位置辨别能力。此外,补充产麦角硫因的蓝细菌同样能够改善奥氮平引起的认知缺陷。因此,这些结果证实,补充麦角硫因或恢复产麦角硫因的菌群可有效对抗抗精神病药物所致的神经突触损伤和记忆功能障碍。
麦角硫因:被耗竭的护脑分子,补回来就能逆转损伤
更令人瞩目的是这一机制的普适性。研究团队测试了氯氮平、利培酮、氟哌啶醇、阿立哌唑等不同化学结构的抗精神病药物,发现它们均导致血液和脑组织ET水平显著降低,且耗竭程度与临床认知副作用发生率的文献报道趋势相符。ET补充对每种药物诱导的认知障碍均显示显著改善效果。
总之,这项研究打破了抗精神病药物认知副作用「不可避免」的传统认知,将其重新定义为一种可干预的“药物-微生物-代谢物-脑轴”失调。麦角硫因作为连接肠道微生物与认知功能的关键效应分子,为精神疾病的精准医学干预开辟了新途径。临床实践中,血液ET水平有望成为预测患者认知风险的生物标志物,而ET补充或产ET益生菌的联合应用,可能在不牺牲抗精神病疗效的前提下,显著改善患者的生活质量和长期预后。
不过,当前的人类证据仍局限于小样本横断面研究,尚未有前瞻性干预试验证实ET补充在人体中的有效性和安全性。此外,ET与抗精神病药物疗效的相互作用、长期使用的最佳剂量、以及在不同精神疾病亚型中的适用性,都有待更大规模的临床研究阐明。同时ET通过改善肠道屏障功能产生的系统性获益,与其直接神经保护作用的相对贡献,仍需进一步解析。
相关论文信息
研究成果发表在Cell Press旗下期刊
Cell Host &Microbe,
原标题:《Cell Host &Microbe:抗精神病药越吃越呆?徐州医科大学发现肠菌代谢物或可挽救 | Cell Press论文速递》

