北京大学邓宏魁院士领衔Cell发文揭示p53在化学重编程中发挥核心保护作用,为安全干细胞制备开辟新范式

近日,北京大学邓宏魁院士领衔在国际顶尖期刊《Cell》发表题一项重磅研究。研究发现关键肿瘤抑制因子p53在化学重编程中发挥核心保护作用,打破了“p53阻碍细胞重编程”的传统认知。揭示了p53在诱导多能干细胞生成中扮演的全新、关键角色,这从根本上改变了我们对细胞重编程安全控制机制的理解。
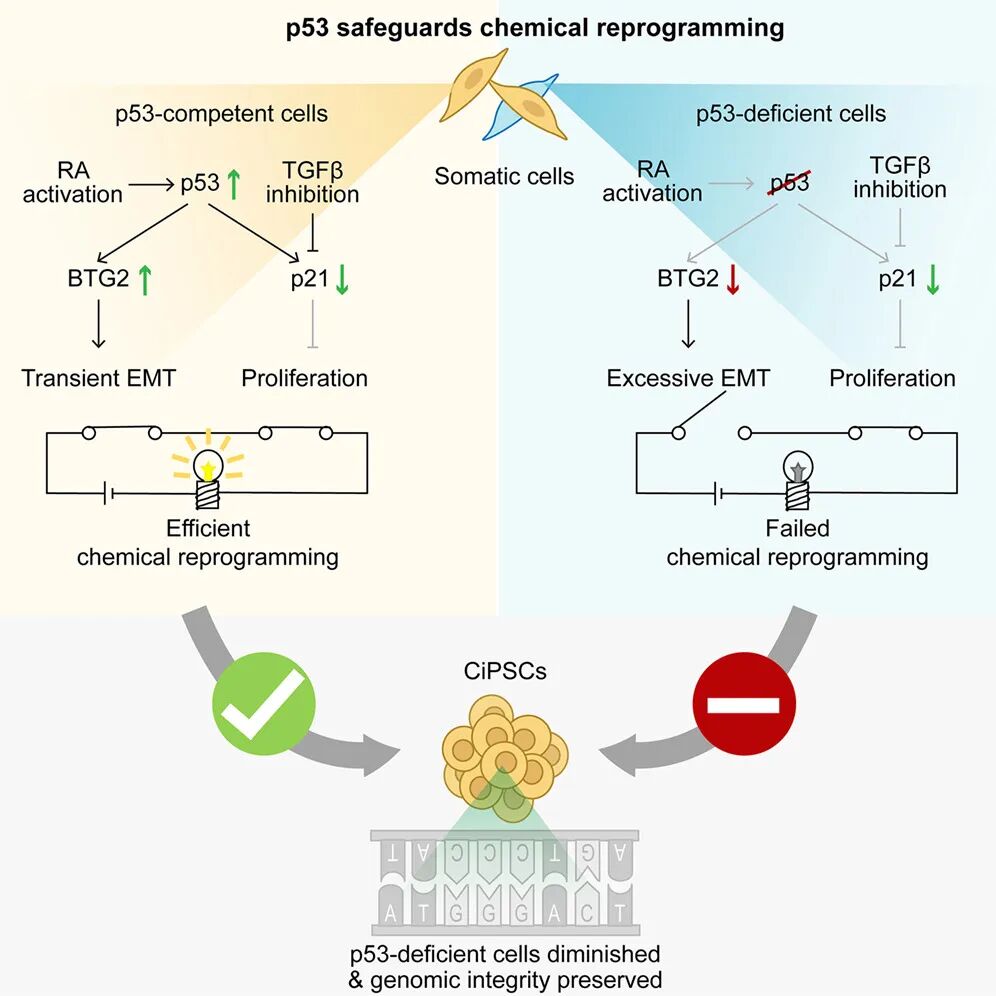
图形摘要
核心发现:p53的角色发生根本性反转
传统上,在基于“山中因子”等转录因子的重编程过程中,p53因其抑制细胞增殖的特性而被视作效率障碍,其活性常被抑制。然而,该研究显示,在完全使用化学小分子进行重编程时,p53的功能发生了根本性反转——它从“障碍”转变为不可或缺的“效率促进因子”和“基因组守护者”。 抑制p53,反而会严重损害CiPSC的生成。这一发现标志着化学重编程在底层调控逻辑上与转录因子重编程存在本质区别。
核心机制:化学小分子实现对p53功能的“精准雕琢”
研究阐明了化学重编程能够“扬长避短”、精细调控p53通路的独特优势:
利用其“抑转移”功能:重编程鸡尾酒中的视黄酸信号激活剂,可特异性通过p53下游靶点BTG2,抑制过度的上皮-间质转化(EMT),为细胞命运转变扫清障碍。
绕开其“增殖抑制”功能:同时,化学组合中的TGF-β抑制剂能够下调p53的另一关键下游因子p21,从而解除细胞周期阻滞,保证重编程所需的细胞扩增。
这种精准雕琢使得p53的基因组监控功能得以全程在线,自然淘汰掉p53功能缺陷或携带突变的异常细胞,从源头上确保了最终干细胞产物的基因组完整性。
研究意义与未来展望
这项研究的最重要意义在于,它为解决细胞重编程领域长期存在的“效率与安全难以兼得”的矛盾,提供了革命性的解决方案。化学重编程不再需要以牺牲基因组稳定性为代价来换取高效率,而是在p53这个天然“质检员”的保驾护航下,实现安全、高效、可控的细胞命运逆转。
该研究是细胞命运调控理论的重要发现,有望推动再生医学的突破性发展,在细胞治疗、体内再生与延缓衰老等研究领域具有广阔应用前景。
原文链接:
https://www.cell.com/cell/abstract/S0092-8674(26)00339-9
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
原标题:《颠覆性发现!北京大学邓宏魁院士领衔Cell发文揭示p53在化学重编程中发挥核心保护作用,为安全干细胞制备开辟新范式》

