四川大学华西第二医院周圣涛团队Trends in Immunology综述

生命科学
神经与免疫之间的相互作用已成为研究热点。子宫内膜异位症正日益被视为一种全身性疾病,其机制涉及神经与免疫细胞间复杂的相互作用,驱动着慢性疼痛和炎症。近期突破性研究揭示,异常的感觉神经生长和功能失调的免疫应答是病灶发展和疼痛持续的关键事件。
近日,四川大学华西第二医院周圣涛在Cell Press细胞出版社旗下期刊Trends in Immunology发表题为"Charting the nerve–immune axis in endometriosis"的综述性论文。该文针对近年来免疫学领域的前沿议题“神经免疫相互作用”进行了系统综述,阐述了神经免疫相互作用与子宫内膜异位症之间的功能联系,展示了神经和免疫细胞之间的相互信号如何积极地塑造上皮和基质行为,放大炎症,并加强疼痛回路。并探讨了针对关键神经-免疫节点的干预,或能为遏制病灶进展及相关慢性疼痛提供新的治疗策略。
文章共同第一作者为四川大学华西临床医学院博士研究生陆天怡、博士研究生邓峥嵘和美国克利夫兰医学中心杨楷林医师。
有兴趣在Trends in Immunology发表您的综述文章?请扫描提交论文提案 (presubmission inquiry)。
子宫内膜异位症是一种常见的妇科疾病,以异位子宫内膜样组织生长为特征的雌激素依赖性慢性炎症性疾病。其发病机制尚不完全清楚。神经免疫相互作用现在被认为是各种炎症性疾病的关键。最近伤害感受器-巨噬细胞相互作用的证据强调了神经免疫轴在子宫内膜异位症中的关键作用。本综述及时整合了这种对疾病理解的范式转变,系统描述了神经与免疫细胞的异常分布,从外周和中枢视角全面梳理了神经-免疫的交互对话。重点阐述了神经纤维、免疫细胞和上皮/基质细胞的相互网络,形成了一个强化循环,促进了子宫内膜异位症的病变生长和慢性疼痛。
神经纤维的异常分布
异常神经支配是子宫内膜异位症的一个关键特征。目前大量证据证实,子宫内膜异位病灶内存在密集的神经支配,不同亚型的子宫内膜异位症表现出不同的神经纤维分布模式。这种神经纤维密度的增加与疾病严重程度呈正相关。神经纤维包括自主神经纤维、感觉神经纤维和有髓纤维。其中,无髓的感觉C纤维是主要类型,也存在少量有髓的Aδ纤维和自主神经纤维。子宫内膜异位病灶内各亚型之间存在显著失衡,其特征是感觉神经支配增加,同时与副交感神经相比,交感神经中的自主神经纤维减少。
巨噬细胞作为子宫内膜异位症神经-免疫重塑的中枢枢纽
子宫内膜异位症的微环境中存在显著的巨噬细胞浸润。这些巨噬细胞主要通过IL-4Rα/STAT6信号通路极化为CD206+免疫抑制表型。这些免疫抑制性的巨噬细胞表现出免疫抑制、促纤维化、促血管生成和促神经血管生成的功能,从而促进病灶生长和持续性疼痛。
传统的以雌激素为中心的模型描述了一个"雌激素-巨噬细胞-神经"三联回路:雌激素促进神经元募集巨噬细胞,这些巨噬细胞随后分泌NGF、IGF-1、BDNF和NT-3等神经营养因子,进一步刺激轴突发芽。然而,新近发现揭示了更复杂的图景。CGRP/RAMP1轴是关键的神经-免疫交互范例。病灶中的血管内皮生长因子/胎盘生长因子激活伤害感受器,触发CGRP释放并与巨噬细胞上的RAMP1结合。这同时抑制了巨噬细胞的吞噬功能并诱导其产生促血管生成的VEGF-A/C/D,后者再次激活伤害感受器,从而促进病灶生长和疼痛敏化。
这些发现超越了以雌激素为中心的模型,揭示了相互关联的神经-免疫交互网络:神经肽(CGRP/P物质)激活巨噬细胞,后者释放促进神经敏化的神经营养因子,形成自我强化的循环,并为新的治疗靶点(如CGRP/RAMP1)提供了依据(图1)。
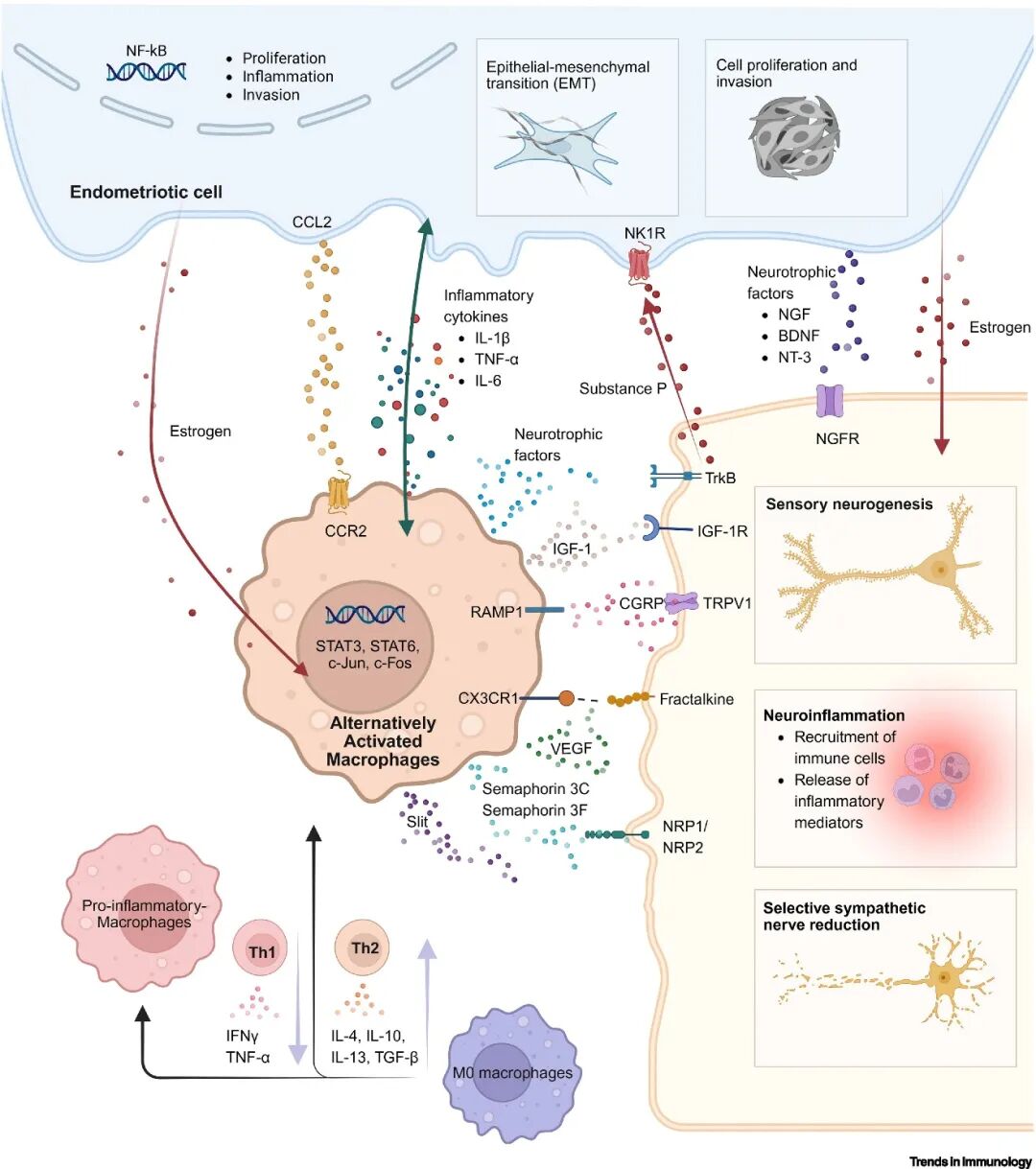
图1 子宫内膜异位症病变中巨噬细胞与神经纤维之间可能的交叉对话
神经与免疫细胞相互作用促进疾病进展
外周神经系统与免疫细胞之间的相互作用在子宫内膜异位症的发病机制中至关重要。这种交互是双向的:活化的神经元释放神经肽(如P物质、降钙素基因相关肽)以募集免疫细胞;反之,免疫细胞分泌神经营养因子(如神经生长因子、脑源性神经营养因子)以促进神经元生长和敏化。这种相互作用驱动疾病进展,涉及神经源性炎症和免疫介导的神经重塑,最终导致外周敏化和中枢敏化(图2)。
感觉神经元活化引起的神经源性炎症是疾病的关键特征,不仅与疼痛相关,还促进疾病进展。感觉神经可分泌P物质和降钙素基因相关肽,分别通过神经激肽1受体和降钙素受体样受体/RAMP-1轴发挥作用,进一步诱导上皮-间质转化、平滑肌分化及病灶纤维化。反之,子宫内膜异位症间质细胞和上皮细胞分泌神经营养因子,促进神经发生,并调控神经纤维比例的失衡。
免疫细胞通过分泌炎症介质推动疾病进展。巨噬细胞释放IL-1家族细胞因子、TNF-α和TGF-β,增强间质细胞的黏附、迁移和增殖能力。活化的肥大细胞释放组胺、TNF-α、神经生长因子、IL-6和CCL8,其中后者通过CCR1促进上皮细胞增殖、迁移和纤维化。因此,免疫细胞通过协同的炎症和血管生成机制促进子宫内膜异位症的进展。随着疾病进展,微环境转向免疫耐受状态。子宫内膜异位间质细胞促进了这种免疫逃逸状态,来源于子宫内膜异位间质细胞的乳酸通过Mettl3/Trib1/ERK/STAT3通路诱导巨噬细胞免疫抑制特性增强且吞噬能力下降。间质细胞还分泌IL-15,触发杀伤活性较低的CD16⁻CD56⁺自然杀伤细胞分化。因此,上皮/间质细胞与免疫细胞之间的双向对话也是驱动疾病进展的关键因素。
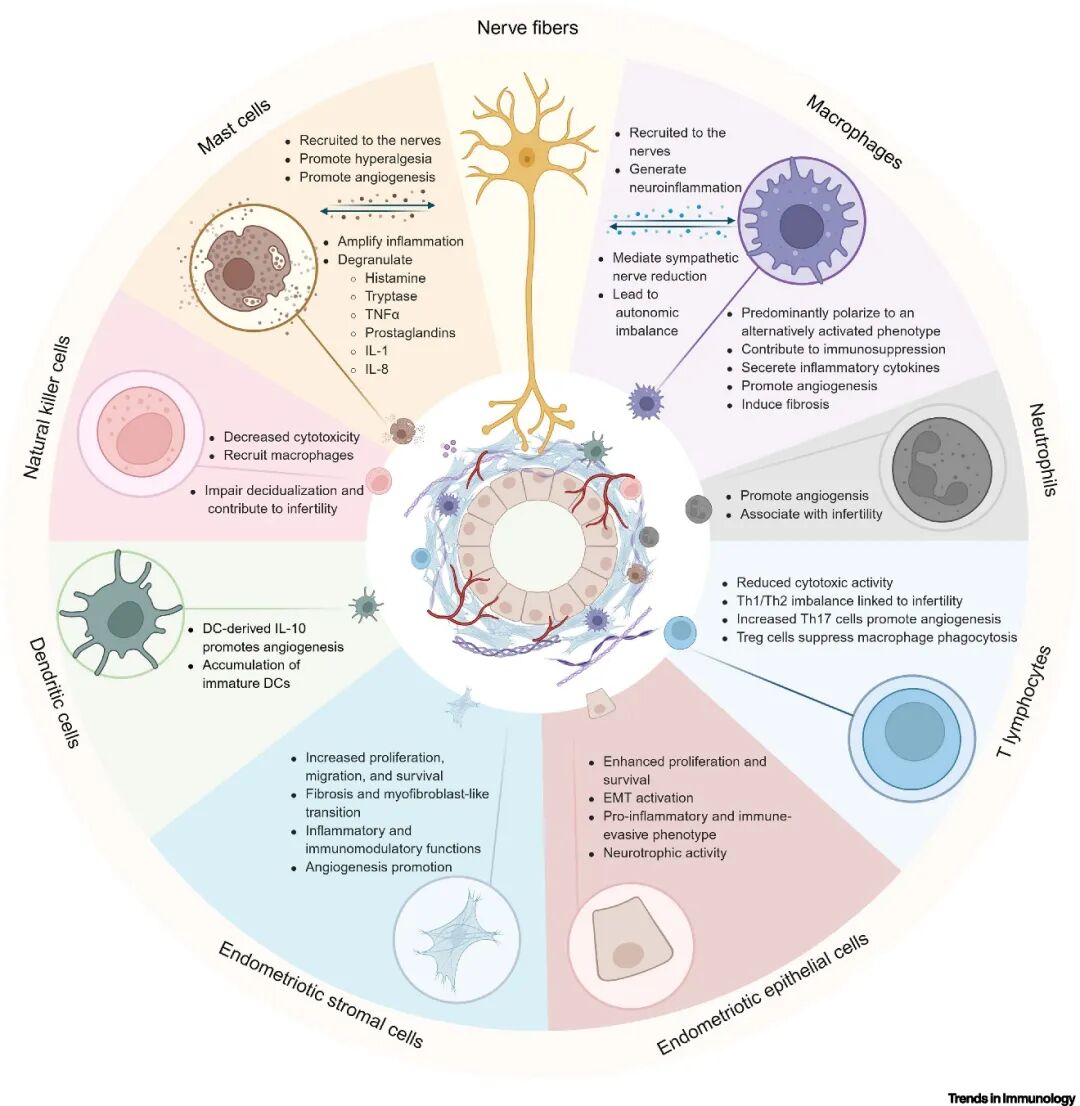
图2 神经免疫相互作用共同促进疾病的进展
结语
本综述阐述了神经纤维和免疫细胞与子宫内膜异位病灶中的上皮细胞及间质细胞相互作用,共同塑造了炎症和纤维化的微环境。形成了一个促进子宫内膜异位症病灶生长和慢性疼痛的强化循环。展望未来,我们对神经-免疫-间质相互作用的分子机制需要进行系统性地解析。研究应结合最前沿的多学科整合方法,包括单细胞与空间转录组图谱分析、神经-病灶与神经-免疫共培养系统,结合动物体内模型来描绘神经-免疫-间质网络。在临床转化方面,针对神经-免疫轴多个节点的联合疗法可能比单一靶点方法更有效。未来子宫内膜异位症的临床研究应根据以下维度对患者进行分层:病灶神经纤维表型、病灶免疫组成、循环及脑脊液神经免疫生物标志物,以及疼痛表型分类。这些生物标志物应在个体患者层面上与临床试验结果前瞻性关联,从而识别哪些机制、通路在个体患者中是限速性的或多余的,并实现新疗法的机制靶点与患者表型的匹配。通过这些协同努力,我们可以朝着新的治疗范式迈进,不仅缓解症状,更能真正改变子宫内膜异位症的疾病进程。

论文作者介绍

周圣涛
教授
周圣涛,教授,博士生导师,国家杰出青年基金获得者,四川大学华西第二医院党委委员,妇科副主任。国家重点研发计划青年首席科学家,2030四大慢病重大研究计划首席科学家,曾获得四川省自然科学一等奖(第一完成人),国之名医青年新锐奖,教育部霍英东青年科技一等奖,中国肿瘤青年科学家奖,首批何享健青年科学基金。担任中华医学会妇科肿瘤分会常务委员,中国抗癌协会青年理事会常务理事等。带领团队长期从事妇产科相关疾病免疫微环境分子机制及靶向治疗相关基础与临床转化研究,近年来以通讯作者身份在Cancer Discovery(3篇)、Nature Cancer、Science Advances、Genome Biology、PNAS(2篇)等国际期刊发表多篇研究论文。
相关论文信息
相关研究发表在Cell Press细胞出版社
旗下期刊Trends in Immunology
▌论文标题:
Charting the nerve–immune axis in endometriosis
▌论文网址:
https://www.sciencedirect.com/science/article/abs/pii/S1471490626000086
▌DOI:
https://doi.org/10.1016/j.it.2026.01.005
原标题:《四川大学华西第二医院周圣涛团队Trends in Immunology综述 | 子宫内膜异位症的神经-免疫轴解析》

