中国科学院分子细胞科学卓越创新中心童明汉团队:哺乳动物减数分裂DNA双链断裂形成的机制和调控

生命科学
减数分裂同源重组起始于SPO11-TOP6BL及其辅助蛋白介导的程序性DNA双链断裂(double-strand break,DSB)。DSB的分布具有偏好性,那些高频发生DSB的区域被称为热点。在大多数哺乳动物中,热点由减数分裂特异性组蛋白甲基转移酶PRDM9决定。减数分裂DSB形成的精确时空调控对于遗传多样性和基因组稳定性的维持至关重要。该过程的异常会导致异常重组、染色体错误分离和生殖障碍。
中国科学院分子细胞科学卓越创新中心的童明汉研究员团队在Cell Press细胞出版社旗下期刊Trends in Biochemical Sciences发表了题为“Mechanism and regulation of meiotic double-strand break formation in mammals”的综述,第一作者是童明汉课题组的博士后汤辛哲。该文全面总结了减数分裂DSB形成近期在遗传学、生物化学和结构生物学方面的进展,并特别介绍了哺乳动物减数分裂DSB形成的分子调控机制。
有兴趣在Trends in Biochemical Sciences发表您的综述文章?请扫描提交论文提案 (presubmission inquiry)。
减数分裂同源重组的分子机制概述
减数分裂是一种存在于有性生殖生物中特殊的细胞分裂方式,其特点是DNA复制一次,细胞连续分裂两次,最终产生单倍体配子。根据两次细胞分裂的顺序,可将减数分裂划分为减数第一次分裂和减数第二次分裂。同源重组是减数第一次分裂中最重要的生物学事件,它确保了来自父母双方的遗传物质的交换。减数分裂同源重组起始于SPO11-TOP6BL及其辅助蛋白介导的DSB形成[1, 2]。DSB形成后,SPO11会共价连接在DNA缺口处的5'末端,随后在MRE11(具有核酸内切酶和3'→5'核酸外切酶活性)的帮助下释放。之后,5'→3'核酸外切酶EXO1对断裂DNA的5'末端进行进一步加工,形成一个长的3'单链DNA(ssDNA)尾巴[3]。RPA复合体首先结合在该ssDNA上,随后被DMC1和RAD51替换,形成核酸蛋白纤维。这些核酸蛋白纤维将会侵入同源染色体,形成置换环(D-loop)。大部分D-loop通过合成依赖性链退火(synthesis-dependent strand annealing,SDSA)修复为非交叉(non-crossover,NCO)。少部分D-loop会通过第二链捕获形成双霍利迪连接体(double Holliday junction),最终大部分被修复为交叉(crossover,CO)。交叉的形成会导致大片段的DNA发生交换。只有少部分DSB会被修复为交叉(图1)。
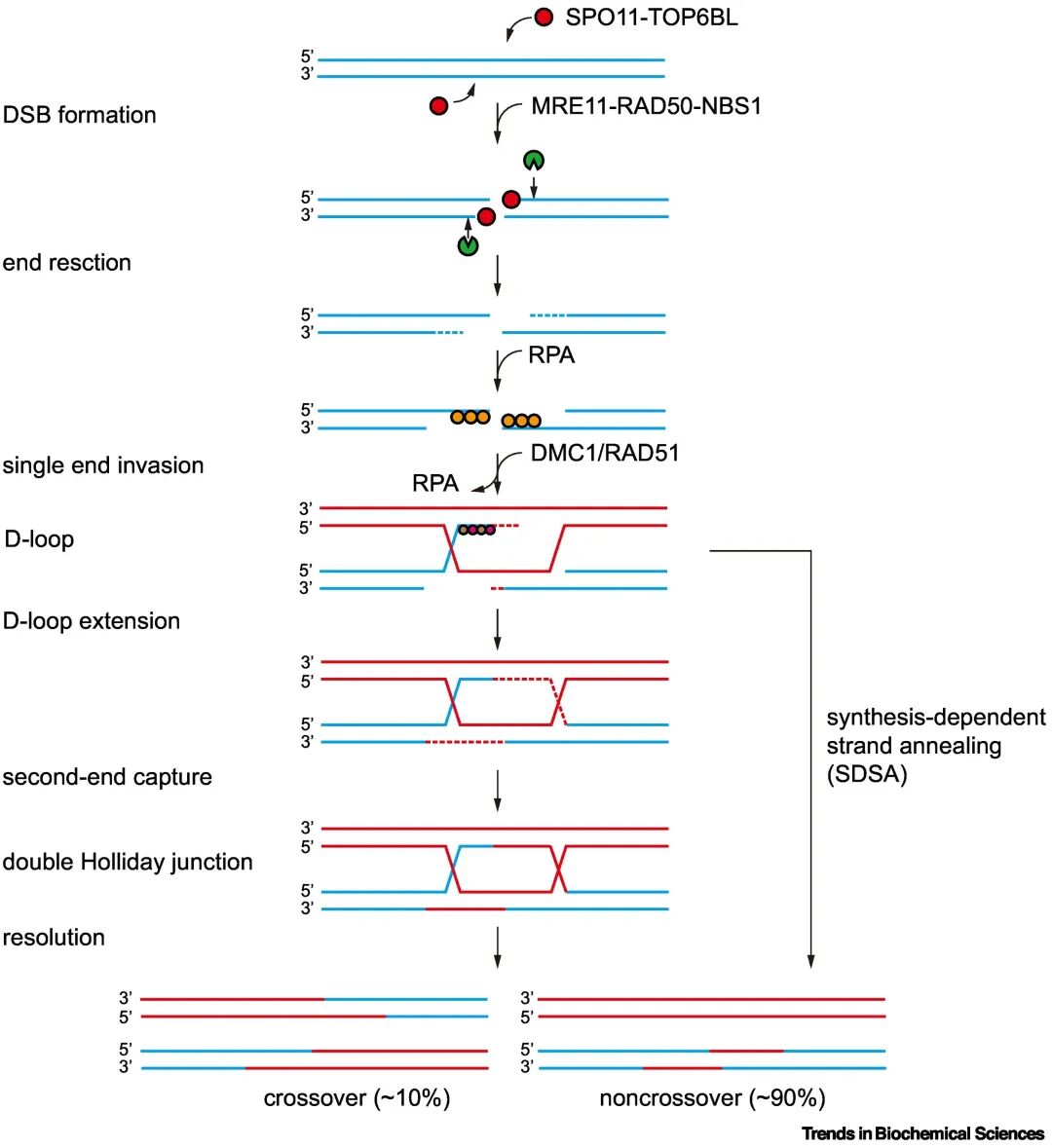
图1 同源重组的分子机制
减数分裂重组由SPO11介导的DNA双链断裂形成所引发。DSB形成,SPO11通过磷酸酪氨酸键共价结合在断裂DNA的5'末端,随后被MRE11-RAD50-NBS1复合物(具有核酸内切酶和3'→5'核酸外切酶活性)切除,产生5'末端。这些5'末端再由5'→3'核酸外切酶进一步切割,形成长的3'单链DNA突出末端。3'单链DNA首先被RPA复合体包被,随后由重组酶DMC1和RAD51替代,形成核酸蛋白纤维。这些核酸蛋白纤维会搜寻同源序列并侵入同源染色体上的同源双链,形成D-loop,这一过程称为单链侵入。大部分D-loop通过SDSA修复,产生NCO。少部分D-loop通过第二链捕获形成dHJ。dHJ可被解离为CO或NCO;在减数分裂中,dHJ偏好解离为CO。
减数分裂DSB形成具有显著的空间特异性。在减数第一次分裂前期,染色体组装为稳定的“轴-环”结构——染色体环的基部锚定于由减数分裂特有蛋白和粘连蛋白构成的染色体轴上,而环部则游离向外延伸。DSB并非随机发生于整个基因组,而是倾向于聚集在被称为“热点”的特定区域。越来越多的证据表明,这种DSB的位点选择与形成过程,受到染色质三维结构的严密调控。
热点的生物学特点
1. 热点的分布
DSB的形成是非随机性,而是偏好在某些特定区域,被称为热点。高通量测序结果揭示,小鼠基因组约有1.5-2万个DSB热点,而人类则有3-4万个。热点活性差异可达千倍,但每个精母细胞实际仅形成约200-300个DSB,卵母细胞约250-300个,说明每次减数分裂只使用一小部分潜在热点。DSB位点的选择机制是领域的未解之谜。
2. 热点的调控
DSB的数量、分布以及修复的结局对基因组的稳定性至关重要,因此必须受到严格精细地调控。在多数哺乳动物中,PRDM9决定了DSB热点。在第一次减数分裂前期,PRDM9首先通过其锌指结构域,与热点基序结合;随后,它的SET结构域甲基化附近的核小体,使染色质转换为开放状态,随后招募DSB形成复合体至热点,以催化DSB形成。
DSB的分布还受DNA损伤应答激酶(DDR)ATM和ATR调控。ATM/ATR能抑制已形成DSB的位点附近形成DSB,从而确保基因组的稳定性,这一现象被称为DSB干扰。在小鼠中敲除Atm,会导致DSB数量增加至10倍,从而导致基因片段的丢失[4]。
DSB形成的分子机制
DSB形成的分子机制在不同物种间高度保守,在几乎所有已研究的物种中,DSB由保守的Spo11催化。Spo11是拓扑异构酶VI A亚基的同源物。在芽殖酵母中,DSB形成至少还需要其它9个蛋白的帮助,它们分别是:Rec102,Rec104,Ski8,Rec114,Mei4,Mer2,Mre11,Rad50,Xrs2,它们与Spo11构成了DSB形成复合物。DSB形成复合物可以分为三个部分,Spo11核心复合体(Spo11-Rec102-Rec104-Ski8),RMM复合体(Rec114-Mei4-Mer2)和MRX复合体(Mre11-Rad50-Xrs2)。除了Ski8外,哺乳动物中能找到上述所有蛋白的同源物,例如,Rec102-Rec104的同源物是TOP6BL,Mer2的同源物是IHO1,MRX的同源物是MRE11-RAD50-NBS1。在小鼠中敲除上述任一基因均会导致严重的减数分裂障碍。
1. SPO11-TOP6BL复合体
Spo11催化DSB形成的核心酶,最初于1997年在芽殖酵母中被发现,在小鼠中的同源物是SPO11。SPO11是拓扑异构酶VI A亚基的同源物,拓扑异构酶VI通常以A2B2的形式(即两个A亚基和两个B亚基形成的异源四聚体)发挥功能。在减数分裂中拓扑异构酶VI B亚基的同源物是TOP6BL。当SPO11切割DNA时,其保守的酪氨酸残基(小鼠中为Y138)会进攻DNA的磷酸二酯键,与DNA的5’末端形成稳定的磷酸酪氨酸键,这一过程需要Mg2+或Mn2+的帮助。在DSB形成中,TOP6BL的功能暂未完全明确,有报道称TOP6BL能与RMM复合体中的REC114互作,提示TOP6BL的作用可能是将SPO11和RMM相联系[5-7]。
2. RMM复合体
DSB的形成还受REC114,MEI4和IHO1的调控,然而其中的分子机制尚未明确。在芽殖酵母中,Rec114-Mei4和Mer2能以液-液相分离的形式形成液滴,从而招募Spo11至热点切割DNA[8]。在哺乳动物中,REC114-MEI4和IHO1是否以类似机制参与调控DSB形成目前仍未明确。结构生物学的研究表明,REC114的PH结构域能和TOP6BL的C端互作,提示REC114-MEI4-IHO1对SPO11-TOP6BL有招募作用[9]。另一方面,IHO1能与染色质轴元件HORMAD1互作,这一过程受磷酸化激酶CDC7的调节,提示RMM复合体可能是SPO11-TOP6BL和轴连接的桥梁[10]。
3. MRN复合体
MRN/X复合体是一类高度保守的复合体,对体细胞和生殖细胞中DSB的识别和修复至关重要。尽管MRN/X在DSB的加工过程中是必需的,然而其在减数分裂DSB形成中的功能并非保守:MRN/X参与酿酒酵母和秀丽隐杆线虫的DSB形成,却不参与裂殖酵母、拟南芥和小鼠的DSB形成。
从PRDM9到染色体轴:连接热点与DSB形成的分子机制
DSB的形成发生在减数分裂特异性的轴环结构上:热点在环上,而DSB形成复合物在轴上。在DSB形成时,环上的热点被拉向染色体轴,形成“环挤压结构”(tethered loop-axis complex,TLAC)。在芽殖酵母中,Spp1是维持这一结构的关键蛋白质。Spp1一方面与决定酵母DSB热点的COMPASS复合体相互作用,另一方面结合RMM复合体中的Mer2;而Mer2又通过与轴蛋白Hop1的直接互作,最终实现了"热点决定-DSB形成-染色体轴锚定"的偶联机制。
在哺乳动物中,虽然已知DSB形成复合物与染色体轴通过RMM与HORAMD1和TOP6BL之间的互作实现(见RMM复合体),但仍未发现连接热点决定因子PRDM9和DSB形成复合物的关键分子。PRDM9如何调控DSB形成复合物(SPO11-TOP6BL和RMM等)以及如何与染色体轴发生动态互作,其底层分子机制仍有待解析,是未来阐明哺乳动物减数分裂重组调控的关键所在(图2)。
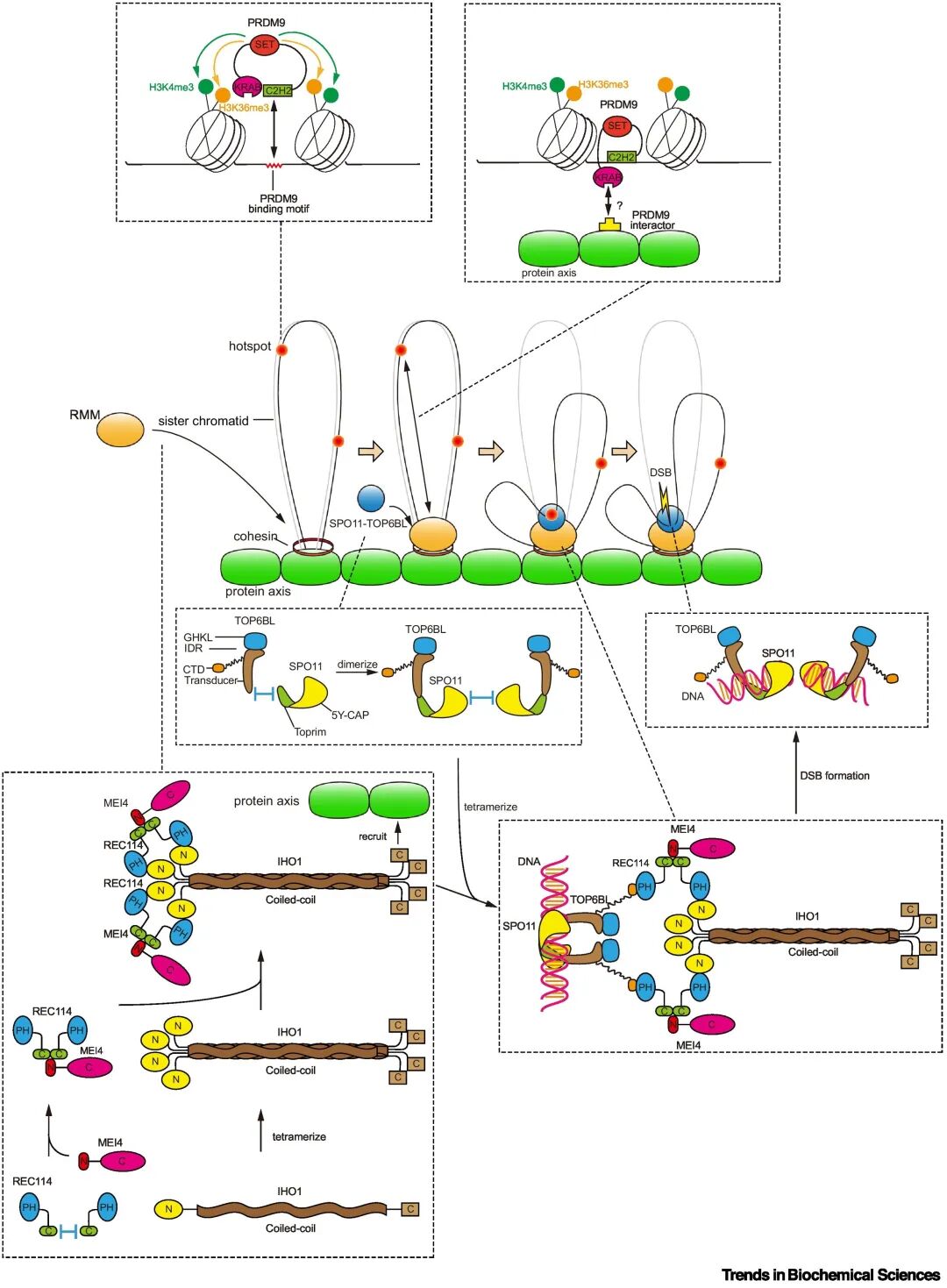
图2 哺乳动物DSB形成的分子机制
在减数第一次分裂前期,PRDM9通过其C2H2锌指结构域识别热点序列,从而与热点DNA结合,随后通过某种目前未知的方式将环上的热点拉向轴。与此同时REC114-MEI-IHO1组装成复合体,锚定至轴的过程中同时招募SPO11-TOP6BL复合体,后者对被拉向轴的热点进行切割,最终形成DSB。
总结与展望
近期研究进展极大地深化了我们对哺乳动物减数分裂DSB形成及其调控机制的理解。基因组学、生物化学与结构生物学的研究为我们揭示了SPO11–TOP6BL复合物及其辅助因子(包括REC114、MEI4和IHO1)之间的相互作用,以及DSB形成复合物通过HORMAD1与染色体轴偶联的机制。这些突破为进一步探究这些相互作用的调控方式,以及它们如何激活SPO11–TOP6BL复合体奠定了坚实基础。值得注意的是,利用重组小鼠SPO11-TOP6BL复合体在体外成功重构减数分裂DSB的形成,为深入解析DSB形成的分子机制提供了一个易于操控的全新平台,必将引领该领域新一轮的研究浪潮[5-7]。
尽管取得了上述进展,关键科学问题依然待解。例如:PRDM9如何将DSB形成复合物招募至热点和/或染色体轴?哪些分子调控哺乳动物减数分裂轴-环结构以及TLAC的组装?TLAC又如何调控DSB形成的时空分布?未来,结合体外生化重组系统和突变导向的结构分析,将为我们绘制减数分裂DSB形成的精细分子图谱。
本文参考文献(上线划动查看)
1. Keeney, S. et al. (1997) Meiosis-specific DNA double-strand breaks are catalyzed by Spo11, a member of a widely conserved protein family. Cell88 (3), 375-84.
2. Bergerat, A. et al. (1997) An atypical topoisomerase II from Archaea with implications for meiotic recombination. Nature386 (6623), 414-7.
3. Arter, M. and Keeney, S. (2024) Divergence and conservation of the meiotic recombination machinery. Nat Rev Genet25 (5), 309-325.
4. Paiano, J. et al. (2020) ATM and PRDM9 regulate SPO11-bound recombination intermediates during meiosis. Nat Commun11 (1), 857.
5. Oger, C. and Claeys Bouuaert, C. (2025) SPO11 dimers are sufficient to catalyse DNA double-strand breaks in vitro. Nature639 (8055), 792-799.
6. Zheng, Z. et al. (2025) Reconstitution of SPO11-dependent double-strand break formation. Nature639 (8055), 784-791.
7. Tang, X. et al. (2025) In vitro reconstitution of meiotic DNA double-strand-break formation. Nature639 (8055), 800-807.
8. Claeys Bouuaert, C. et al. (2021) DNA-driven condensation assembles the meiotic DNA break machinery. Nature592 (7852), 144-149.
9. Nore, A. et al. (2022) TOPOVIBL-REC114 interaction regulates meiotic DNA double-strand breaks. Nat Commun13 (1), 7048.
10. Dereli, I. et al. (2024) Seeding the meiotic DNA break machinery and initiating recombination on chromosome axes. Nat Commun15 (1), 2941.

相关研究发表在Cell Press细胞出版社旗下期刊
Trends in Biochemical Sciences
▌论文标题:
Mechanism and regulation of meiotic double-strand break formation in mammals
▌论文网址:
https://www.sciencedirect.com/science/article/abs/pii/S096800042600006X
▌DOI:
https://doi.org/10.1016/j.tibs.2026.01.006
原标题:《中国科学院分子细胞科学卓越创新中心童明汉团队Trends in Biochemical Sciences综述丨哺乳动物减数分裂DNA双链断裂形成的机制和调控》

