痴呆新解法!河北医科大学王珊团队揭示CH-I如何阻断阿尔茨海默病中的铁死亡


铁死亡是一种铁依赖性的脂质过氧化驱动的程序性细胞死亡途径,已被证实与阿尔茨海默病(AD)的发生发展相关。然而,铁死亡在AD发病机制中的具体作用尚不清楚。
基于此,河北医科大学第二医院神经内科王珊研究团队在《European Journal of Pharmacology》杂志发表了“Cerebroprotein hydrolysate-I ameliorates cognitive dysfunction in APP/PS1 mice by inhibiting ferroptosis via the p53/SAT1/ALOX15 signalling pathway”揭示了脑蛋白水解物-I通过p53/SAT1/ALOX15信号通路抑制铁死亡改善APP/PS1小鼠的认知功能障碍。

本研究发现,脑蛋白水解物-I(CH-I)可显著改善APP/PS1阿尔茨海默病(AD)小鼠的认知功能,减轻Aβ沉积和tau蛋白过度磷酸化。机制研究表明,CH-I通过抑制铁死亡发挥神经保护作用:它有效降低海马中脂质过氧化、亚铁离子和活性氧水平并逆转铁死亡关键基因(如SLC7A11、SAT1、GPX4)的异常表达。进一步分析揭示,p53/SAT1/ALOX15信号通路在AD中被激活并驱动铁死亡,而CH-I能显著抑制该通路的活化。因此,CH-I通过靶向p53/SAT1/ALOX15轴缓解铁死亡,为AD治疗提供了新思路和潜在靶点。
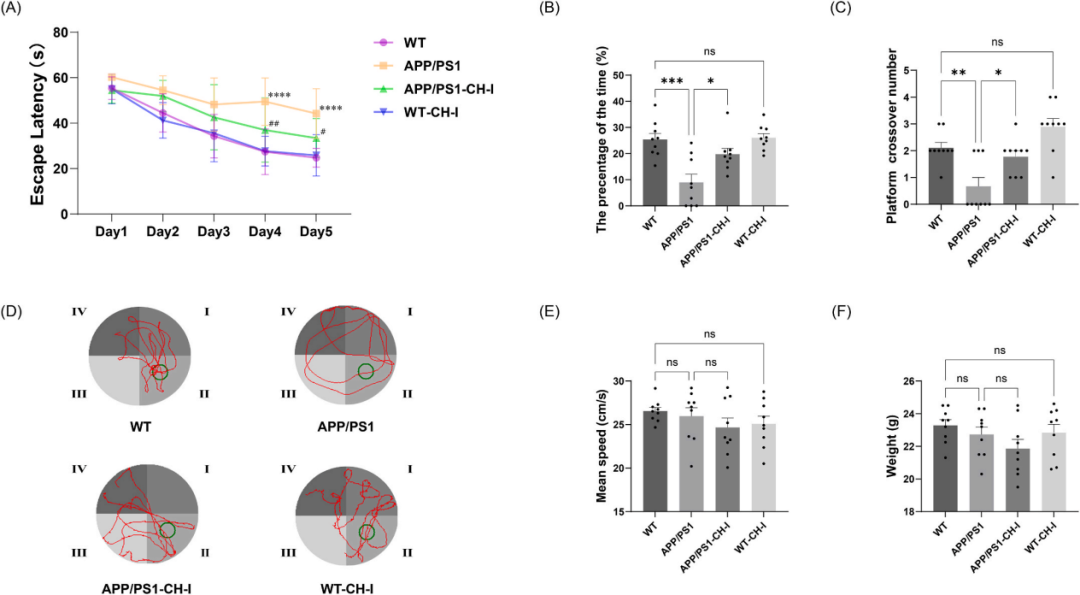
图一 CH-I改善了APP/PS1小鼠的认知障碍
在为期5天的Morris水迷宫(VisuTrack,上海欣软)隐蔽平台训练中,所有小鼠的学习能力随时间提升,而APP/PS1阿尔茨海默病小鼠找到平台所需时间(逃避潜伏期)明显长于野生型小鼠。脑蛋白水解物-I治疗显著缩短了APP/PS1小鼠在第4、5天的潜伏期,表明其学习能力得到改善。
第6天的探索实验(移除平台)显示:APP/PS1小鼠在目标象限停留时间更短、穿越原平台位置次数更少;经脑蛋白水解物-I治疗后,这些指标显著恢复,接近正常水平;而在野生型小鼠中,该药物未产生额外影响,说明其作用针对病理状态。
此外,各组小鼠的游泳速度和体重无差异,证明药物不影响基本运动能力,行为改善真实反映认知功能提升。
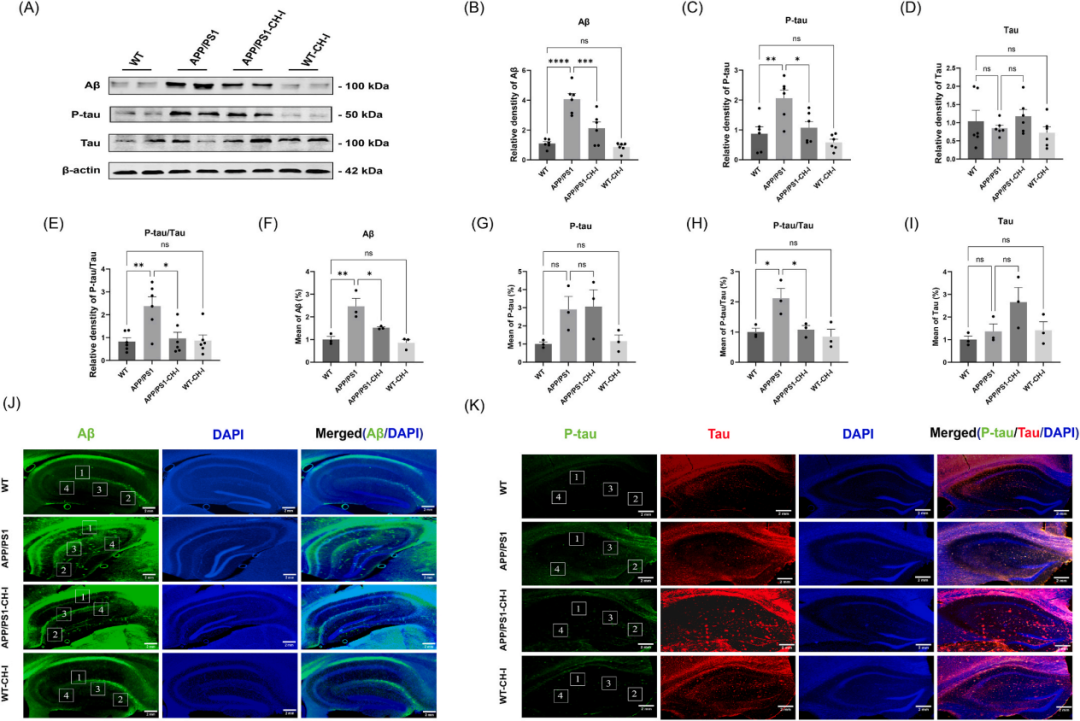
图二 CH-I减轻了APP/PS1小鼠海马组织中的β-淀粉样蛋白聚集和tau蛋白过度磷酸化
蛋白质印迹结果显示,APP/PS1组的β-淀粉样蛋白和磷酸化tau蛋白水平显著高于野生型组。CH-I显著降低了AD小鼠海马中β-淀粉样蛋白聚集和磷酸化tau的水平。
尽管tau蛋白水平无显著变化,但磷酸化tau与tau蛋白的比值存在显著差异。免疫荧光染色显示模型小鼠海马中存在β-淀粉样蛋白聚集和tau蛋白过度磷酸化。与AD小鼠相比,APP/PS1-脑蛋白水解物-I组的海马β-淀粉样蛋白阳性荧光强度显著降低。尽管各组间tau蛋白阳性和磷酸化tau蛋白阳性荧光强度水平无显著差异,但脑蛋白水解物-I治疗显著降低了APP/PS1组升高的磷酸化tau与tau蛋白比值。
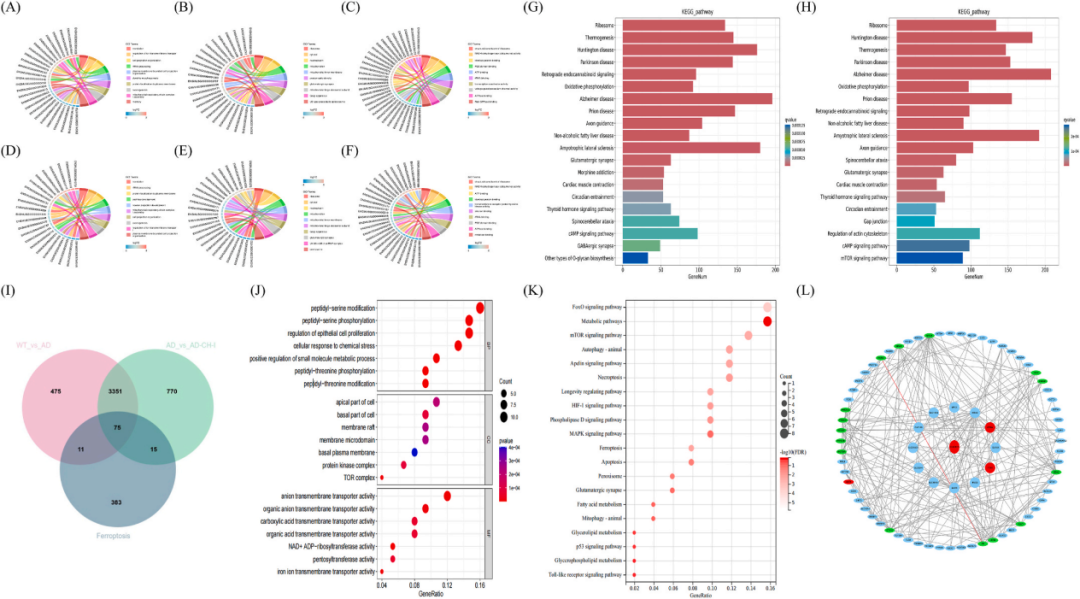
图三 功能富集分析与蛋白质-蛋白质相互作用网络
为系统阐明CH-I改善AD的分子机制,作者结合RNA测序与多组学富集分析。
GO分析显示,APP/PS1小鼠在记忆、谷氨酸能突触及金属离子跨膜转运等生物过程显著失调,而CH-I治疗可有效调控ATP酶结合、线粒体呼吸链复合物I组装及离子转运等功能。
KEGG通路分析进一步表明,AD模型中氧化应激、谷氨酸能突触异常等通路被激活,而CH-I显著调节了谷氨酸能突触、氧化磷酸化、cAMP及mTOR信号通路,这些均与铁死亡密切相关。通过将差异表达基因与铁死亡相关基因取交集,获得75个核心基因;对其再次富集发现,p53信号、mTOR复合物及铁离子跨膜转运活性显著改变。蛋白质互作网络分析进一步鉴定出SLC7A11和SAT1等关键铁死亡调控因子。
综合结果表明,CH-I通过抑制p53/SAT1/ALOX15轴并调控mTOR信号通路,有效阻断铁死亡进程,从而改善APP/PS1小鼠的认知功能障碍。
总结
脑蛋白水解物-I通过抑制p53/SAT1/ALOX15通路减轻铁死亡,从而改善AD小鼠的认知障碍和病理特征,为AD治疗提供新策略。
文章来源:
https://doi.org/10.1016/j.ejphar.2024.176820
欣软产品应用

原标题:《痴呆新解法!河北医科大学王珊团队揭示CH-I如何阻断阿尔茨海默病中的铁死亡》

