【科技前沿】骨骼肌兴奋-收缩偶联的“分子舞台”:原位结构揭示三联体中的精密协作
本篇报道来源于中国生物物理学会
冷冻电子显微学分会
正高级工程师李硕果团队
秦璐璐工程师助理投稿
当我们的身体完成一次奔跑、一次呼吸,甚至一次心跳,背后都离不开骨骼肌纤维中一场高度协调的分子事件——兴奋-收缩偶联(excitation-contraction coupling, ECC)。这一过程将电信号转化为机械收缩,其核心发生在被称为“三联体”的亚细胞结构中:横管(T管)与两侧的肌浆网(SR)终池紧密贴合,构成一个信号转导的“枢纽”。在这里,电压敏感的二氢吡啶受体(DHPR)感知兴奋信号,并通过与1型兰尼碱受体(RyR1)的偶联,触发肌浆网中钙离子的快速释放,最终引发肌肉收缩。
然而,这一关键过程的分子机制长期以来缺乏直观的结构证据。DHPR与RyR1之间是否存在直接的物理偶联?它们如何排列以确保信号快速、同步地传递?相邻RyR1之间又如何协同工作?中国科学院生物物理研究所孙飞团队利用冷冻电子断层扫描(cryo-ET)结合冷冻聚焦离子束(cryo-FIB)减薄技术的研究,首次在小鼠骨骼肌组织中,以近分子分辨率原位解析了三联体连接的超微结构,为这些悬而未决的问题提供了直接而精细的答案。
技术突破:从组织到薄片,在原位捕捉分子瞬间
传统结构生物学研究多依赖纯化后的蛋白样品,但这种方法会剥离蛋白的天然环境,丢失其与邻近分子的相互作用信息。为了在细胞原位观察RyR1与DHPR的真实状态,研究团队发展了一套适用于骨骼肌组织的cryo-FIB减薄流程。他们从小鼠趾长伸肌中分离出完整的肌纤维,经快速冷冻玻璃化后,利用cryo-FIB将样品减薄至约150纳米厚度,恰好适合cryo-ET成像。这一流程保留了三联体连接的完整超微结构,使得研究人员能够在断层图像中同时观察到T管、肌浆网膜、肌丝,乃至RyR1与DHPR的清晰密度。
在此基础上,通过子断层平均(STA)技术,团队分别获得了RyR1-FKBP12-钙调蛋白复合物(分辨率16.7 Å)以及RyR1-DHPR超级复合体(分辨率33 Å)的原位三维结构。这是首次在未纯化的骨骼肌组织中,直接观察到RyR1与DHPR之间的物理偶联。
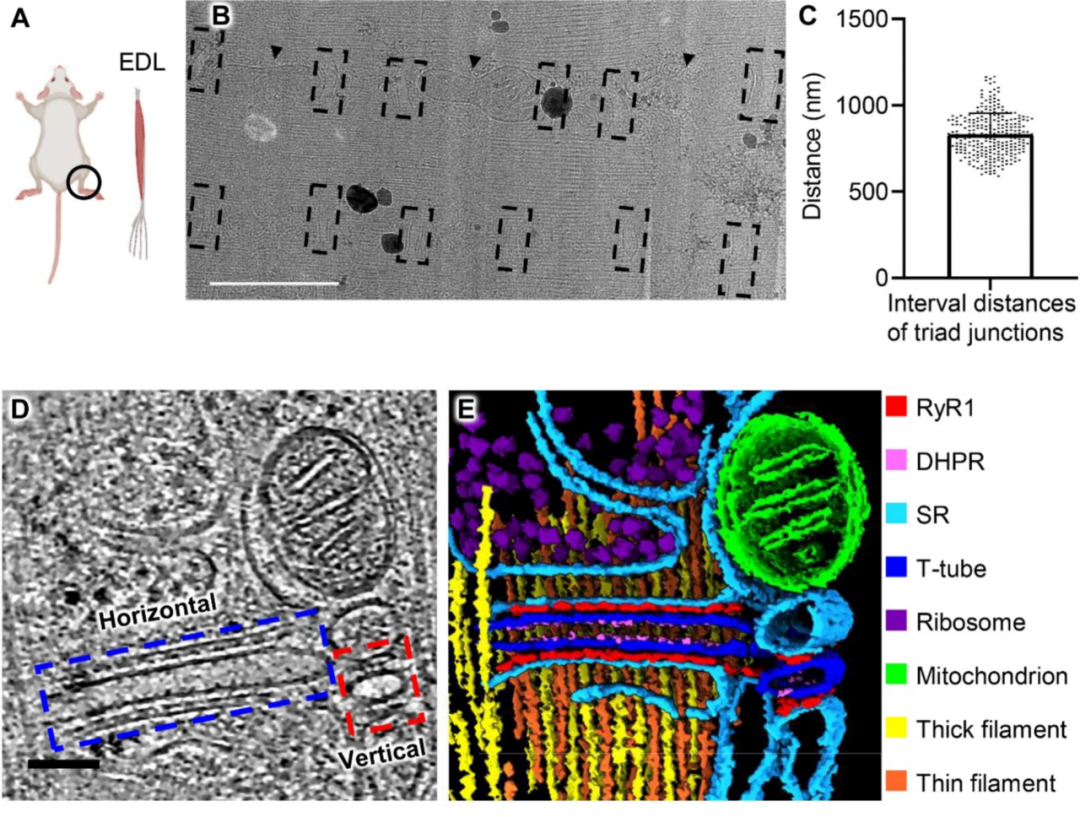
图1.小鼠骨骼肌中天然三联体连接的整体结构(A)从小鼠腿部手动提取的伸趾长肌纤维,黑色圆圈标示提取位置。(B)小鼠骨骼肌冷冻薄片的低倍冷冻电镜图像。规则排列的三联体连接由黑色虚线框标出,三联体连接附近的线粒体以黑色三角形标示。比例尺:1 μm。(C)三联体连接间隔距离的分布情况。(样本数277,均值833 nm,标准差122 nm。)(D)代表性断层切片显示两个垂直排列的三联体连接及其周围环境。比例尺:100 nm。水平与垂直方向的三联体连接分别由蓝色和红色虚线框标出。(E)分割后的断层图像展示(D)中三联体连接周围的不同组分。
核心发现之一:RyR1的“右手对角线”排列
在三联体的肌浆网膜上,RyR1并非随机分布,而是形成高度有序的阵列。研究发现,RyR1四聚体(即一个完整的RyR1通道)主要以两行平行排列的方式嵌入肌浆网膜,相邻的四聚体之间采用“右手角对角”的相互作用模式:从细胞质侧观察,一个四聚体的角总是与其右侧相邻四聚体的角接触。这种排列方式使得相邻RyR1之间的中心间距稳定在约31纳米。
通过分子动力学模拟,研究进一步揭示了这种排列的功能意义。模拟显示,处于开放状态的RyR1更容易自发形成这种角对角接触,并且这种接触会促进相邻RyR1之间的协同运动,尤其是在P2与螺旋结构域等关键区域。这意味着,当一个RyR1被激活后,其构象变化可以通过物理接触快速“扩散”到邻近的RyR1,从而实现钙释放的同步放大——这为过去在心肌细胞中观察到的“钙火花”现象提供了结构基础。
核心发现之二:DHPR与RyR1的1:2棋盘式偶联
更令人兴奋的是,研究在T管膜上首次原位识别出了DHPR的密度。这些密度以四个为一组,形成“四联体”,并以交替方式与RyR1结合:每两个RyR1四聚体中,只有一个会与一个DHPR四联体形成超级复合体,形成一种规则的棋盘状排列。这一发现直接证实了骨骼肌中DHPR与RyR1之间物理偶联的存在,而非仅依赖钙离子作为中介的化学偶联。
在RyR1-DHPR超级复合体的三维结构中,研究团队识别出两个连接密度——分别位于RyR1的P1与P2亚结构域附近,表明二者之间可能通过多个结合位点直接相互作用。这些位置与先前通过遗传学手段鉴定的关键功能区域高度吻合,例如对ECC至关重要的II-III环和STAC3、JP2等辅助蛋白的结合位点。这为理解DHPR如何将电压信号直接传递给RyR1提供了结构上的合理解释。
结构赋予功能:一个“精巧而高效”的信号网络
综合上述发现,研究团队提出了骨骼肌三联体的结构模型:T管与肌浆网膜之间形成约16纳米的间隙空间,T管膜上的DHPR四联体与肌浆网膜上的RyR1阵列通过“连接密度”直接耦合;而RyR1之间则通过“右手角对角”的物理接触实现协同门控。这种布局保证了即使在肌肉纤维长达数毫米的尺度上,兴奋信号也能在毫秒级时间内迅速传播,引发大量钙离子同步释放,从而驱动肌丝滑动,完成高效收缩。
值得注意的是,DHPR四联体并未与每一个RyR1结合,而是以1:2的比例交替出现。这可能是一种“经济型”设计:一个DHPR四联体激活后,其下方RyR1的开放可通过RyR1-RyR1相互作用“接力”传递至相邻未直接耦合的RyR1,既保证了信号放大,又减少了结构冗余。
结语:原位结构生物学照亮肌肉研究的新路径
这项研究不仅是骨骼肌ECC机制研究的重要里程碑,也展示了原位结构生物学在复杂组织样本中解析大分子机器真实状态的巨大潜力。通过cryo-FIB与cryo-ET的结合,我们得以在“天然环境”中直接观察蛋白与蛋白、蛋白与膜之间的精细互作,为理解生命活动的分子机制提供了前所未有的视角。
同时,这项研究也传递出一个重要启示:结构生物学的未来,不仅在于解析高分辨率的“孤立”结构,更在于将这些结构放回细胞这个复杂而有序的“舞台”上,去理解它们如何在动态网络中协同完成生理功能。骨骼肌三联体中的这场精密协作,正是这一理念的生动写照。
参考文献:
1.Jiashu Xu et al. ,In situ structural insights into the excitation-contraction coupling mechanism of skeletal muscle.Sci.Adv.10,eadl1126(2024).DOI:10.1126/sciadv.adl1126
相关推荐:
【科技前沿】Adv Sci | 电子科大宫玉彬团队提出离子靶向新机制:太赫兹波直接共振钙通道内离子,实现通透增强
【科技前沿】精准聚焦生命奥秘——冷冻原位光电关联成像技术

中国生物物理学会官方订阅号,
为BSC会员及生物物理领域专业人士服务。
投稿及授权请联系:bscoffice@bsc.org.cn。
原标题:《【科技前沿】骨骼肌兴奋-收缩偶联的“分子舞台”:原位结构揭示三联体中的精密协作》

