Immunity:急性和慢性感染如何引导记忆性CD4⁺ T细胞走向不同命运?

生命科学
在抗感染免疫中,CD4+ T细胞是协调免疫应答的核心枢纽。然而,在慢性感染及肿瘤等持续性抗原暴露情境下,T细胞功能会逐渐耗竭。目前对于CD8+ T细胞的耗竭机制已有较深入认识,但有关CD4+ T细胞在人类慢性感染中的分化与维持机制尚不清晰。
丙型肝炎病毒(HCV)感染为研究这一问题提供了理想的模型。HCV感染可导致两种截然不同的结局:自发清除或慢性感染,后者可通过直接抗病毒药物实现彻底治愈,为追踪不同感染结局下CD4+ T细胞的命运转变提供了独特条件。
近日,来自德国弗莱堡大学医学中心的科学团队在Cell Press细胞出版社旗下期刊Immunity上发表题为“Acute and chronic infections drive distinct trajectories in human memory CD4+ T cell formation”的重磅研究。文章利用MHC II类四聚体直接捕获急性、慢性、治愈及自发清除感染者体内的HCV特异性CD4+ T细胞,结合单细胞转录组测序、TCR追踪及多参数流式细胞术,系统揭示了不同感染背景下CD4+ T细胞的分化路径与记忆形成规律。
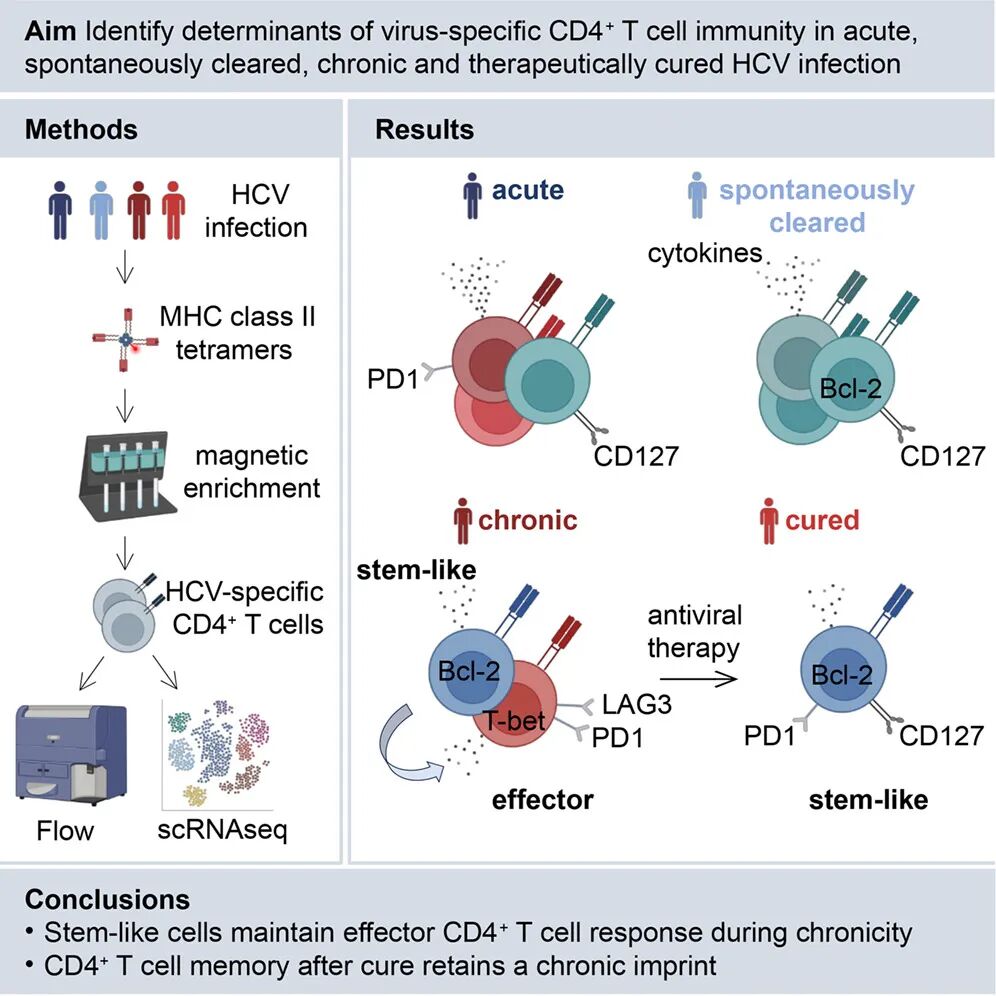
研究首先分析了不同感染阶段HCV特异性CD4+T细胞的检出率与频率。结果显示,急性感染与自发清除感染者中,该细胞的检出率高达90%,而在慢性感染患者中则显著降至48%。即便在可检出的人群中,慢性感染状态下病毒特异性CD4+T细胞的频率也远低于急性期。表型分析显示,多数病毒特异性CD4+T细胞表达CXCR3,提示其具有Th1分化倾向。其中部分细胞同时表达CXCR5,依据现行命名规则,共表达CXCR3与CXCR5的循环细胞被定义为cTfh1样细胞,而仅表达CXCR3者称为Th1样细胞。研究发现,自发清除感染者中cTfh1样细胞在病毒特异性CD4+T细胞中的占比显著升高,而在病毒血症期(急性和慢性)及治愈后患者中均未观察到同等程度的增加。
为了进一步评估不同感染状态下CD4+T细胞的辅助性T细胞极化特征,研究者开展了单细胞转录组分析。结果显示,尽管不同感染阶段获得的细胞在CXCR3与CXCR5蛋白表达水平上相近,但其转录组层面的辅助性T细胞极化特征却存在显著差异。具体而言,急性和慢性感染期病毒特异性CD4+T细胞以促炎性Th1与Th17特征为主,而自发清除后形成的记忆性CD4+T细胞则呈现出更为均衡的极化特征,与其具备分化为多种辅助性T细胞亚群的潜力相符。相比之下,慢性感染期及治愈后患者体内的病毒特异性CD4+T细胞表现出明显的滤泡辅助性T细胞(Tfh)偏倚,且这种偏倚在治愈后并未伴随Th1或Th17特征的增强。这一发现提示,仅凭传统的Tfh与Th1分类框架,难以充分描述慢性感染及治愈后CD4+T细胞的实际功能状态。
为了解析不同感染阶段病毒特异性CD4+T细胞的异质性,研究者对来自急性、慢性、治愈及自发清除感染者的单细胞转录组数据进行了无监督聚类分析,共鉴定出5个转录特征各异的细胞亚群。这些亚群在表观遗传重塑、细胞激活、效应分子调控及迁移相关基因的表达上存在显著差异。基于细胞激活状态相关基因集的富集分析显示,其中三个亚群处于相对静息状态,另两个亚群则呈现激活或效应特征。将不同感染阶段的细胞映射至各亚群后发现,来自病毒血症期(急性和慢性)的细胞主要富集于激活/效应亚群,而来自感染后清除状态(治愈或自发清除)的细胞则主要分布于静息亚群。进一步细分发现,慢性感染患者的细胞主要集中于一个特定的效应亚群,而急性感染患者的细胞则富集于另一个效应亚群,后者高表达ZEB2、TBX21、PRDM1及STAT1等与效应分化相关的转录因子。相比之下,治愈患者来源的细胞主要集中于一个静息亚群,自发清除患者的细胞则分布于另外两个静息亚群。流式细胞术的降维聚类分析在蛋白层面也证实了类似的分群模式:治愈或自发清除感染者体内以静息、高表达Bcl-2的细胞为主,而病毒血症期则以表达CD38、ICOS和T-bet的活化细胞为主。
针对慢性感染中病毒特异性CD4+T细胞的特性,研究进一步开展了亚群分析,鉴定出两个主要亚群。其中一个亚群高表达TCF7、SELL和CCR7等与干性和静息状态相关的基因,转录因子活性分析显示该亚群中TCF7和NFKB1的活性较高,提示其具有干细胞样特征。另一个亚群则高表达HLA-DRA、CD74等与活化和效应相关的基因,STAT1和PRDM1活性较高,代表效应性CD4+T细胞。流式细胞术的蛋白表达分析进一步以Bcl-2与T-bet的表达差异明确了干细胞样亚群与效应亚群的划分:前者高表达Bcl-2,后者高表达T-bet、Ki-67、CD38及ICOS。尽管两个亚群均表达TOX和PD-1,但效应亚群中这两个分子的表达水平更高。单细胞轨迹分析显示,慢性感染中干细胞样亚群与效应亚群之间存在明确的前体-子代关系,且同一患者体内两个亚群共享相同的T细胞受体克隆型,进一步证实了二者的谱系关联。将慢性与急性感染中病毒特异性CD4+T细胞的转录组数据联合分析后发现,干细胞样亚群在急性和慢性感染中均有存在,提示这类细胞在急性期即已预形成;而效应亚群在急性和慢性感染中则呈现不同的基因表达特征,反映了不同感染背景下效应分化的差异。
研究进一步评估了慢性感染治愈后病毒特异性CD4+T细胞的长期维持能力。通过对治愈患者长达3至8年的纵向随访发现,病毒清除后效应亚群迅速消失,而干细胞样亚群则持续存在,表型稳定,仍表达TOX、PD-1等分子。单细胞转录组数据显示,治愈后病毒特异性CD4+T细胞的转录谱与慢性感染期的干细胞样亚群高度重叠,两者间差异表达基因极少,而与慢性感染期的效应亚群则存在大量差异表达基因。同时,同一患者治愈前后检测到的干细胞样细胞共享相同的T细胞受体克隆型,表明这些细胞并未随病毒清除而消失,而是得以长期存续。功能层面,治愈后HCV特异性CD4+T细胞仍可在非特异性刺激下产生IFN-γ、TNF、IL-2及IL-21等多种细胞因子。
尤为关键的是,研究报道了一例独特的临床案例。该患者在首次抗病毒治疗后出现病毒复发,随后再次接受治疗并最终获得持续病毒学应答。动态监测显示,慢性感染期存在的活化与增殖特征在首次治疗后消失,仅干细胞样细胞持续存在;当病毒复发、抗原再度出现时,这些干细胞样细胞迅速被重新激活,重新获得CD38和Ki-67的表达,并分化为T-bet阳性效应细胞;而再次清除病毒后,细胞又恢复为静息的干细胞样状态。这一动态过程有力证明了干细胞样CD4+T细胞具备功能性记忆潜能,能够在抗原再次暴露时启动有效的回忆反应。
最后,研究系统比较了慢性感染治愈后形成的记忆性CD4+T细胞与自发清除后形成的经典记忆性CD4+T细胞之间的差异。转录组多维尺度分析显示,治愈后细胞的转录谱与慢性感染期细胞高度相似,而与急性期及自发清除后细胞则明显不同。功能层面,自发清除后细胞的多功能性更强,产生三种及以上细胞因子的细胞比例显著高于治愈后细胞。治愈后细胞富集了与LAG3介导的功能受损、T细胞耗竭及“无伴侣”NFAT通路相关的基因特征,而自发清除后细胞则富集了与干性及缺乏抑制信号相关的基因。蛋白水平上,治愈后细胞PD-1表达更高,CD45RA、CD127、CCR7、CD38及ICOS的表达则低于自发清除后细胞。
尽管两类细胞均位于干细胞样亚群且均高表达TOX,但转录因子调控网络分析显示,TOX在两类细胞中调控的下游基因网络存在显著差异。治愈后细胞中TOX与TCF7、ETS1、NFKBIA等基因关联,而自发清除后细胞中TOX则与FOXN2、FOXP1、STAT4等基因关联,说明即便TOX蛋白表达水平相似,其在不同背景下发挥的转录调控功能也发生了重编程。此外,RUNX3、STAT4、BATF、ZEB1、ID3、FOXO3、LEF1及MYC等转录因子在两类细胞中亦呈现不同活性,进一步凸显治愈后形成的记忆细胞保留了慢性感染期间的分子印迹。
综上所述,本研究通过对不同感染结局下HCV特异性CD4+T细胞的系统解析,揭示了CD4+T细胞在急慢性感染中的分化轨迹与记忆形成机制。研究发现,慢性感染中的病毒特异性CD4+T细胞并非均一的耗竭群体,而是由干细胞样亚群与效应亚群共同构成,两者之间存在明确的前体-子代关系。干细胞样CD4+T细胞在急性期即已形成,并在慢性感染中持续存在,即使在病毒清除后仍能长期维持,形成稳定的记忆细胞池。然而,这种在慢性感染背景下形成的记忆细胞,与自发清除后形成的经典记忆细胞在转录组、功能及转录因子调控网络上均存在显著差异,保留了“慢性印迹”。上述发现深化了对人类CD4+T细胞在慢性病毒感染中分化与维持机制的认识,也为未来通过靶向干细胞样CD4+T细胞优化慢性感染及肿瘤免疫治疗策略提供了新的理论依据。

相关论文信息
论文原文刊载于Cell Press细胞出版社
旗下期刊Immunity
▌论文标题:
Acute and chronic infections drive distinct trajectories in human memory CD4+T cell formation
▌论文网址:
https://www.sciencedirect.com/science/article/pii/S1074761326001196
▌DOI:
https://doi.org/10.1016/j.immuni.2026.03.008
原标题:《Immunity:急性和慢性感染如何引导记忆性CD4⁺ T细胞走向不同命运? | Cell Press论文速递》

