浙大最新:短期禁食让肿瘤细胞“拱手相让”营养,激活T细胞抗癌,提升免疫治疗效果
这几年,要说哪种「养生大法」最容易在打工人、减肥党和熬夜人之间形成「跨圈层共识」,「16+8轻断食」绝对算得上头部选手。
它的实操方法也确实很「讨喜」:不用餐餐盯着热量表,只需要把吃饭这件事压缩进8小时内,剩下连续16小时保持空腹(可以喝水)。听起来,既不像节食那么痛苦,也比「顿顿水煮菜」更容易坚持。
事实上,这套看似很「新」的养生法,骨子里一点也不新。
无论是古代医学里「少食以养」的朴素经验,还是许多修行传统中「节食、控食」的做法,本质上都在传递一个相似的信号——吃少一点、空一会儿,未必是亏待自己,反而可能是在给身体一次喘息和重整秩序的机会。
16小时轻断食+免疫治疗,
抗癌效果被进一步「放大」
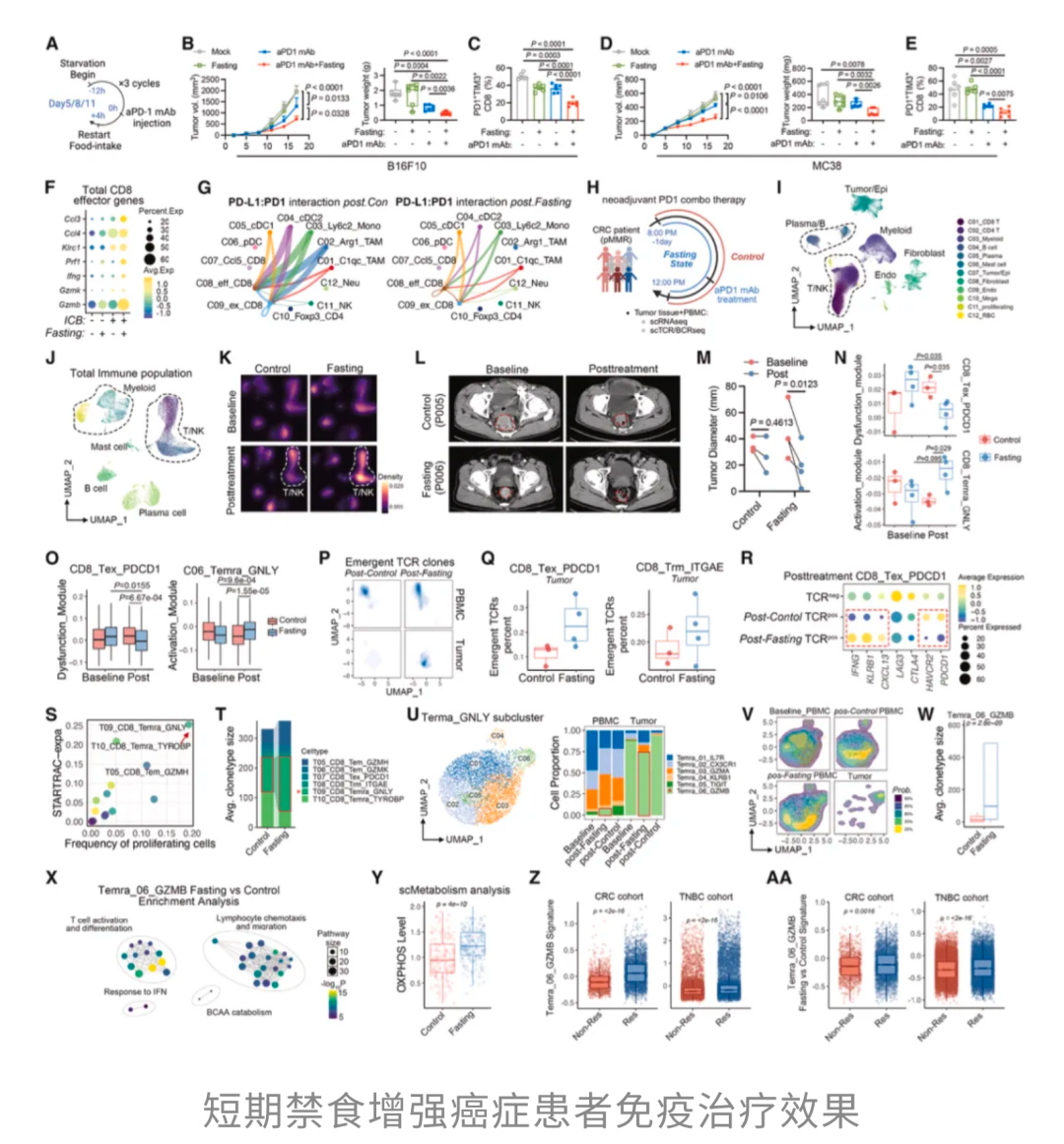
近期,来自浙江大学的研究团队发表于Cell子刊Cell Metabolism的一项研究[1]发现,「空一会儿肚子」可能不只是让脂肪更难囤、让裤腰更松一点,它甚至有可能在关键时刻,帮免疫细胞抢回「战场」。短短16小时的禁食,足以诱导异亮氨酸这种必需氨基酸在肿瘤局部积累,进而给CD8⁺T细胞加满「战斗值」,增强它们杀伤癌细胞的能力,并显著放大癌症免疫治疗的效果。

他们发现,经过这段短期禁食后,肿瘤中的CD8⁺T细胞像是被重新「充了电」,抗肿瘤战斗力明显提升,原本那种疲惫、「打不动」的耗竭倾向减轻了,连γ干扰素(IFN-γ)和颗粒酶B(GZMB)这两类专门用来「清剿」癌细胞的效应分子,也都明显增加。
换句话说,禁食让肿瘤中的免疫细胞重新找回了状态,从「有点蔫」变成了「真能打」。

结果观察到,短期禁食同样能够在人类结直肠癌患者体内重塑肿瘤免疫微环境。CD8⁺T细胞同样更倾向于走向细胞毒性更强、耗竭程度更低的状态。
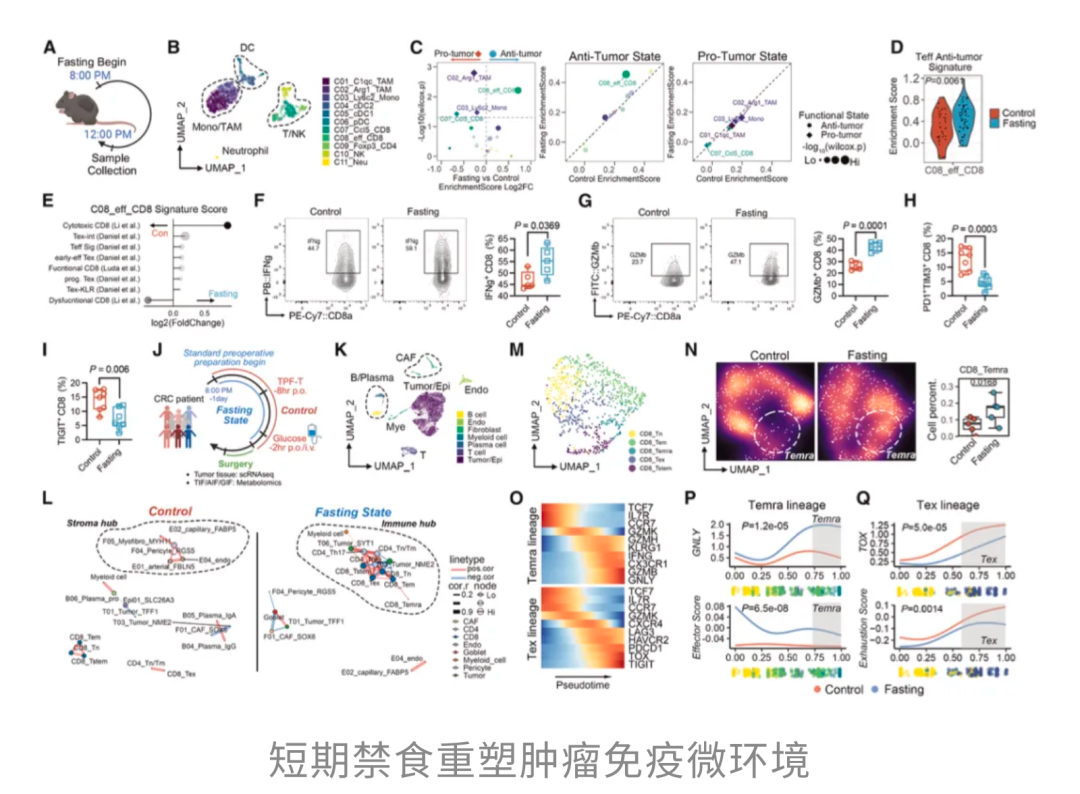
那短期禁食,究竟是怎么把肿瘤里的免疫细胞重新「调动起来」的?
研究团队顺着代谢这条线往下挖,他们发现,大约16小时的短期禁食,足以特异性地重塑肿瘤微环境中的代谢状态,让异亮氨酸(Ile)在肿瘤内部明显富集,这正是肿瘤内CD8⁺T细胞重新恢复战斗力的重要基础。
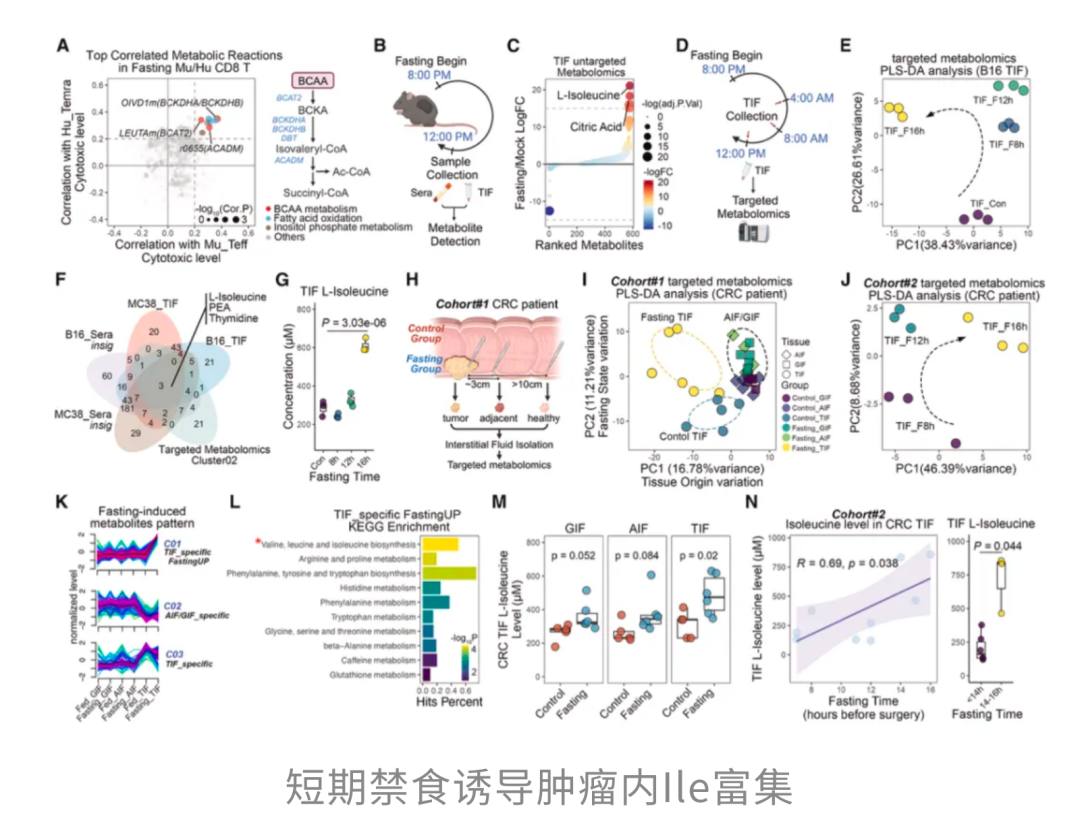
Ile是人体必需的九种氨基酸之一,属于支链氨基酸家族。在模拟肿瘤内部「捉襟见肘」的营养环境时,研究者进行了一个很直观的对比:一旦在培养基中补充Ile,原本状态低迷的CD8⁺T细胞,不仅增殖能力恢复了,连杀伤功能也明显增强;而把Ile撤走后,这些细胞很快又变得「提不起劲」,活性和功能双双下滑。
这也意味着,CD8⁺T细胞想要「打」得动肿瘤,前提之一,就是获取并利用lle。
Ile被CD8⁺T细胞「吃进去」之后,是怎么把免疫细胞重新「带飞」的呢?
原来,Ile进入T细胞后,会被一步步送入线粒体,经过一连串代谢反应,最终转化为乙酰辅酶A。一方面,乙酰辅酶A能参与线粒体的氧化磷酸化,为T细胞提供充足能量。
另一方面,CD8⁺T细胞想要真正进入高效杀伤状态,还得把一批关键的效应基因彻底「打开」。这一步,离不开一种重要的表观遗传调控——组蛋白乙酰化。直白来说,就是要在某些关键基因所在的位置贴上「现在可以高效表达」的标签。Ile代谢产生的乙酰辅酶A,正是制造这些「激活标记」的原材料。
不仅如此,乙酰辅酶A还是合成磷脂等膜脂的重要原料。对于CD8⁺T细胞来说,它们要想精准贴近肿瘤细胞、形成稳定接触,并顺利释放杀伤性效应分子,细胞膜结构必须足够完整、灵活。少了这层「硬件支持」,再强的杀伤程序也很难真正落地。
因此,lle通过提供乙酰辅酶A,同时为CD8+T细胞提供了能量、表观遗传重塑的指令,以及物质合成的原料,把CD8⁺T细胞从「有心无力」推到「火力全开」的状态,三位一体地撑起它们强大的抗肿瘤能力。
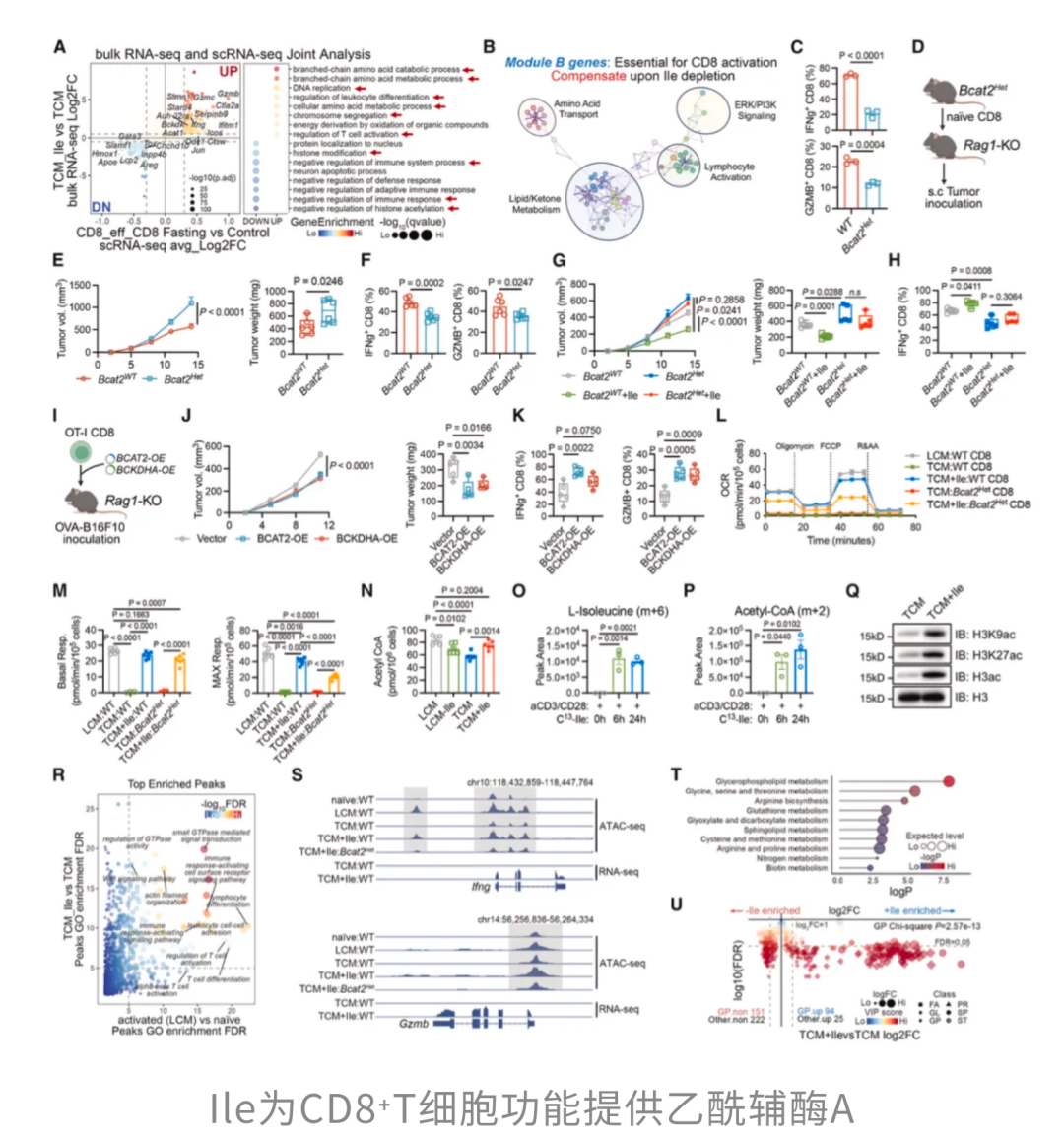
既然短期禁食后,肿瘤中的Ile水平明显升高,而且偏偏又对CD8⁺T细胞大有好处,那这些Ile,究竟是从哪里「冒出来」的?
研究者进一步进行了代谢通量分析,发现:禁食之后,肿瘤细胞自身对支链氨基酸(包括Ile)的分解利用反而下降了。换句话说,肿瘤细胞自己先不怎么「吃」了,于是Ile才在局部环境中慢慢积了起来。
但这并不意味着肿瘤细胞就此「认命挨饿」。恰恰相反,在断食带来的营养压力下,它们很快切换到了另一套「求生模式」:少碰Ile,多抓谷氨酰胺。对肿瘤细胞来说,谷氨酰胺更能帮它们「保命」,帮助它们维持线粒体代谢和基本生存。
为了高效拿到这份「救命口粮」,肿瘤细胞启动了一场精打细算的氨基酸交换。它们通过细胞膜上的特定转运蛋白,把手里的某些氨基酸「拿出去换」,以换回自己更急需的谷氨酰胺。在这个过程中,Ile就成了那个被拿来「交易」的筹码,被不断释放到肿瘤微环境中。
简而言之,16小时左右的短期禁食,迫使肿瘤细胞为了获取生存必需的谷氨酰胺,不得不进行一种「代谢交易」,将宝贵的lle「拱手相让」给周围的CD8+T细胞。肿瘤细胞原本是想“自救”,结果却在无意中给免疫细胞递了「燃料」。
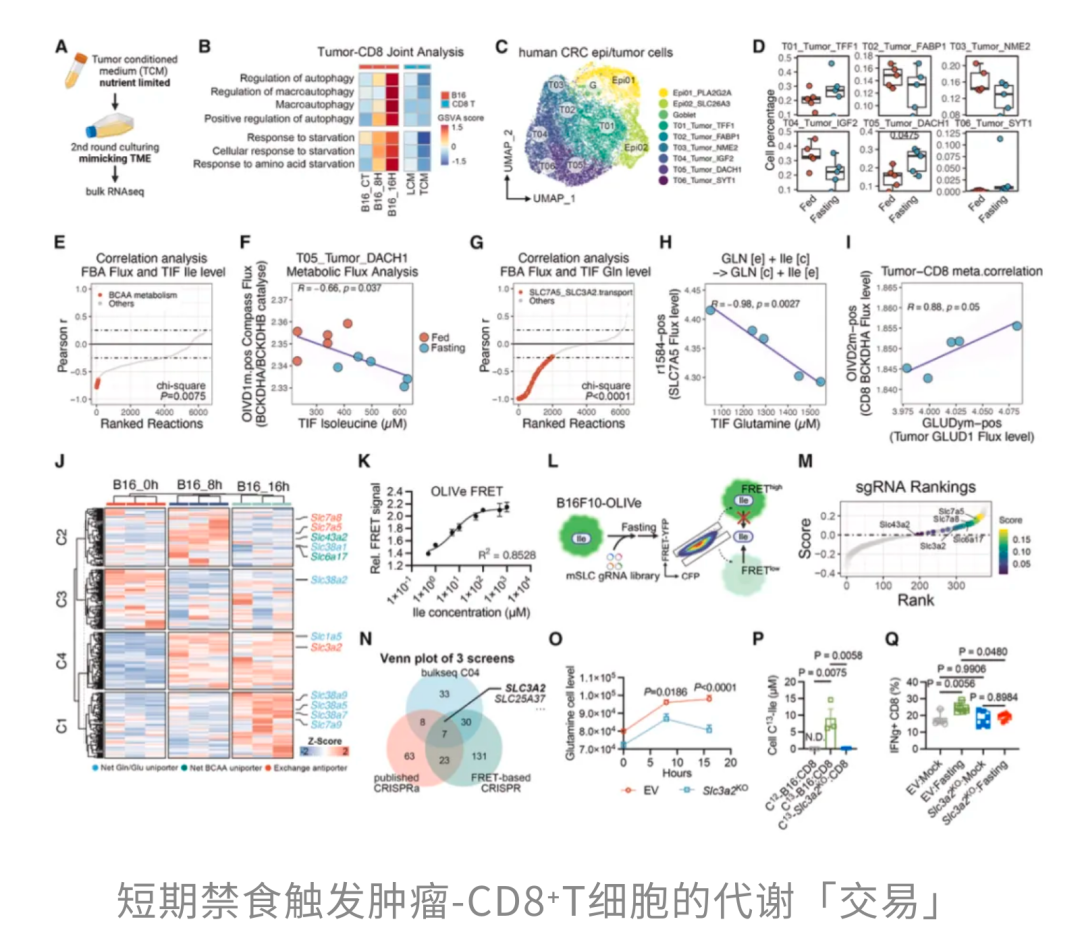
基于上述发现,研究团队验证了这套「16小时轻断食+免疫治疗」的组合方案的治疗潜力。

换言之,短期禁食可以重塑代谢环境,增强T细胞功能,并进一步放大免疫治疗的效果。
16+8轻断食,怎么一会儿「封神」,
一会儿「翻车」?
不过,这些年一直稳坐饮食圈的「顶流」位置的16+8轻断食,支持者不少,争议声也同样不小。
比如,此前一项由上海交通大学医学院联合哈佛大学开展的研究[2],就让不少「轻断食人」当场破防。研究结果显示,与每天进食时间集中在12-14小时的人相比,每天进食窗口少于8小时的人,心血管死亡风险反而高出了135%。
看到这里,很多人开始嘀咕:“同样是16+8轻断食,怎么有时候被捧上「神坛」,有时候又被认为「翻车」?”
正因为结论时常「打架」,我们才有必要把近年来关于16+8轻断食正负两方面的研究放在一起,重新捋一捋。
近年16+8轻断食正负两方面的研究汇总

不难发现,16+8轻断食的「高光时刻」,大多集中在机制和代谢层面;而它「翻车」的地方,往往在于执行方式出了偏差——比如把它当成了「乱挨饿」,或者不管自己适不适合,都一股脑儿往身上套。
事实上,16+8是一种帮助饮食自律的时间框架。但如果有人一边16+8,一边在8小时进食窗口里奶茶照喝、炸鸡照炫,把原本的宵夜改成「下午茶暴食」,那最后多半只是把「乱吃」从晚上平移到了白天。
说到底,科学的16+8,尽量得让吃饭时间顺着身体的生物钟走。相比于把主餐拖到深夜,更推荐把进食窗口安排在白天和傍晚,比如9:00–17:00、10:00–18:00或11:00–19:00。
而且,对大多数普通成年人来说,比起一上来就死磕16+8,更适合先从12+12或14+10过渡。进入8小时进食窗口后,也别把它当成「饿了半天终于放飞自我」的补偿时段,而是尽量把饭吃得更规整、更有质量:蛋白质、蔬菜、水果和优质碳水该有的都得有。
当然,16+8也不是人人都适合。它更适合那些平时夜宵多、饮食节律混乱、总热量容易失控,或者本身就有控体重、改善代谢需求的成年人。可如果是孕哺期女性、青少年、体重偏低或营养不足者、容易低血糖,以及胃肠功能较差的人,不太适合盲目跟风~
注:研究[1]临床队列样本量偏小,需大样本随机对照试验验证;且未拓展至更多癌种,普适性待验证。
参考资料:
[1]Chen S, Hu T, Zhu K, Liu Y, Yang Y, Li X, et al. 16-h fasting optimizes cancer immunotherapy in mice and humans. Cell Metab. 2026;38:1–19. https://doi.org/10.1016/j.cmet.2026.01.015.
[2]Chen M, Xu L, Van Horn L, Manson JE, Tucker KL, Du X, Feng N, Rong S, Zhong VW. Association of eating duration less than 8h with all-cause, cardiovascular, and cancer mortality. Diabetes Metab Syndr. 2025 Aug 21:103278. doi: 10.1016/j.dsx.2025.103278. Epub ahead of print. PMID: 40849219.
[3]Lowe DA,Wu N, Rohdin-Bibby L, et al. Effects of Time-Restricted Eating on Weight Loss and Other Metabolic Parameters in Women and Men With Overweight and Obesity: The TREAT Randomized Clinical Trial. JAMA Intern Med. 2020;180(11):1491–1499. doi:10.1001/jamainternmed.2020.4153
[4]Liu D, Huang Y, Huang C, et al. Calorie restriction with or without time-restricted eating in weight loss. N Engl J Med. 2022;386(16):1495-1504. doi:10.1056/NEJMoa2114833.
[5]Yang, Y., &Liu, D. (2024). Impacts of time-restricted feeding on middle-aged and old mice with obesity. The Journal of Physiology, 602(22), 6109–6123. https://doi.org/10.1113/JP285462.
[6]Oparija-Rogenmozere, L., Di Natale, M. R., Hunne, B., Koo, A., Ringuet, M., Fazio Coles, T. E., Fothergill, L. J., McQuade, R., &Furness, J. B. (2025). Time-restricted feeding leads to sex- and organ-specific responses in the murine digestive system. PLOS ONE, 20(9), e0332295. https://doi.org/10.1371/journal.pone.0332295
[7]Ye, Y., Xu, H., Xie, Z., Wang, L., Sun, Y., Yang, H., Hu, D., &Mao, Y. (2020). Time-restricted feeding reduces the detrimental effects of a high-fat diet, possibly by modulating the circadian rhythm of hepatic lipid metabolism and gut microbiota. Frontiers in Nutrition, 7, 596285. https://doi.org/10.3389/fnut.2020.596285
[8]Isenmann, E., Dissemond, J., &Geisler, S. (2021). The effects of a macronutrient-based diet and time-restricted feeding (16:8) on body composition in physically active individuals-A 14-week randomised controlled trial. Nutrients, 13(9), 3122. https://doi.org/10.3390/nu13093122
[9]Azemi, A. K., Siti-Sarah, A. R., Mokhtar, S. S., &Rasool, A. H. G. (2022). Time-restricted feeding improved vascular endothelial function in a high-fat diet-induced obesity rat model. Veterinary Sciences, 9(5), 217. https://doi.org/10.3390/vetsci9050217
[10]Mengi Çelik, Ö., Köksal, E., &Aktürk, M. (2023). Time-restricted eating (16/8) and energy-restricted diet: effects on diet quality, body composition and biochemical parameters in healthy overweight females. BMC Nutrition, 9(1), 97. https://doi.org/10.1186/s40795-023-00753-6
[11]Arruda A C, Santos R B, Freitas-Lima L C, et al. 16/8 intermittent fasting in mice protects from diet-induced obesity by increasing leptin sensitivity and postprandial thermogenesis[J].Acta Physiologica, 2025, 241(5): e70036. DOI: 10.1111/apha.70036.
[12]Yuan X Y, Zhao W B, Wang Y C, et al. Time-restricted feeding ameliorates hepatic lipid and glucose metabolism dysregulation induced by PM2.5 exposure in mice[J]. Ecotoxicology and Environmental Safety, 2026, 309: 119719. DOI: 10.1016/j.ecoenv.2026.119719.撰文 | 木白
编辑 | 木白

