成分都是布地奈德,耐赋康为何被批准用于IgA肾病,其他剂型不行?
许多IgA肾病患者都知道布地奈德肠溶胶囊(原研)是首个获批的对因治疗药物。
但一个常见的疑问是:布地奈德早就有了,成分同样是“布地奈德”,耐赋康为何能精准治疗肾脏疾病,而其他剂型却不行?
答案的关键,在于其根据IgA肾病发病机制创新发明的药物递送系统,这就像为药物配备了“体内GPS”,它可以突破胃酸、避开小肠上段误投,药物精准直达IgA肾病病灶源头——回肠末端的派尔集合淋巴结崩解并释放。
那么,这套“导航”系统如何工作?其精准性、有效性又如何被科学验证?下文将为您揭秘。
怎么做到靶向溶解、直击目标部位?
口服药物吃下去之后,要依次经过食道、胃、空肠、回肠、结肠等消化器官。要想让药物在目标——回肠末端发挥作用,得保证它不会在胃和空肠就被溶解和吸收,还要保证它能够在回肠溶解、起效。
如何做到呢?
我们的胃肠道中不同的部位酸碱度(pH值)有所不同,胃里最酸(pH最小,约为1.7),随后酸度降低,空肠至回肠末端的pH从6.5逐渐上升至8.01[2]。
基于此,特定pH值下溶解的胶囊外层包衣,可以帮助药物到达目标部位。研发人员通过调整溶解pH不同的两种材料(比如一个溶解pH为6,一个为7)的配比,把控最终的溶解pH。
在TARGIT™技术的帮助下,布地奈德肠溶胶囊的胶囊壳能够在回肠末端特定的pH值环境下溶解,释放出活性成分,也就是含布地奈德的缓释微丸,作用于目标部位——派尔集合淋巴结。另外,这个缓释微丸有3层包衣结构,能够有效延长药物的作用时间。
道理我们已经懂了,那么这个胶囊真的能精准地在目标部位溶解吗?这就需要精确的科学实验帮助我们来了解。
溶出度试验:测定药物溶解释放情况的关键方法
溶出度试验是一种在体外模拟药物在胃肠道中释放与溶解过程的研究方法。该试验通过配制不同成分与PH值的模拟胃肠液,将药物置于其中,并在恒温(约37℃)和持续搅拌的条件下,模拟人体消化道的温度与蠕动环境。
试验时长的设定通常参照药物在人体消化道各部位的生理停留时间(如空腹状态下,药物在胃内约停留1小时,经小肠前段约需2个多小时),以使试验条件更贴近真实情况。
试验过程中,研究人员会定时测定药物溶出的量,计算溶出百分比,并绘制成“溶出曲线”。该曲线直观展示药物随时间的释放情况,就能分析单种药物的溶出特性,也可用于比较不同药物之间的释放差异。
布地奈德肠溶胶囊的溶出情况
根据上述溶出度试验原理,有研究[4]对比了不同布地奈德制剂的溶出情况,这些药物分别可以在特定pH溶解,也就是能够在胃肠道的不同部位释放,用于治疗IgA肾病(Nefecon)、溃疡性结肠炎(Cortiment)、克罗恩肠病(Entocort、Budenofalk)等疾病。
胃液模拟:首先,研究者在胃液(pH1.2)模拟环境下观察了药物的溶出情况,发现包括布地奈德肠溶胶囊在内的布地奈德制剂,都没有药物溶解出来,符合“不在胃内就释放”。
肠液模拟:接下来,研究人员模拟了肠液(pH6.5、6.8),观察了药物在3个小时内(模拟药物通过真实小肠的时间)的溶解情况。
结果显示,布地奈德肠溶胶囊(Nefecon)在模拟的肠液中的第一个小时内,几乎不释放药物,随后呈现适度、缓慢的释放模式,大部分的药物释放发生在第二个小时,3个小时基本完成释放。
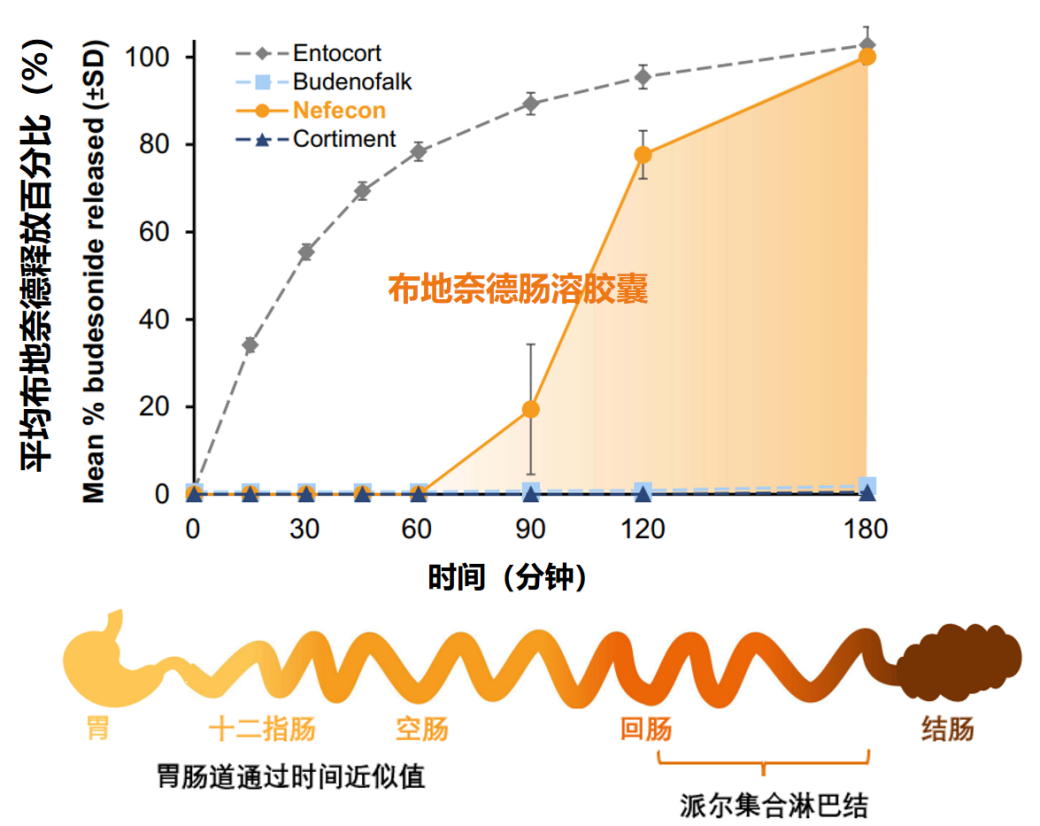
不同布地奈德制剂的溶出曲线(橙色曲线为布地奈德肠溶胶囊)
结合真实的小肠转运时间来看,也就是大约在空肠中药物开始缓慢的释放,到了富集派尔集合淋巴结的回肠后,药物释放加快,通过小肠的时候药物已经释放完毕。也就是说,布地奈德肠溶胶囊(Nefecon)确实能够将活性成分送到靶向目的地派尔集合淋巴结,从而在此抑制B淋巴细胞,减少Gd-IgA1的产生[3]。
另外也可以看到,不同的布地奈德制剂的溶出曲线差别很大,有的一进入小肠就快速溶解释放(上图中灰色的曲线),有的在整个小肠中都没反应(上图中浅蓝、深蓝色的曲线),而布地奈德肠溶胶囊(Nefecon,橙色曲线)呈现出独特的延迟、缓慢释放模式。这清楚地表明,不同布地奈德制剂在体内的行为差异很大,因此不能相互替代。
布地奈德肠溶胶囊(原研)的设计初衷正是最大化局部作用、最小化全身暴露,它的疗效源于药物在派尔集合淋巴结处的局部浓度(并非血液循环中的药物浓度)。通过TARGIT™技术,布地奈德肠溶胶囊实现了从“广泛免疫抑制”到“肠道源头靶向”的突破,溶出度试验就是这一过程的科学证据,以此达成治疗IgA肾病的理论基础。不过在更为复杂的人体环境下,就需要广泛的临床疗效数据来判断了。
长期临床研究进一步佐证
布地奈德肠溶胶囊(原研)的疗效是基于其独特的溶出曲线实现的,并经过了大型III期临床试验(NefIgArd)验证。该研究纳入364个IgA肾病患者,结果显示应用布地奈德肠溶胶囊(原研)治疗9个月,不仅带来了持久的蛋白尿下降,减少镜下血尿风险,更重要的是患者估算肾小球滤过率(eGFR)的下降也有了明显的延缓,肾功能衰退减少了50%[5]。
随着布地奈德肠溶胶囊(原研)在临床中的广泛应用,其在真实医疗环境里的疗效与安全性数据不断累积,在各类患者(比如严重肾功能不全、IgA肾病早期等特殊人群)中均表现出稳定疗效,且整体耐受良好,没有出现严重安全问题。此外,使用超过9个月的患者数据显示,长期治疗的效果明确且安全性良好。
这些临床数据都是布地奈德肠溶胶囊(原研)能够有效治疗IgA肾病的坚实基础,而不仅仅是血药浓度、溶出度试验等单纯环境的结果。
总结
布地奈德肠溶胶囊通过其TARGIT™递送技术,能够将药物精准递送至回肠末端的派尔集合淋巴结,从而在源头干预IgA肾病。溶出试验证实了它能在目标部位精准释放,同时也提醒我们:虽然主要成分都是“布地奈德”,但不同制剂释放方式不同,也是能否用于治疗IgA肾病的关键区别。在此基础上,布地奈德肠溶胶囊(原研)的临床证据充足可靠,这也是对广大IgA肾病患者负责的态度。
参考文献:
[1]陈沁兰, 吕继成. 布地奈德肠溶胶囊在IgA肾病中的免疫调节作用和研究进展[J]. 中华内科杂志, 2025, 64(7): 688-692.
[2]Avdeef A. Physicochemical profiling (solubility, permeability and charge state). Curr Top Med Chem. 2001 Sep;1(4):277-351.
[3]Barratt J, Kristensen J, Pedersen C, et al. Insights on Nefecon®, a Targeted-Release Formulation of Budesonide and Its Selective Immunomodulatory Effects in Patients with IgA Nephropathy. Drug Des Devel Ther. 2024 Jul 31;18:3415-3428.
[4]Jennifer Dressman. Comparative Dissolution of Budesonide from Four Commercially Available Products for Oral Administration: Implications for Interchangeablity. Dissolution Technologies, 2023, dx.doi.org/10.14227/DT300423P224.
[5]Lafayette R, Kristensen J, Stone A, et al. Efficacy and safety of a targeted-release formulation of budesonide in patients with primary IgA nephropathy (NefIgArd): 2-year results from a randomised phase 3 trial. Lancet. 2023 Sep 9;402(10405):859-870.
原标题:《成分都是布地奈德,耐赋康为何被批准用于IgA肾病,其他剂型不行?释放方式区别较大》

