【科技前沿】精准聚焦生命奥秘——冷冻原位光电关联成像技术
本篇报道来源于中国生物物理学会冷冻电子显微学分会青年委员李硕果研究员投稿,张小云为共同第一作者。
细胞内部结构的三维可视化是理解生命活动的关键。冷冻电子显微镜(cryo-EM)技术,尤其是单颗粒分析,已在体外实现生物大分子的高分辨率结构解析。然而,细胞内分子机器是在复杂、动态的环境中发挥功能的,这就需要在原位——即细胞内部——研究它们。冷冻电子断层扫描(cryo-ET)正是这样一种强有力的技术,它能够对冷冻保存的细胞进行三维成像,揭示大分子复合物在近天然状态下的结构与组织方式。
但cryo-ET的应用面临一个根本性挑战:电子束的穿透能力有限。在300 kV加速电压下,可观测的样品厚度通常不超过200 nm。绝大多数真核细胞厚度远超此值,因此必须制备出足够薄的“冷冻含水切片”。目前,冷冻聚焦离子束(cryo-FIB)减薄技术被认为是制备高质量、表面平整的冷冻含水切片的标准方法。
然而,如何让cryo-FIB精准地“切到”细胞内稀有的、特定的目标结构(如中心体、病毒工厂等),而非随机减薄,一直是该领域的技术瓶颈。传统的工作流程往往依赖独立的冷冻荧光显微镜(cryo-FM)先进行荧光成像,再将样品转移至冷冻扫描电镜(cryo-SEM)中进行FIB减薄,通过复杂的图像关联对齐来导航减薄位置。这种方式不仅操作繁琐、易引入冰污染,而且受限于光学显微镜的分辨率,关联精度往往不足以定位微小或稀少的目标结构。
正是在这一背景下,中国科学院生物物理研究所蛋白质科学研究平台生物成像中心团队自主研发的两项原创性技术——HOPE-SIM与ELI-TriScope分别从“高精度三维关联”和“原位实时监控”两个角度,提出了解决方案。
HOPE-SIM:冷冻三维超分辨,精准关联
HOPE-SIM系统是在技术团队2017年开发的高真空光学冷台(HOPE)基础上,将宽场荧光显微镜升级为三维结构光照明显微镜(3D-SIM),并配套开发了专用三维关联软件3D-View。
结构光照明显微镜(SIM)通过照明光栅产生干涉条纹,使传统宽场显微镜的分辨率提升一倍,且其照明功率远低于其他超分辨技术(如PALM、STORM),对冷冻样品的加热效应极低,非常适合低温成像。更重要的是,3D-SIM能够提供目标结构的三维超分辨信息,使得在cryo-FM图像中不仅能精准定位目标在xy平面的位置,还能获得其在z方向上的分布,从而显著提高与cryo-FIB图像之间的关联精度。
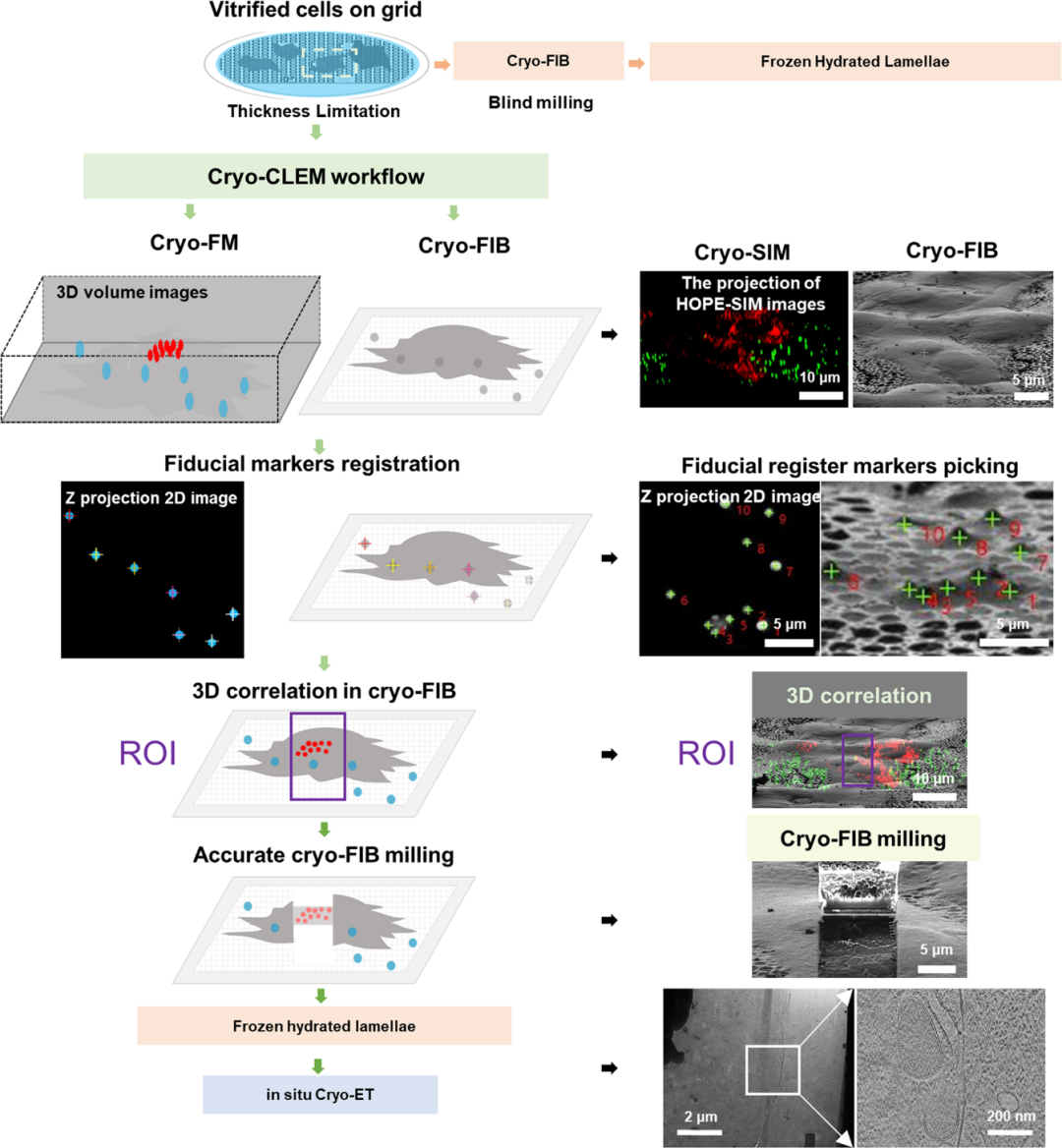
图1. 基于冷冻结构光照明显微镜(HOPE-SIM)的冷冻光电关联成像(cryo-CLEM)流程
实验表明,HOPE-SIM系统的定位精度可达约110 nm,足以高效引导cryo-FIB减薄。研究团队成功利用该系统制备了靶向线粒体、HeLa细胞中心体以及感染疱疹病毒的BHK-21细胞的冷冻含水切片,验证了其在多种生物学体系中的适用性。
ELI-TriScope:电子束、离子束、光束三束共焦,实时导航
ELI-TriScope系统核心理念可概括为“将荧光监控引入聚焦离子束减薄现场”。该系统在双束扫描电镜(SEM)内部集成了两套关键模块:一套基于冷冻样品杆的传输系统,另一套为内嵌的倒置宽场荧光成像系统(cryo-STAR)。通过精密校准,实现了电子束、离子束与光束三者聚焦于样品台上的同一点。
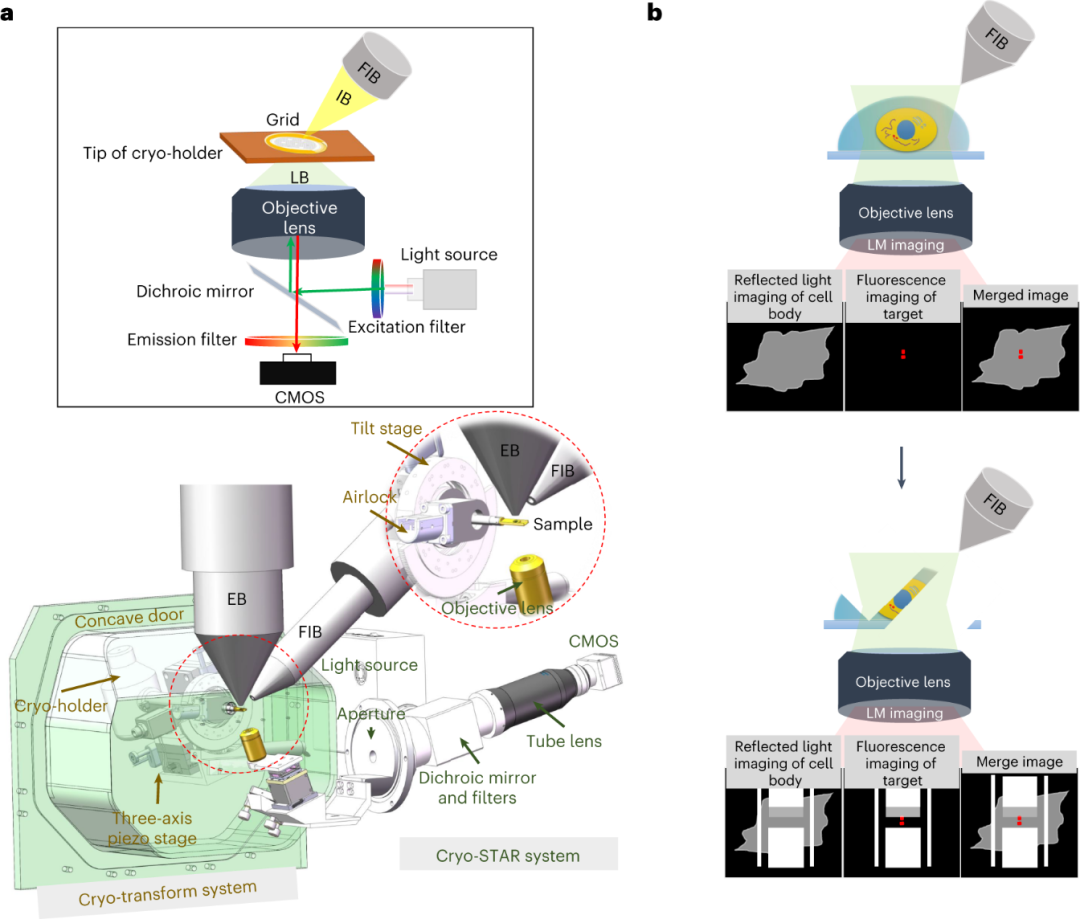
图2. ELI-TriScope 的系统设计原理
这意味着,在cryo-FIB减薄的同时,研究人员可以实时监测目标分子的荧光信号,实时调整减薄位置,直至将荧光信号所在的区域保留在最终切片中。整个过程不再需要样品在cryo-FM与cryo-SEM之间反复转移,也不再依赖荧光珠等外部标记物进行图像对齐。与已有技术相比,ELI-TriScope将单个冷冻切片的制备时间从2~2.5小时缩短至约0.8小时,并显著提高了成功率和定位精度。
为验证系统性能,研究团队选择了人源HeLa细胞中的中心体作为目标。中心体是细胞中高度有序、数量稀少(通常仅一个)的细胞器,传统方法极难精准制样。利用ELI-TriScope,团队成功制备了61个靶向中心体的冷冻切片,获得72套电子断层数据,靶向捕获成功率高达91%。随后通过cryo-ET成像与子断层平均(STA)分析,不仅观察到人类中心粒典型的九重对称结构、微管三联体(MTT)、远端附属结构等已知特征,还首次在人类中心粒中识别出一种新的内部环状结构——RD3,并揭示了A-C连接子在不同区域的结构差异。这项研究表明,ELI-TriScope不仅大幅提升了cryo-FIB制样的效率与精度,也为研究稀少、微小细胞器的高分辨率原位结构开辟了可行路径。
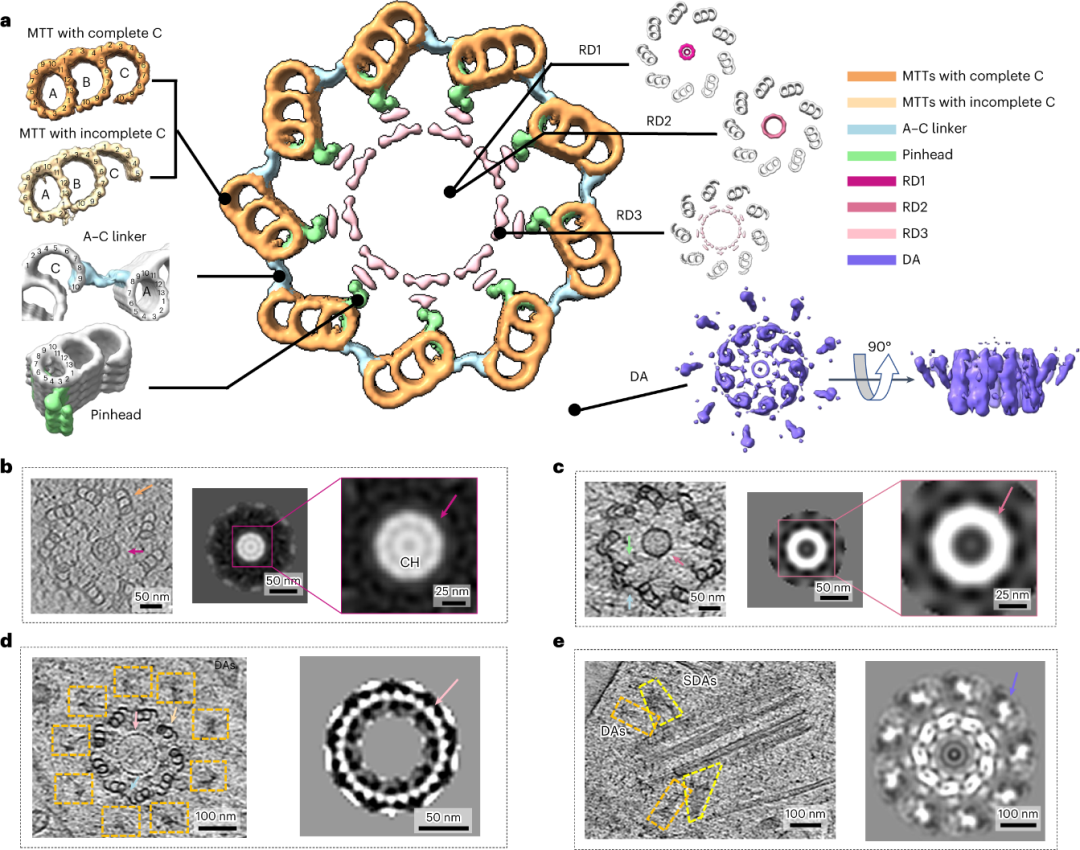
图3. 人中心粒的原位结构
a,通过子断层平均(STA)重构得到的人中心粒不同局部区域的横截面视图。b,断层切片中箭头所示的RD1和具有完整c-小管的MTTs(左),以及通过STA获得的RD1图谱(应用九重对称)的横截面视图(右)。c,断层切片中箭头所示的RD2、A-C连接子和针头(左),以及通过STA获得的RD2图谱(应用九重对称)的横截面视图(右)。d,断层切片中箭头和方框所示的RD3、具有不完整c-小管的MTTs、A-C连接子和DA(左),以及通过STA获得的RD3图谱(应用九重对称)的横截面视图(右)。e,断层切片中方框所示的远端下附属物(SDA)和DA(左),以及通过STA获得的DA图谱(应用九重对称)的横截面视图(右)。
HOPE-SIM和ELI-TriScope在技术路径上各具特色,但都指向同一个目标:让cryo-ET能够“看到”细胞中任何感兴趣的角落。
技术互补与未来展望
ELI-TriScope与HOPE-SIM代表了cryo-CLEM技术发展的两条重要方向:
HOPE-SIM通过提升cryo-FM本身的成像分辨率与维度,在减薄前完成高精度的三维关联,适合对定位精度要求极高、但可接受一定转移步骤的实验场景。
ELI-TriScope通则过将荧光成像系统直接嵌入FIB-SEM腔体,实现了减薄过程的实时监控,适用于需要动态反馈、目标结构极小或信号较弱的情况,极大提升了制样效率与成功率。
二者并非替代关系,而是互为补充。对于原位结构生物学研究而言,如何根据具体生物学问题选择合适的技术路径,将直接影响实验的成败与效率。
从更宏观的角度来看,这两项技术的发展反映了冷冻电子断层扫描领域的一个核心趋势:样品制备正在从“经验驱动”走向“精准导航”。随着荧光标记技术、超分辨成像、自动化控制与数据处理方法的不断融合,我们有理由相信,未来将有更多复杂的、稀有的、动态的细胞事件在近原子分辨率下被揭示。
对于正在进入这一领域的科研工作者们而言,理解这些技术背后的科学问题与工程思路,不仅有助于掌握当前cryo-ET样品制备的最前沿方法,更能在自己的研究中灵活选择或组合不同工具,真正实现“看见生命”的科学目标。
参考文献:
1.Li, S., Jia, X., Niu, T. et al. HOPE-SIM, a cryo-structured illumination fluorescence microscopy system for accurately targeted cryo-electron tomography. Commun Biol 6, 474 (2023). https://doi.org/10.1038/s42003-023-04850-x
2.Li, S., Wang, Z., Jia, X. et al. ELI trifocal microscope: a precise system to prepare target cryo-lamellae for in situ cryo-ET study. Nat Methods 20, 276–283 (2023). https://doi.org/10.1038/s41592-022-01748-0
相关推荐:
【科技前沿】孙飞研究组与合作者共同揭示哺乳动物精子鞭毛通过原位翻译–折叠的偶联机制维持持久运动
【科技前沿】张宏研究组揭示机械感知通道通过Ca²⁺瞬变触发自噬体形成的分子机制

中国生物物理学会官方订阅号,
为BSC会员及生物物理领域专业人士服务。
投稿及授权请联系:bscoffice@bsc.org.cn。
原标题:《【科技前沿】精准聚焦生命奥秘——冷冻原位光电关联成像技术》

