Adv Sci | 徐医大肖诚/周春艺/崔桂云团队揭示黑质 - 丘脑底核多巴胺能环路调控痛觉新机制
提起帕金森病,人们最先想到的往往是手抖、僵硬、走路缓慢,却忽略了最让患者煎熬的,是不为人知的慢性疼痛。临床数据显示,近八成帕金森患者都会被疼痛困扰,其中三成患者因疼痛彻夜难眠、无法自理,生活质量比仅有运动障碍的患者低了一半以上。
那么,帕金森疼痛究竟由大脑哪条环路控制?

2026年4月7日,徐州医科大学肖诚、周春艺和徐州医科大学附属医院崔桂云团队在《Advanced Science》上发表的研究《Nigra-Subthalamic Dopaminergic Circuitry Modulates and Represents Distinct Pain Modality in Physiological and Pain States in Mice》,第一次发现了一条全新的痛觉环路。
该研究发现黑质致密部 - 丘脑底核多巴胺环路专门调控对侧机械痛,不影响热痛;该通路通过丘脑底核的 D2 样受体发挥作用,黑质网状部 GABA 能神经元是其上游调控节点;激活这条环路或丘脑底核 D2 受体,可缓解神经病理性疼痛与帕金森痛,为两类疼痛治疗提供新靶点。

SNc-STN 多巴胺通路调控机械痛
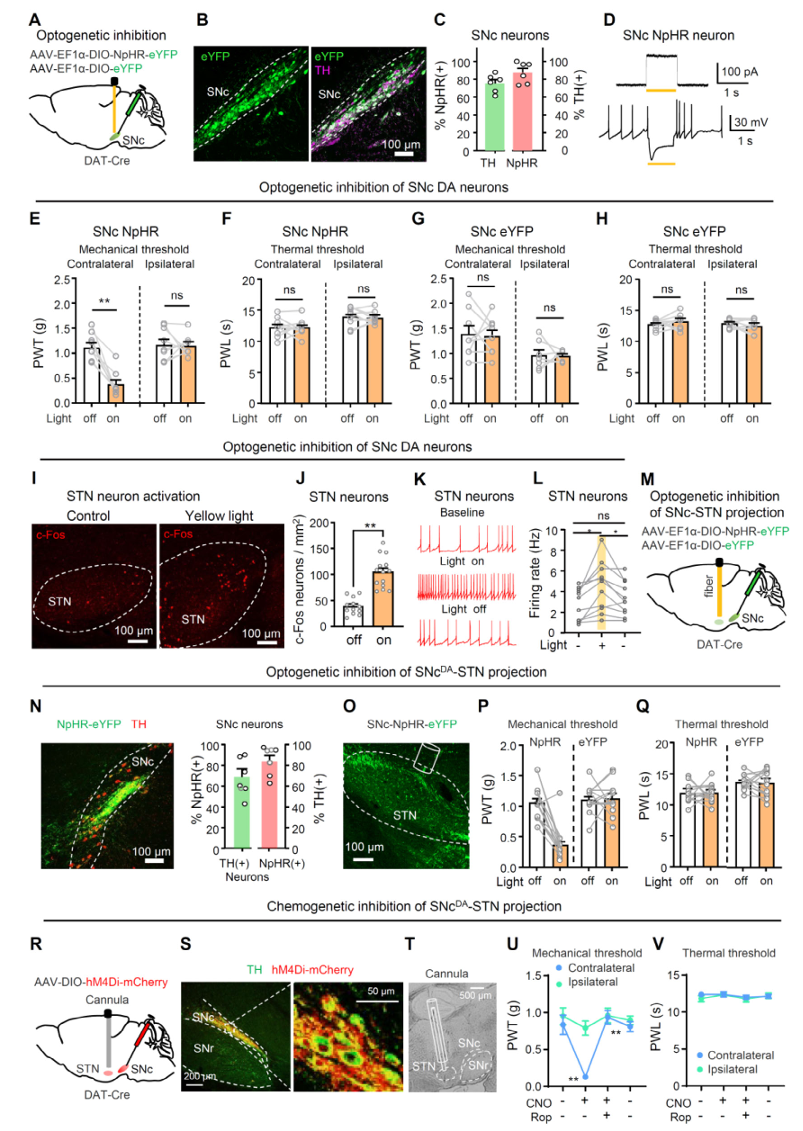
研究者用光遗传学和化学遗传学操控黑质致密部(SNc)的多巴胺神经元,发现了一个有趣的分工:
抑制SNc多巴胺神经元或其投向丘脑底核(STN)的神经纤维,小鼠对侧爪子的机械痛显著增强(一碰就疼),热痛完全没有变化。进一步发现,STN里的D2受体是关键,用D2受体激动剂能逆转痛敏,而D1受体没用。在神经病理痛(SNI模型)和帕金森模型小鼠中,激活这条通路能明显缓解对侧机械痛,同样不影响热痛。
因此,SNc→STN多巴胺通路是一条专门调控对侧机械痛的镇痛环路。
疼痛会关掉自己的镇痛开关
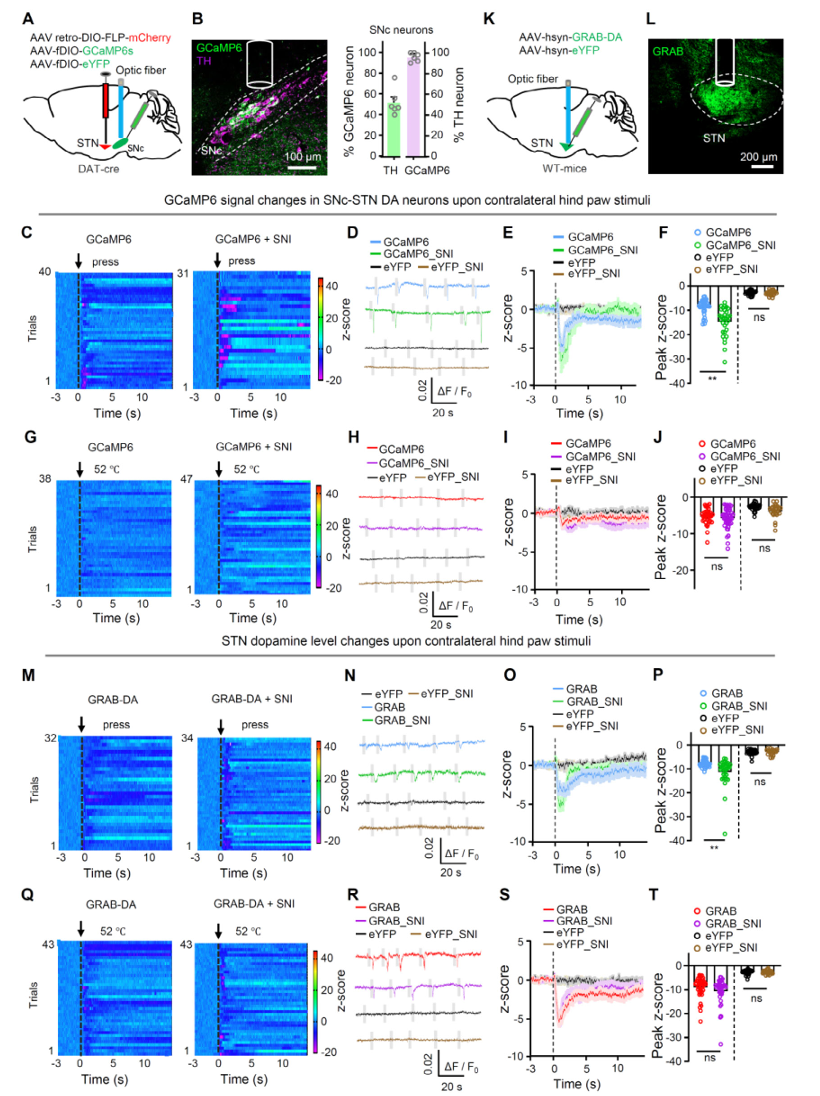
用光纤钙信号和多巴胺探针实时记录:给小鼠对侧爪子机械刺激时,SNc→STN多巴胺神经元活动显著下降 → STN内多巴胺释放减少;在神经病理痛小鼠中,这种下降更明显。也就是说,疼的时候,这条镇痛环路会被抑制。在帕金森模型小鼠中,SNc多巴胺神经元本来就受损,STN多巴胺本底就低。痛刺激带来的下降虽然变弱,但机械痛敏依然存在。直接往STN注射D2激动剂,能同时缓解机械痛和部分热痛。
因此,疼痛本身会抑制这条镇痛环路,形成越疼→镇痛越弱→更疼的恶性循环。
谁在抑制镇痛系统?
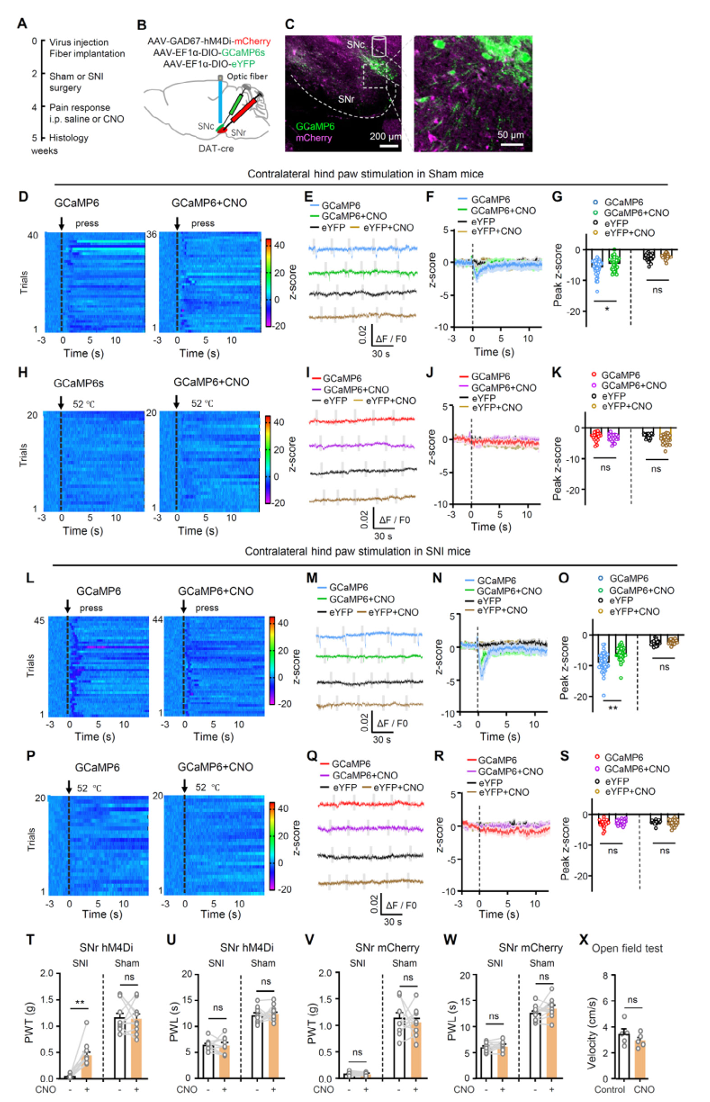
用逆行示踪和电生理记录,找到了上游黑质网状部(SNr)的GABA能神经元。
SNr的GABA能神经元直接抑制投向STN的SNc多巴胺神经元。机械刺激和热刺激都会激活SNr GABA能神经元,进而抑制下游多巴胺通路。用化学遗传学抑制SNr GABA能神经元,能减弱机械刺激带来的多巴胺神经元抑制,并提升神经病理痛小鼠的机械痛阈值。
也就是说,疼痛先激活 SNr ,再抑制 SNc-STN镇痛开关,最终加重疼痛。
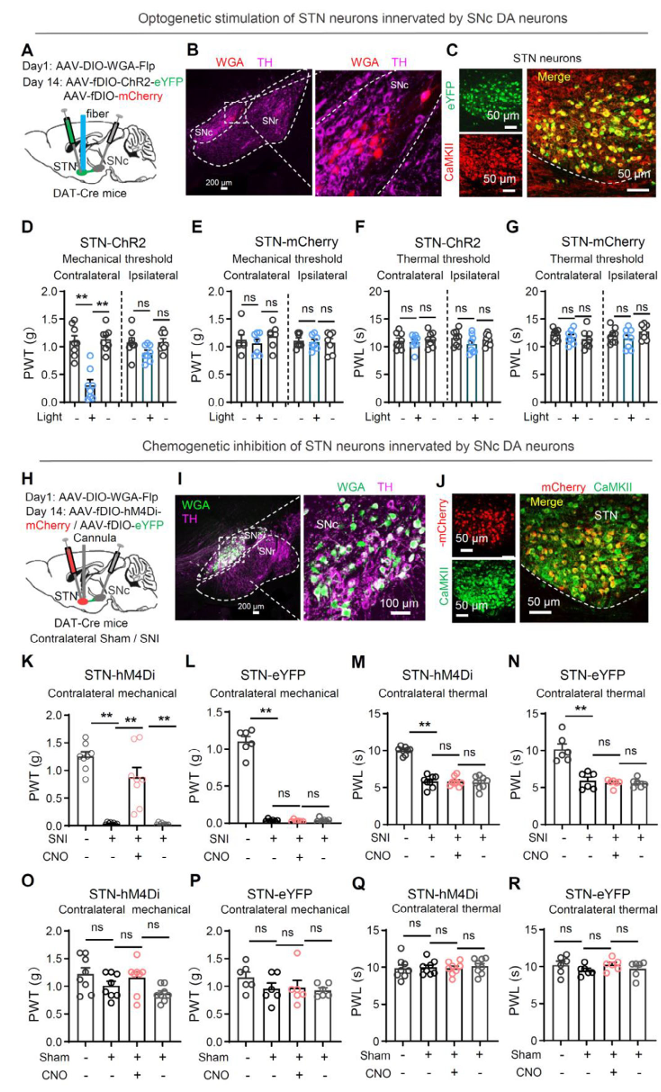
STN内部也分工明确
用跨突触病毒标记接受 SNc 投射的 STN 神经元,发现激活这群神经元会诱发对侧机械痛敏,抑制则缓解神经病理痛的对侧机械痛,不影响热痛。这说明STN 内部是分工的,和 SNc 相连的这部分神经元,专门调控对侧机械痛,和整体 STN 同时调控双侧、多种疼痛不同。
全文总结
本研究揭示了SNrGABA-SNcDA-STN这条全新的基底神经节疼痛调控环路,它特异性调节对侧机械痛,依赖 STN 的 D2 样受体;生理状态下维持正常痛阈,病理状态下因多巴胺不足、神经元过度兴奋引发痛敏;抑制上游 SNr 或激活该环路、STN D2 受体,均可缓解神经病理痛与帕金森痛,是两类疼痛共有的潜在治疗靶点。
小编寄语:
帕金森病的运动症状(震颤、僵直、迟缓)早已为人熟知,但疼痛长期被忽视。临床数据显示,超过80%的帕金森患者经历过疼痛,且其严重程度常高于普通人群。但这种疼痛的神经机制,一直模糊不清。
徐州医科大学肖诚、周春艺、崔桂云团队的这项研究,第一次在基底节环路中找到了答案。他们发现了一条从黑质致密部(SNc)到丘脑底核(STN)的多巴胺环路,专门调控对侧机械痛,不参与热痛。该环路通过STN的D2样受体发挥作用,上游受黑质网状部(SNr)GABA能神经元的抑制性调控。在生理状态下,它维持正常痛阈;在病理状态下(神经病理痛、帕金森病),多巴胺不足导致环路功能下降,STN神经元过度兴奋,引发痛敏。更关键的是,激活该环路或STN的D2受体,可同时缓解两类疼痛,为神经病理痛和帕金森痛提供了共同的精准靶点。

原文链接:
https://doi.org/10.1002/advs.202519913
原标题:《Adv Sci | 徐医大肖诚/周春艺/崔桂云团队揭示黑质 - 丘脑底核多巴胺能环路调控痛觉新机制》

