登上Nature:中国团队新型碱基编辑疗法,成功治疗β-地中海贫血
撰文丨王聪
编辑丨王多鱼
排版丨水成文
2026 年 4 月 8 日,国际顶尖学术期刊 Nature 在线发表了正序生物与广西医科大学第一附属医院、上海科技大学、复旦大学、上海临床研究中心合作临床完成(上海科技大学陈佳教授、广西医科大学第一附属医院赖永榕教授、复旦大学杨力教授、正序生物牟晓盾博士为论文共同通讯作者)的研究成果,论文题为:Clinical application of base editing for treating β-thalassaemia。
该研究利用了基于团队自主开发的变形式碱基编辑器(transformer Base Editor,tBE)的碱基编辑疗法 CS-101 治疗 β-地中海贫血患者的 IIT 临床试验结果,5 名输血依赖型 β-地贫患者在接受单次治疗后,造血功能快速重建,总血红蛋白和 HbF 水平迅速提升且持续高水平表达,迅速摆脱输血依赖。
据悉,这是中国基因编辑药物管线临床结果首次发表在 Nature 正刊,也是中国地贫领域临床研究首次发表于 Nature 正刊。

地中海贫血:全球性遗传疾病挑战
β-地中海贫血是一种常见的单基因遗传疾病,全球每年有超过 4 万名儿童患病。这种疾病由于 β-珠蛋白合成减少或缺失,导致α/非α珠蛋白链失衡,过量的 α-珠蛋白链形成毒性聚集体,引发贫血、无效红细胞生成以及铁代谢紊乱。
对于重度患者,特别是输血依赖型 β-地中海贫血(TDT),终身定期输血是维持生命的唯一选择。传统治疗方法包括定期红细胞输注和铁螯合治疗,但这些方法无法根治疾病,且长期输血会导致铁过载等严重并发症。
异基因造血干细胞移植,虽然是一种潜在的治愈方法,但面临供体匹配困难、移植物抗宿主病以及移植相关死亡风险等挑战。
基因编辑:从“可编辑”到“安全精准编辑”
以 CRISPR 为代表的基因编辑技术为遗传疾病的治疗带来了革命性希望。此前,研究人员已经尝试使用 CRISPR-Cas9 技术编辑 BCL11A 的红系增强子区域,通过重新激活 γ-珠蛋白基因的表达来治疗 β-地中海贫血。该疗法已获得 FDA批准用于治疗 12 岁及以上伴有复发性血管闭塞危象的镰状细胞病(SCD)和输血依赖型 β-地中海贫血(TDT)。
然而,CRISPR-Cas9 技术会产生 DNA 双链断裂,这会触发 p53 依赖的 DNA 损伤反应,导致细胞周期停滞和凋亡,并存在染色体异常甚至致癌风险。
上海科技大学陈佳教授团队开发的变形式碱基编辑器(tBE)属于下一代基因编辑技术。它通过巧妙的“锁-钥匙”设计,从根本上避免了 CRISPR-Cas9 技术导致的 DNA 双链断裂及脱靶风险,实现了从“可编辑”到“安全、精准编辑”的跨越。
tBE技术原理:精准靶向 BCL11A 结合基序
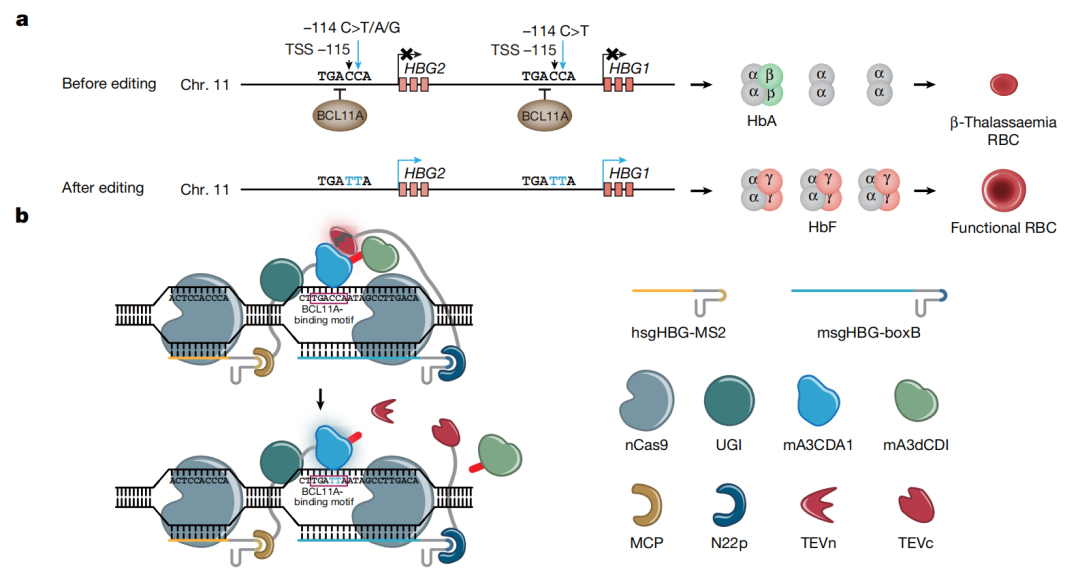
tBE 技术的核心在于精准编辑 HBG1 和 HBG2 启动子区域中的 BCL11A 结合基序。BCL11A 是成人期 γ-珠蛋白基因的主要转录抑制因子,而 γ-珠蛋白是胎儿血红蛋白(HbF)的组成部分。
在胎儿期,HbF 是主要的血红蛋白类型,但出生后逐渐被成人血红蛋白(HbA)取代。通过编辑 BCL11A 结合基序,tBE 能够破坏 BCL11A 的结合,重新激活 γ-珠蛋白表达,从而增加 HbF 水平。
tBE 系统采用双 sgRNA 设计:一个辅助 sgRNA(hsgHBG-MS2)和一个主 sgRNA(msgHBG-boxB)。只有当两个 sgRNA 在靶点位置共定位时,脱氨酶抑制剂才会被切割,激活脱氨酶活性,实现精准的 C-to-T 碱基编辑。这种设计确保了编辑的特异性,只有在靶点位置才会发生编辑,其他地方脱氨酶活性被抑制,从而避免了脱靶突变。
临床试验结果:5 名患者全部摆脱输血
这项临床试验纳入了 5 名重度输血依赖型 β-地中海贫血患者,患者的中位年龄为 18.8 岁,其中 3 名男性,2 名女性,患者基因型包括 β0/β0、β0/β0-like 和 β0/β+。
治疗过程包括采集患者自体的 CD34+ 造血干细胞,使用 tBE 进行体外碱基编辑,然后回输给经过白消安清髓预处理的患者,中位随访时间为 23.0 个月。
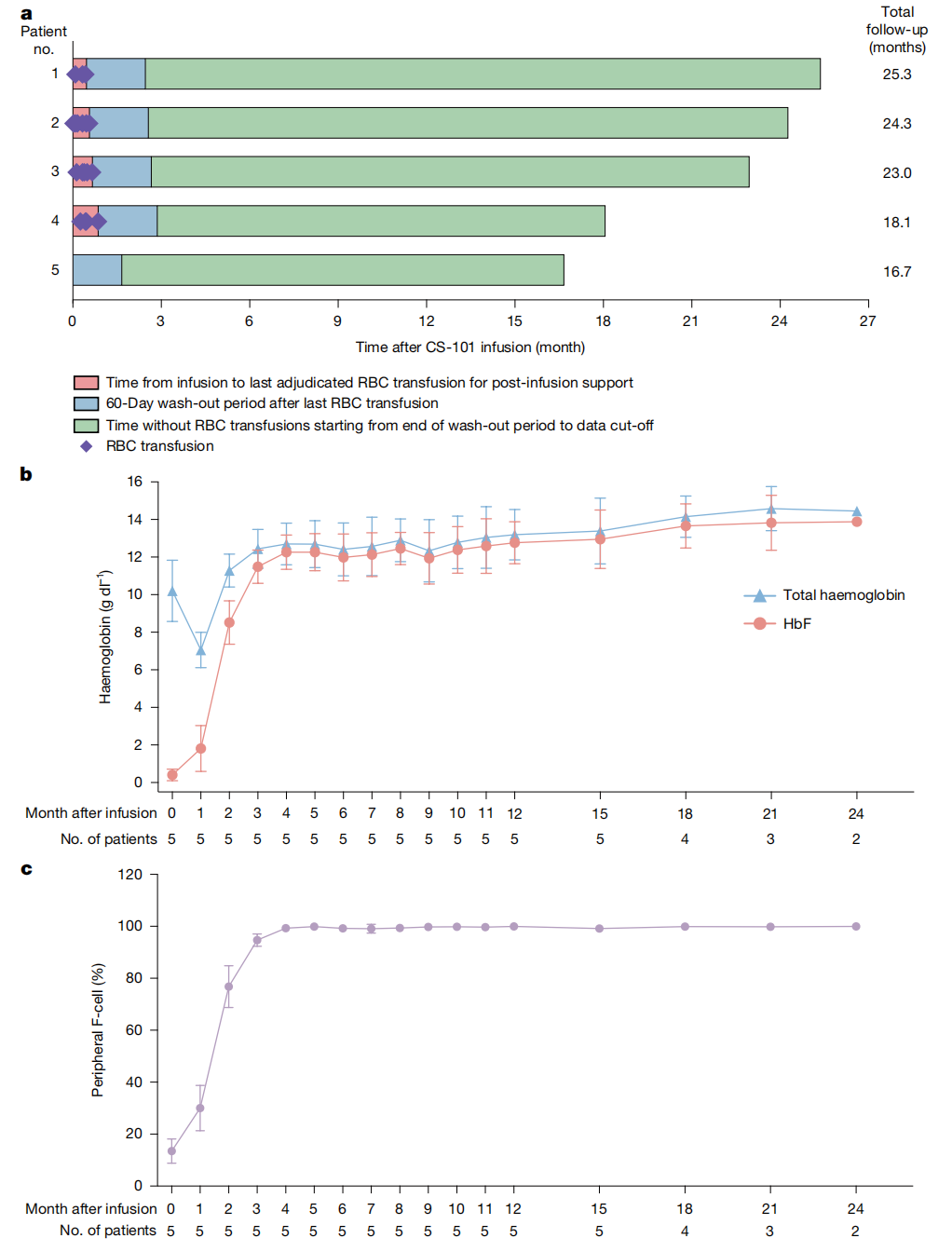
临床治疗效果惊人:所有 5 名患者(100%)均停止了红细胞输注,平均最后一次输血时间为 CS-101 输注后 16 天。所有患者均达到了主要终点——输注后 3 个月起的 6 个月输血独立。
更令人振奋的是,所有患者都实现了长期输血独立,输血自由期持续 15.0-22.9 个月。
血红蛋白水平:快速且持续提升
CS-101 治疗后,患者的总血红蛋白和 HbF 水平迅速提升,输注后 3 个月,平均总血红蛋白浓度为 12.4±1.0 g/dL,平均 HbF 浓度为 11.5±0.9 g/dL。
这些水平在整个随访期间保持相似或更高水平,表明患者的造血重建迅速。值得注意的是,3名 β0/β0 或 β0/β0-like基因型患者几乎不产生 β-珠蛋白,在实现输血独立后,他们的 HbF 水平几乎接近 100%。相比之下,β0/β+ 基因型患者保留了部分 β-珠蛋白产生能力,在输血独立后继续合成少量 HbA,因此他们的 HbF 比例未达到 100%。
安全性与特异性:未检测到脱靶编辑
安全性是基因编辑疗法的关键考量。在这项研究中,CS-101 的不良事件通常与白消安清髓预处理和自体造血干细胞移植一致,未报告死亡或癌症发生。
编辑效率稳定:在患者外周血单个核细胞中,BCL11A 结合基序的编辑频率从第 1 个月起保持稳定,在整个随访期间始终维持在 34% 以上。在骨髓血细胞中,第 3 个月的平均碱基编辑频率为 39.8±7.2%,并在随访期间保持稳定。
无脱靶突变:研究团队使用 Cas-OFFinder、Digenome-seq 和 COSMID 算法鉴定了 145 个潜在脱靶位点。在所有 5 名患者中,这些位点均未检测到脱靶编辑。
这一结果与传统的 CRISPR-Cas9 技术以及碱基编辑器形成鲜明对比,tBE 不需要产生 DNA 双链断裂,从而避免了相关的细胞毒性和染色体异常风险。其他碱基编辑器,例如 hA3A-BE3、ABE8e 等,虽然在靶点编辑效率和 HbF 诱导方面也很高效,但它们在某些位点诱导了显著的脱靶编辑。
未来展望
总的来说,该研究证明了基于 tBE 开发的碱基编辑疗法 CS-101 注射液展现了出色的疗效、安全性以及持久性,效果优于其他基因疗法,具有显著的临床应用价值。CS-101 注射液作为全球首个且唯一在治疗后有两年以上长期观察数据的碱基编辑疗法,具有成为治疗 β-血红蛋白病的全球 Best-in-Class 基因编辑药物的潜力。
这项研究标志着基因编辑治疗 β-地中海贫血的重要进展,基于 tBE 的碱基编辑疗法不仅展示了良好的安全性和有效性,还为其他遗传疾病的治疗提供了新思路。
据悉,正序生物目前正在针对全球多个国家的 β-血红蛋白病患者开展临床治疗,并已治愈多位国内外患者。相关药物管线 CS-101 除了在进行治疗 β-地中海贫血的临床试验外,还在进行治疗镰状细胞病(SCD)的临床试验。
值得一提的是,2026 年 4 月 1 日,《新英格兰医学杂志》(NEJM)同期发表了 3 篇关于基因编辑治疗血红蛋白病的临床试验结果,分别是 CRISPR-Cas12a 基因编辑治疗镰状细胞病、CRISPR-Cas12a 基因编辑治疗 β-地中海贫血、碱基编辑治疗镰状细胞病。
前两项疗法来自张锋等人创立的 Editas Medicine,第三项疗法来自刘如谦等人创立的 Beam Therapeutics。分别代表了 CRISPR-Cas12a 和碱基编辑两种技术平台的重要进展。



这些研究共同推动基因编辑技术向精准化发展,为遗传疾病患者摆脱疾病负担、改善生活质量带来了新的希望。
论文链接:
https://doi.org/10.1038/s41586-026-10342-9
原标题:《登上Nature:中国团队新型碱基编辑疗法,成功治疗β-地中海贫血,5名患者摆脱输血依赖》

