【科技前沿】张宏研究组揭示机械感知通道通过Ca²⁺瞬变触发自噬体形成的分子机制
内质网是细胞内由片状和管状膜结构组成的网络系统,负责蛋白质的合成与折叠,也是细胞内主要的Ca2+储存库。当内质网出现局部损伤时,细胞会启动“内质网自噬”,形成自噬小体包裹受损部分并送去降解,就像清理垃圾一样。但这一过程具体如何启动、信号如何转导以及形成自噬小体的膜从何而来一直未被阐明。
2026年4月2日,中国科学院生物物理研究所张宏团队在《Molecular Cell》发表题为“Mechanosensory channels mediate Ca2+transients to trigger assembly of autophagosome initiation sites for degradation of ER subdomains”的研究论文,首次揭示机械感知通道介导Ca2+瞬变触发内质网片段降解的分子机制。该发现为内质网功能障碍相关疾病的治疗提供了新的研究方向。

研究人员利用超分辨多模态活细胞成像等技术发现,在长期饥饿、胆固醇稳态失常或高Ca2+损伤等应激条件下,内质网中Ca2+含量较高的片状亚结构域会发生扩张,随后被自噬小体包裹并降解。令人意外的是,电子显微镜和光电关联冷冻电子断层扫描结果显示,包裹这些高Ca2+片状内质网的自噬小体膜,竟然直接源于内质网重塑。研究还发现,这一过程依赖两个关键蛋白——内质网自噬受体FAM134B和脂化LC3的协同作用,而传统自噬所需要的ATG14和ATG9蛋白则并非必需。
进一步研究表明,这两种机械感知通道蛋白PIEZO1和TRPV1富集在高Ca2+的片状内质网上。它们能感知钙离子浓度的变化,并触发局部钙离子释放,形成短暂的钙瞬变。这一信号继而触发自噬起始FIP200复合物发生液-液相分离,最终启动内质网自噬。
内质网Ca2+稳态失衡以及内质网自噬功能异常与神经疾病和癌症等多种疾病的发生发展密切相关。该研究揭示的应激诱导高Ca2+含量内质网片段被选择性自噬降解的机制,为探索内质网Ca2+稳态失衡相关疾病的发病机制,及其潜在的干预靶点提供了重要线索。
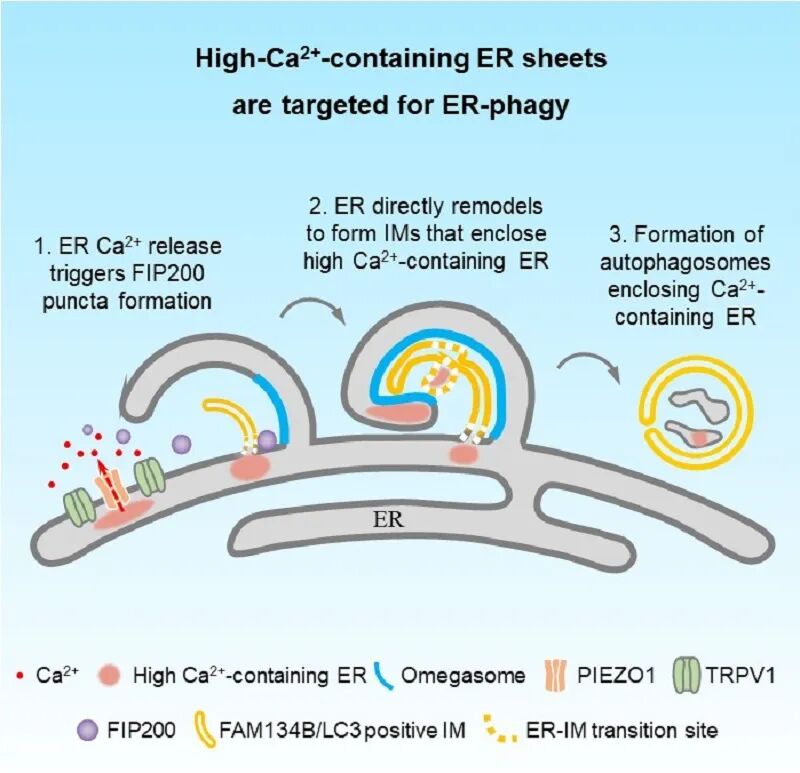
图 含高Ca2+内质网的自噬小体形成模式图
中国科学院生物物理研究所张宏研究员为该论文的通讯作者,张宏研究组马晓丽助理研究员为第一作者。生物物理所纪伟研究员、胡俊杰研究员、王曦研究员,北京大学医学部郑巧霞研究员,同济大学项耀祖教授也对该研究做出了重要贡献。研究得到国家自然科学基金委和新基石科学基金会等机构的资助。
文章来源于:中国科学院生物物理研究所
文章链接:
https://www.sciencedirect.com/science/article/pii/S1097276526001589
相关推荐:
【科技前沿】Molecular Cell | 张恒团队揭示TIGR–TasH系统分子机制并发展基因编辑新工具
【科技前沿】王立堃研究组揭示长期内质网应激下钙离子调控CALR-IRE1α互作驱动IRE1α活性动态波动的新机制
中国生物物理学会官方订阅号,
为BSC会员及生物物理领域专业人士服务。
投稿及授权请联系:bscoffice@bsc.org.cn。
原标题:《【科技前沿】张宏研究组揭示机械感知通道通过Ca²⁺瞬变触发自噬体形成的分子机制》

