【科技前沿】Molecular Cell | 张恒团队揭示TIGR–TasH系统分子机制并发展基因编辑新工具
本篇报道来源于中国生物物理学会冷冻电镜分会委员张恒教授投稿。
RNA引导的核酸酶依赖向导RNA识别靶序列并进行特异性切割,是基因编辑技术的核心工具。通过对核酸酶或向导RNA进行工程化改造,可优化或改变其分子功能,例如实现核酸酶到切口酶的活性转化。切口酶在双链DNA上产生单链切口,可促进同源重组修复,并提升碱基编辑和先导编辑的精准度。目前,链特异性切口酶活性的实现,主要依赖对蛋白关键催化位点的突变。相比之下,在保持核酸酶结构与功能完整的情况下,通过改造向导RNA实现切口酶活性,可实现更灵活的切割模式调控,例如在不同位点针对不同DNA链产生切口。然而,基于RNA改造实现切口酶活性的研究仍较为有限。如何在分子机制解析的基础上设计具有跨靶点普适性的工程化向导RNA,仍有待进一步探索。
2026年3月13日,天津医科大学基础医学院/肿瘤医院张恒课题组在Molecular Cell上发表了题为“Molecular Basis for Dual-spacer-guided Target Cleavage by the TIGR-TasH System”的研究论文。该研究阐明了RNA引导核酸酶TIGR-TasH系统的分子机理,并提出“向导RNA调控型”新型基因编辑机制。通过理性设计向导RNA,该系统可在双链DNA上产生单链切口(nick),显示出TIGR-TasH系统在基因编辑技术开发中的应用前景。

TIGR-Tas系统是一类由RNA引导、靶向双链DNA的新型核酸作用体系,主要分布于细菌、古菌及病毒中。其典型基因座包括TIGR(Tandem Interspaced Guide RNA)阵列及Tas(TIGR-associated)蛋白编码基因。TIGR阵列由重复序列与间隔序列交替排列组成,可被转录并加工为成熟向导RNA(tigRNA)。成熟tigRNA含有两个串联排列的间隔序列,可分别与靶DNA双链的两条单链配对,实现对双链底物的协同靶向。该识别模式不依赖PAM或PFS等靶标邻近基序,理论上拓展了可靶向序列范围。Tas蛋白以源自真核box C/D家族snoRNP复合体的Nop结构域为核心,并常与RuvC或HNH等核酸酶结构域融合,形成具有DNA切割活性的TasR或TasH。Tas核酸酶仅约300-400 aa,大小约为SpCas9的30%,在作为基因组编辑工具时具有明显的小型化优势。然而,该系统的向导RNA产生、底物识别及变构激活等过程的分子机制仍不清楚。
团队对噬菌体来源的SpTasH系统(下称TasH)开展研究。在复合体体外组装实验中,研究人员意外发现,TasH仅依赖自身Nop结构域活性位点处理TIGR转录本,生成36-nt成熟tigRNA。这与此前报道的TaTasR系统需要宿主因子参与tigRNA处理不同,提示TasH系统具备多靶点基因编辑的潜力。在底物识别方面,团队发现TasH在Mg2+或Mn2+等二价金属离子存在下,可切割末端完全配对的双链DNA。生化实验和结构解析证实,一个独特的β-发夹精确限定TasH对靶DNA的识别长度,并参与招募HNH核酸酶结构域;一个保守的赖氨酸残基在DNA双链打开过程中发挥关键作用。此外,该系统对RNA–DNA杂交区的错配容忍度较低,具有高保真的底物靶向识别特异性。
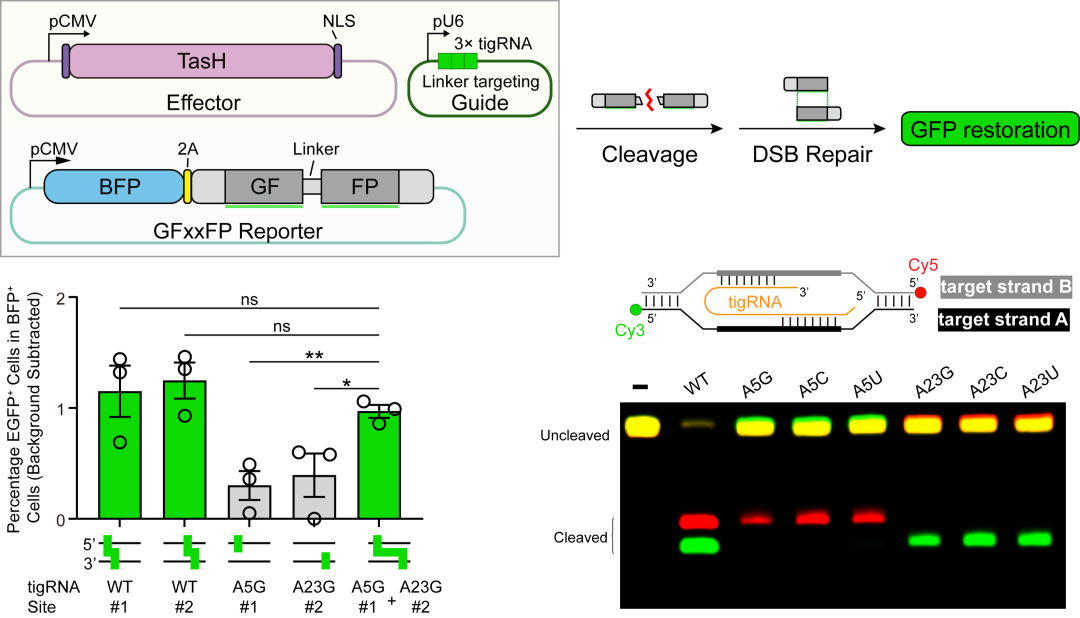
RNA介导的TIGR-TasH切口酶活性
Tas蛋白普遍具有同源二聚结构特征,较难通过蛋白水平突变实现nickase活性。研究团队在理解TIGR-TasH分子机制的基础上,通过在tigRNA重复区引入突变,调控其相邻配对区的DNA链切割活性,并在人细胞系中进行了验证。该策略首次实现了由向导RNA重复区定义的链特异性切口酶活性,为构建高精度基因编辑工具(如碱基编辑和先导编辑)提供了新的分子底盘。
综上,这项研究揭示了TIGR-TasH系统从tigRNA自加工、复合体组装到双链识别与变构激活的完整分子机制。作为一类小型化、无PAM限制的RNA引导核酸靶向系统,TIGR-TasH有望通过进一步工程化改造发展为新一代基因编辑工具。天津医科大学张恒教授为论文通讯作者,杨洁博士、王童谣、刘志坤、孙仰跃、吴文齐博士、詹焱程博士为论文共同第一作者。
天津医科大学基础医学院/肿瘤医院张恒课题组长期从事免疫防御系统相关基础研究,聚焦新型核酸中心型微生物免疫系统的功能与分子机制,并开展衍生技术工具的开发与应用转化,以通讯作者在Nature, Nature Microbiology, Nature Chemical Biology, Molecular Cell, Cell Research等期刊发表研究论文。课题组现招聘测序、微生物学、生物化学等方向博士后,欢迎联系。
实验室官网:https://www.zhanglab.life/
文章链接:https://doi.org/10.1016/j.molcel.2026.02.017

相关推荐:
【科技前沿】王立堃研究组揭示长期内质网应激下钙离子调控CALR-IRE1α互作驱动IRE1α活性动态波动的新机制
【科技前沿】Cell子刊 | 中国农业大学杨丽团队揭示了光调控植物细菌病原体毒力的分子机制
中国生物物理学会官方订阅号,
为BSC会员及生物物理领域专业人士服务。
投稿及授权请联系:bscoffice@bsc.org.cn。
原标题:《【科技前沿】Molecular Cell | 张恒团队揭示TIGR–TasH系统分子机制并发展基因编辑新工具》

