Mol Cell:泛素连接酶RNF25通过调控整合应激反应介导mRNA损伤耐受

生命科学
Life science
DNA和RNA是遗传信息传递与表达的核心分子。然而,在内源代谢压力及外源环境因素的持续作用下,这两类核酸不可避免地发生损伤,从而影响细胞稳态。目前,围绕DNA损伤应答及修复机制的研究已较为系统和深入。然而,由于RNA分子半衰期较短且可通过持续转录进行补充,学界对其损伤的感知、应答及修复机制仍缺乏系统性认识。近年来的研究表明,紫外辐照及内源性代谢产物诱导的炎症反应和细胞应激反应,主要由RNA损伤介导,这提示RNA损伤应答在细胞命运调控中具有重要作用。此外,多数基因毒性因子在诱导DNA损伤的同时也会造成RNA损伤,这些发现进一步提示:在传统上被认为主要靶向DNA的化疗药物作用网络中,RNA损伤应答可能发挥关键的细胞毒性调控作用。
2026年3月23日,来自吉林大学、慕尼黑大学及剑桥大学等多家科研机构的研究团队合作在Cell Press细胞出版社旗下期刊Molecular Cell上在线发表了题为“RNF25 confers mRNA damage tolerance by curbing activation of the integrated stress response”的研究论文。该研究系统揭示了RNA损伤在化疗药物阿扎胞苷发挥作用过程中的关键地位,并进一步阐明泛素连接酶RNF25通过介导核糖体蛋白的泛素化修饰,抑制整合应激反应(Integrated stress response,ISR)的激活以及细胞对阿扎胞苷的毒性响应。
为特异性解析RNA损伤诱导的细胞应答反应,研究团队基于胞苷与脱氧胞苷在细胞内代谢途径上的差异,构建了急性髓系白血病(acutemyeloidleukemia,AML)和骨髓增生异常综合征(myelodysplastic syndrome,MDS)的化疗药物地西他滨(5-氮杂脱氧胞苷)与阿扎胞苷(5-氮杂胞苷)的对照分析体系。结合CRISPR全基因组敲除筛选结果,研究发现,泛素连接酶RNF25特异性抑制阿扎胞苷诱导的细胞毒性,而对地西他滨的处理无明显影响,提示RNF25参与调控RNA损伤相关的细胞毒性应答过程。
进一步结合多个不同遗传背景下的CRISPR全基因组敲除筛选,研究系统绘制了阿扎胞苷急性与慢性作用的分子调控图谱,并明确GCN1-GCN2依赖的ISR的激活是其急性细胞毒性的主要来源。
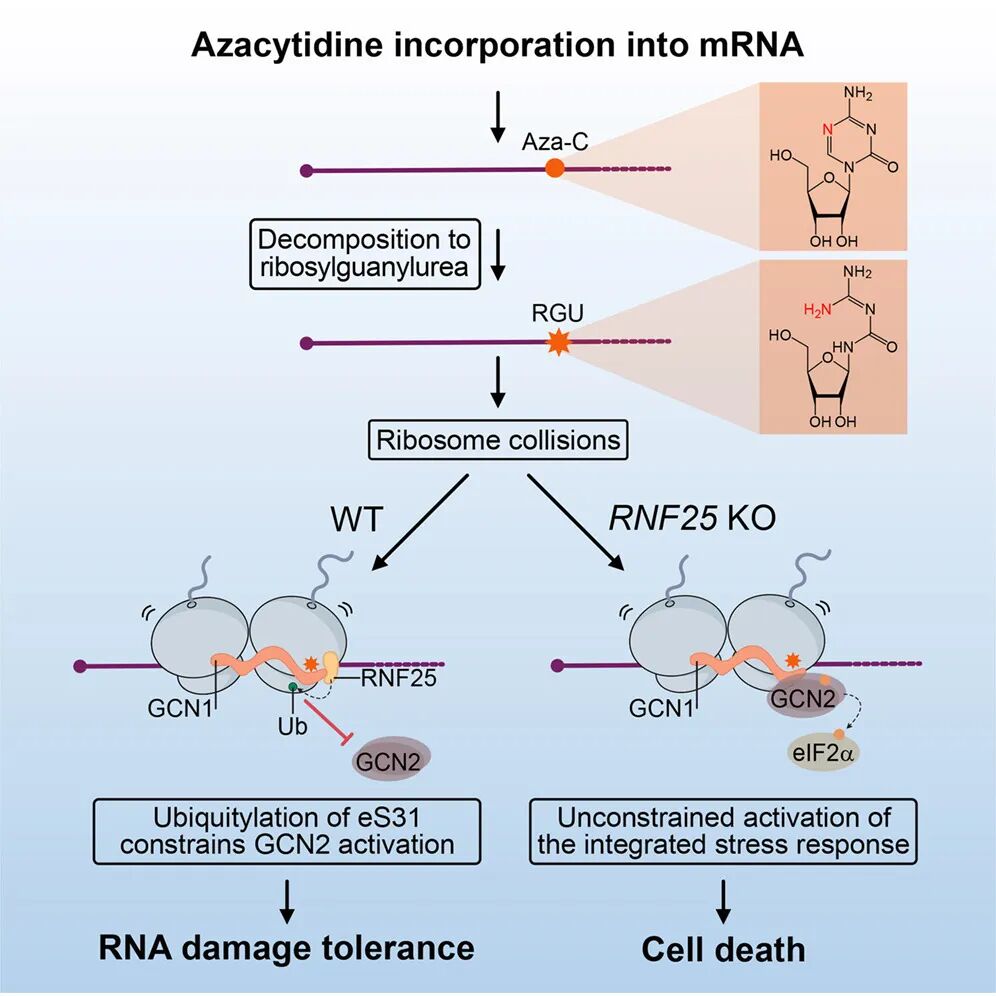
图1 研究内容示意图
在分子机制层面,阿扎胞苷经三磷酸化后掺入mRNA,并发生开环及脱甲酰化修饰,形成异常的RGU结构,从而诱导核糖体停滞及碰撞。该异常翻译状态可被GCN1识别,进而募集GCN2并激活ISR,最终驱动细胞毒性效应。泛素连接酶RNF25可通过与GCN1相互作用特异性介导核糖体小亚基蛋白eS31的第113位赖氨酸发生泛素化修饰,从而限制ISR的过度激活,发挥细胞保护作用。
综上所述,该研究首次证实阿扎胞苷通过诱发RNA损伤并激活相关细胞应答通路发挥细胞毒性作用。同时,研究鉴定了RNF25抑制阿扎胞苷细胞毒性的分子机制,揭示了一条全新的RNA损伤耐受调控通路。该工作不仅阐明RNA损伤在阿扎胞苷药效中的关键作用,还进一步表明RNA损伤诱导的应激反应是决定急性髓系白血病(AML)及骨髓增生异常综合征(MDS)化疗敏感性的关键因素,为通过靶向RNA损伤应答通路提升化疗疗效提供了重要理论依据。

相关论文信息
论文原文刊载于Cell Press细胞出版社期刊
Molecular Cell
▌论文标题:
RNF25 confers mRNA damage tolerance by curbing activation of the integrated stress response
▌论文网址:
https://www.sciencedirect.com/science/article/pii/S1097276526001383
▌DOI:
https://doi.org/10.1016/j.molcel.2026.02.024

CellPress细胞出版社
原标题:《Mol Cell:泛素连接酶RNF25通过调控整合应激反应介导mRNA损伤耐受 | Cell Press论文速递》

