浙大一院联合匹兹堡大学基于跨种族遗传基因组学揭示主要精神疾病的共享生物学通路与风险机制
精神分裂症(SCZ)、双相障碍(BD)和重性抑郁障碍(MDD)是全球致残率极高的主要精神疾病,三者在临床症状和流行病学上表现出高度的共病性,提示它们可能共享潜在的遗传基础。然而,既往的大规模单一种族全基因组关联分析(GWAS)限制了遗传发现的普适性及跨种族生物学机制的解析。如何跨越种族差异,精准捕获三大精神疾病背后的“共享遗传易感性(Shared Genetic Liability)”,是精神病学遗传研究的前沿难题。
近日,浙江大学医学院附属第一医院胡少华教授团队与匹兹堡大学杨晟博士合作,在Molecular Psychiatry发表题为“Cross-ancestry genetic architecture reveals shared biological pathways of major psychiatric disorders”的研究论文。该研究提出了基于GWAS汇总数据的跨种族多组学整合分析框架,纳入目前规模最大的跨种族GWAS汇总数据、英国生物样本库(UKB)和浙大一院精神卫生中心BD队列的个体数据,系统解析了三种主要精神疾病的共享遗传结构,并结合单细胞多组学、脑影像因果推断及多基因风险评分(PRS),揭示了跨种族通用的神经发育通路与基因-环境交互作用。

一、 跨种族“共享遗传因子”识别
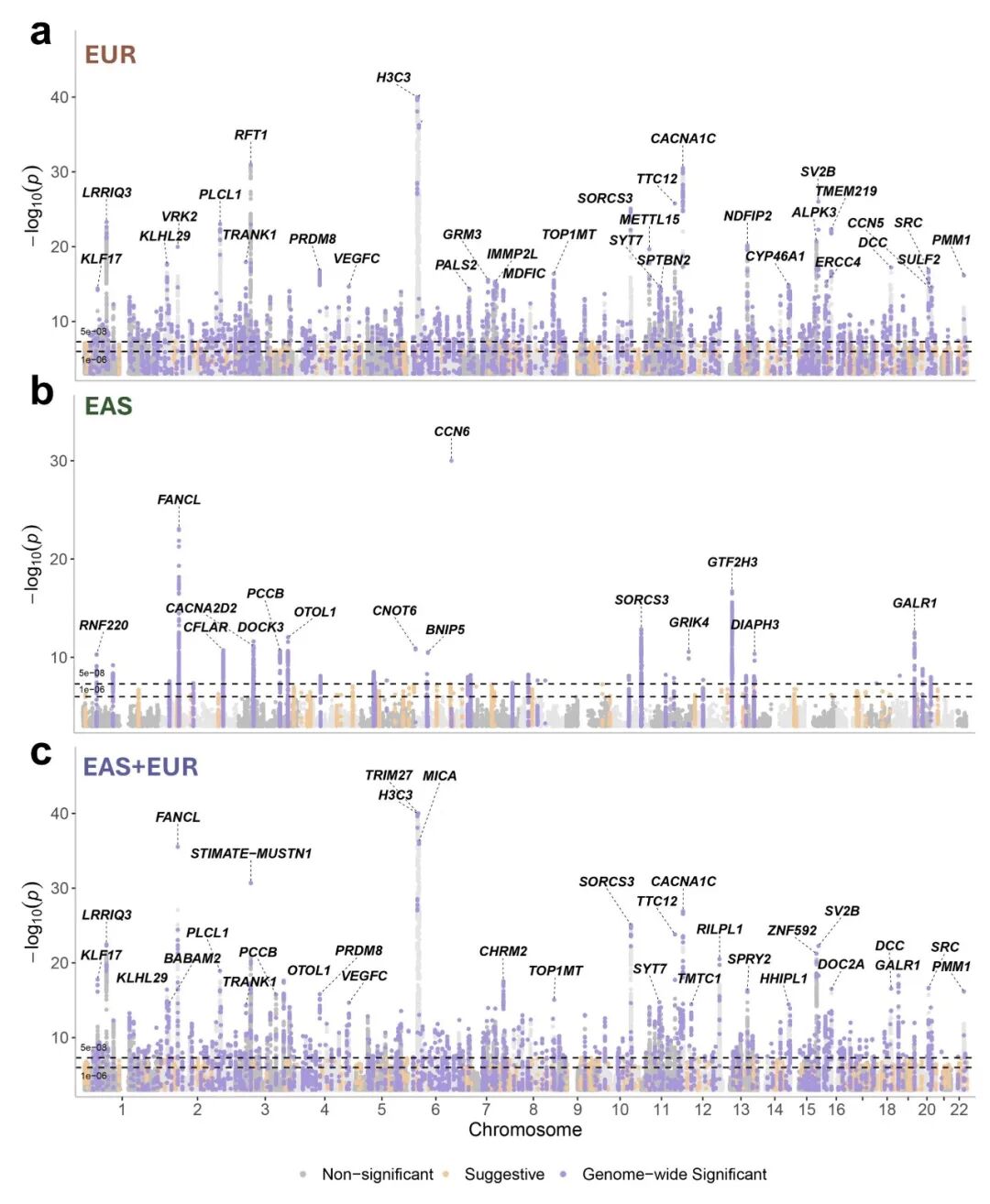
研究团队首先利用基因组结构方程模型(Genomic SEM),在欧洲(EUR)和东亚(EAS)人群中分别构建了潜在的“共享易感因子”。通过跨种族多变量GWAS荟萃分析,成功鉴定出403个与三种疾病共享易感性显著相关的基因座,其中88个为全新发现的位点。值得注意的是,研究发现位于VRK2基因的 rs7596038位点在两个种族中均表现出极强且方向一致的效应(EAS P=1.1×10⁻²³; EUR P=9.6×10⁻¹⁷),并通过MESuSiE精细定位被确认为高置信度的共享因果变异(PIP=1)。这一发现有力证明了精神疾病跨种族共享的生物学基础。
二、 “共享遗传因子”驱动的多组学整合
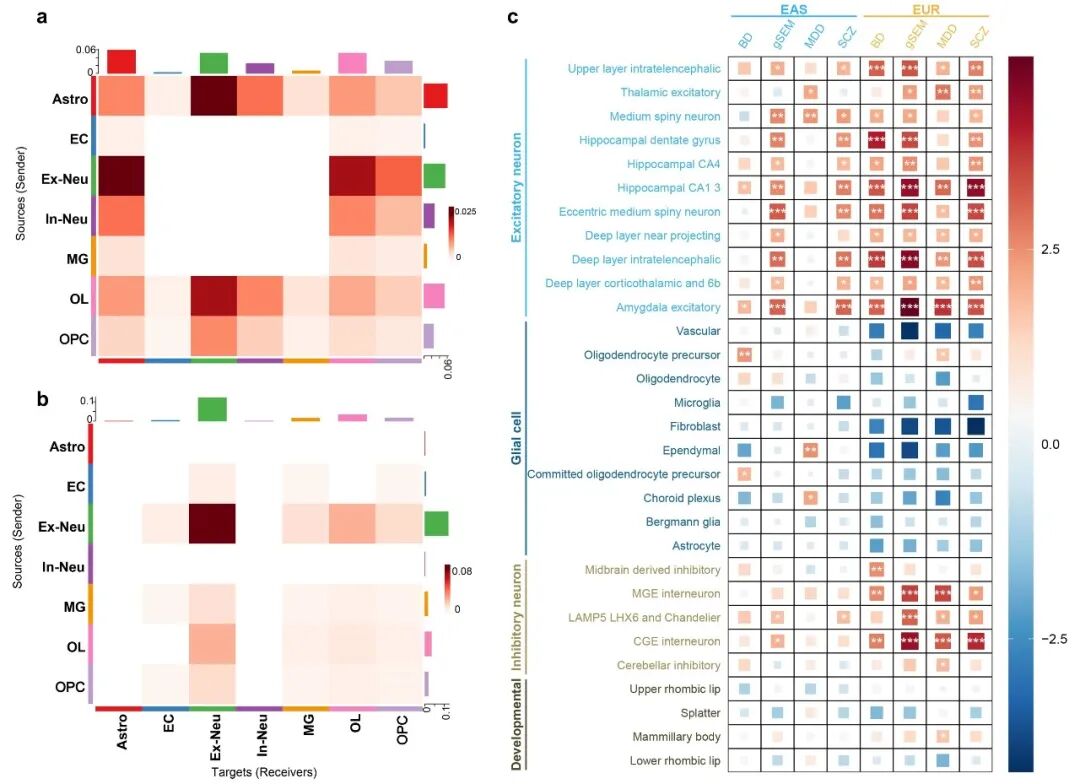
研究整合了位置映射、eQTL、TWAS、SMR及PsyOPS等多种策略,优先筛选出90个高置信度风险基因。功能富集分析显示,这些基因显著富集于神经系统发育、突触形成及环路重塑通路。进一步结合人脑眶额叶皮层单核RNA测序(snRNA-seq)数据,研究发现这些共享风险基因主要在兴奋性神经元和星形胶质细胞中富集。通过CellChat细胞通讯分析,研究揭示了NCAM1–FGFR1和NEGR1–NEGR1配体-受体轴是介导共享遗传风险的关键信号通路。这些通路在神经元与胶质细胞的通讯中异常活跃,可能通过调控突触可塑性和皮层发育,导致了跨诊断的脑环路功能障碍。
三、“共享遗传因子”和脑影像的因果效应
利用孟德尔随机化(MR)分析,研究团队量化了共享遗传易感性对脑结构的因果影响。结果显示,精神疾病的共享遗传风险会导致额叶、扣带回及海马旁回等关键脑区的灰质体积增加,同时破坏右侧矢状层和小脑中脚等白质纤维束的微结构完整性。这为理解精神疾病“认知-情感”双重受损的病理机制提供了影像学证据。
四、“共享遗传因子”的跨种族预测及其与环境交互作用
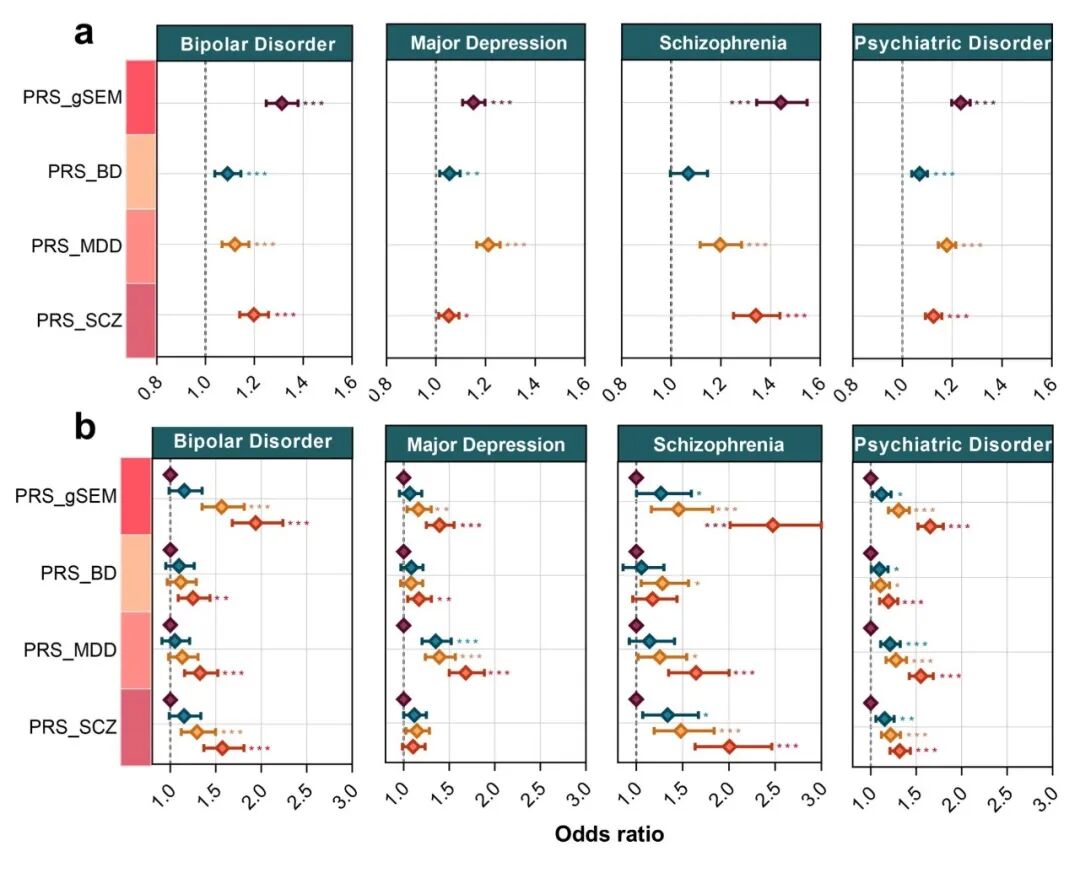
在风险预测层面,基于gSEM提取的共享遗传成分,使用DBSLMM构建的多基因风险评分,在独立队列中展现了优异的跨种族预测性能(Yang &Zhou, AJHG, 2020)。特别是在高风险个体识别上,PRS_gSEM对双相障碍和精神分裂症的预测效力显著优于传统的单病种PRS(Top 25%人群风险增加约2-2.5倍)。此外,研究还验证了经典的“素质-压力模型(Diathesis-Stress Model)”。结果发现,共享遗传易感性与童年创伤(如遭受身体暴力)存在显著的交互作用,即携带高遗传风险的个体在遭受创伤后,患病风险呈非线性指数级上升。
作者信息与资助
浙江大学医学院附属第一医院精神卫生中心胡少华教授与匹兹堡大学杨晟博士为本文共同通讯作者。
本研究得到国家自然科学基金项目(82571735、82173585)、国家重点研发计划项目(2023YFC2506200、2023YFC2506203)、浙江省重点研发计划项目等资助完成。研究得到了浙江省精神障碍精准诊疗重点实验室、脑机智能全国重点实验室、良渚实验室等平台的大力支持。
原标题:《【Nature 子刊】浙大一院联合匹兹堡大学基于跨种族遗传基因组学揭示主要精神疾病的共享生物学通路与风险机制》

