第四军医大学唐都医院常婷团队Med:双靶点CD19/BCMA CAR-T攻克难治性重症肌无力

医学Medicine
2026年2月25日,第四军医大学唐都医院常婷教授团队在Cell Press细胞出版社旗下医学旗舰期刊Med发表了题为“Single-cell profiling of immune reset in patients with refractory generalized myasthenia gravis receiving autologous CD19/BCMA CAR-T cell therapy”的研究论文。该研究创新性采用双靶点CD19/BCMA CAR-T细胞不清淋方案,用于治疗难治性全身型重症肌无力(myasthenia gravis,MG)患者,在临床应用中展现出显著的疗效与良好的安全性,可通过精准“免疫重置”,帮助患者重建健康的免疫系统;同时,研究团队利用单细胞测序等技术,对相关作用机制进行了深入解码与系统阐释。这一突破性成果,为神经免疫疾病的细胞治疗领域开辟了全新路径,也为该类难治性疾病的临床诊疗提供了重要新思路。
MG是一种主要由乙酰胆碱受体(acetylcholine receptor,AChR)抗体介导的神经系统自身免疫疾病,传统治疗主要依靠激素及非激素类免疫抑制剂,难以根治且副作用明显。如何实现疾病的长期缓解,甚至达到“无药生存”,是当前神经免疫治疗领域面临的重大挑战。
常婷教授团队创新性地采用双靶点CAR-T细胞,同时靶向B细胞成熟抗原(BCMA)和CD19,实现对B细胞的深度清除。研究人员对6例难治性全身型重症肌无力患者进行了治疗,并通过流式细胞术和单细胞测序技术,对治疗前后患者的外周血和骨髓样本进行了高精度的免疫全景分析。研究显示,CD19/BCMA CAR-T细胞的疗效显著且安全性良好:
无需清淋预处理:本研究创新性地采用了不含清淋预处理(化疗)的方案,患者不仅耐受性良好,且CAR-T细胞在体内仍能有效扩增并发挥作用,避免了清淋带来的感染和骨髓抑制风险。
临床症状快速改善:6例患者中有4例(66%)在第60天达到了最小症状表达(minimal symptom expression,MSE),即临床症状完全消失。所有患者的肌无力日常生活活动评分(MG-ADL)显著下降,且均成功停用激素。
致病性抗体水平显著降低:AChR或MuSK致病性抗体水平显著下降,高剂量组平均降幅超过80%,其中1例患者抗体转阴。
更重磅的发现来自对“免疫重置”机制的深度解析:该研究发现,CAR-T细胞治疗使重症肌无力患者实现了"免疫重置"——即外周血和骨髓B细胞实现有效清除,在治疗后90天外周血中部分B细胞亚群回升,以未成熟B细胞为主。团队进一步利用单细胞测序技术,在单细胞水平解析了治疗前后B细胞重建的免疫微环境及其动态演变,首次揭示了CD19/BCMA CAR-T细胞诱导免疫耐受的分子机制,为免疫重建提供了科学依据。
B细胞“重启”:治疗后新生的B细胞表现出高水平的抑制信号(如CD22通路激活),回归“低反应”的静息状态,有效防止其异常激活。
骨髓微环境重塑:CAR-T细胞进入骨髓后,增加骨髓基质细胞(间充质干细胞、内皮细胞等)表面抑制性自身免疫分子的表达(CD55),促进免疫稳态恢复。
该研究证实,双靶点CD19/BCMA CAR-T是针对难治性重症肌无力的一种极具前景的治疗策略。不仅能快速缓解病情、停用免疫抑制剂,还能通过重塑骨髓微环境实现长期的免疫系统“重置”。这些发现为下一代CAR-T细胞治疗产品的优化设计奠定了理论基础。目前,团队正推进更大规模的临床研究,以期让更多患者受益于这一创新疗法。
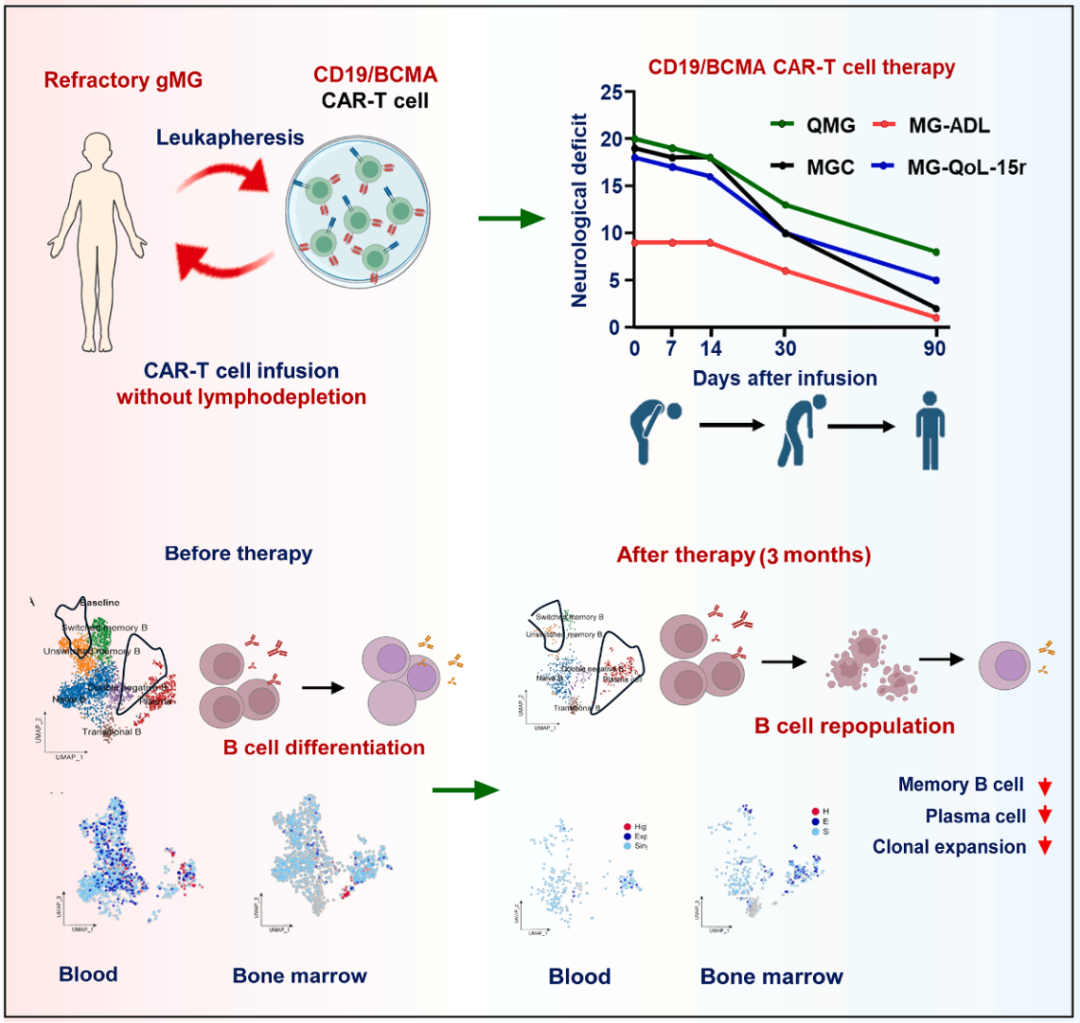
双靶点CD19/BCMA CAR-T细胞治疗后的“免疫重置”
第四军医大学唐都医院神经内科常婷教授为本文第一通讯作者(Lead contact),阮哲主治医师为本文的第一作者。天津医科大学总医院刘强教授、德国柏林夏里特医学院Friedemann Paul教授、中国科学院生物物理研究所李颖教授为本论文共同通讯作者。第四军医大学唐都医院神经内科宁凡医师、李爽博士,天津医科大学总医院神经内科张文彦博士为论文共同第一作者。

研究团队合影
作者专访
Cell Press细胞出版社特别邀请本文通讯作者团队进行了专访,请他们为大家进一步解读。
CellPress:
现有的CAR-T疗法大多针对单一靶点(如仅CD19或仅BCMA),贵团队为什么要选择“双靶点”策略?这在治疗重症肌无力中有何独特优势?
常婷教授团队:
这是一个非常关键的问题。重症肌无力的致病机制较为复杂,成熟B细胞及骨髓中的长寿命浆细胞均可产生致病性抗体。 单一靶点往往存在“漏网之鱼”:仅靶向CD19,无法彻底清除骨髓长寿浆细胞;仅靶向BCMA,虽可清除浆细胞,但无法有效清除自身反应性B细胞。我们选择CD19和BCMA双靶点,就是为了覆盖B细胞发育的全生命周期,实现更彻底的“深层清除”,从源头上阻断致病性抗体的产生,降低复发风险,实现疾病的长期缓解。
CellPress:
研究中提到的“无需清淋预处理”是一个非常大的亮点,这对临床应用意味着什么?安全性如何?
常婷教授团队:
既往的CAR-T细胞治疗通常需要在细胞回输前进行强力清淋预处理,这会带来感染、脱发、骨髓抑制等严重副作用。对于重症肌无力这类非肿瘤患者,我们对安全性的要求极高。我们的研究结果显示,即使不进行清淋预处理,双靶点CAR-T细胞在体内依然扩增良好,且疗效显著。在安全性方面,6例患者均未出现严重的细胞因子释放综合征(CRS)或神经毒性,仅出现一过性发热。这意味着我们将CAR-T疗法的“门槛”大大降低了,患者更容易接受,未来甚至有望在门诊层面进行推广,极大地提高了治疗的可及性。
CellPress:
研究利用单细胞测序技术发现治疗后的“骨髓微环境重塑”,这一发现有何科学价值?
常婷教授团队:
这是本研究机制探索中最令人兴奋的部分。以往我们认为CAR-T只是“杀手”,把致病细胞杀光就行了。但我们的单细胞测序数据揭示,CAR-T还是“教官”,它教育了骨髓这个“大本营”。 我们发现,治疗后骨髓中的基质细胞发生了改变,它们开始分泌抑制自身免疫的信号,并引导造血干细胞向正常的淋巴细胞方向分化。这解释了为什么患者在停药后依然能维持缓解——因为整个免疫系统生态环境被“重置”了。这一发现不仅加深了我们对CAR-T治疗原理的理解,也为未来通过调节微环境来治疗自身免疫病提供了新思路。

作者介绍
常婷
教授
常婷,第四军医大学唐都医院神经内科主任医师、教授、博士(后)导师,神经内科副主任。国家科技重大专项首席专家、陕西中青年科技创新领军人才、陕西省科技创新团队带头人。主持国家科技重大专项1项、国家重点研发计划课题1项、国家自然科学基金4项、国家重大疑难疾病中西医临床协作项目1项。近5年以第一/通讯作者在Cell、Science Translational Medicine、Med、Journal of Neuroinflammation等期刊发表SCI论文34篇;执笔国家级指南2部;授权国家发明专利及软著10项;副主编、参编专著7部;国家神经系统疾病临床研究中心重症肌无力注册登记研究Co-PI以及执行PI,发起全国多中心临床研究23项,承接国际/国内多中心药物临床试验16项。以第一及主要完成人获陕西省高校优秀成果特等奖、省部级一等奖、陕西省创新创业大赛一等奖;荣立“国防科技三等功”1次,“三级表彰”1次,享受军队优秀专业技术人才二类岗位津贴。
相关论文信息
论文原文刊载于Cell Press细胞出版社旗下期刊Med
▌论文标题:
Single-cell profiling of immune reset in patients with refractory generalized myasthenia gravis receiving autologous CD19/BCMA CAR-T cell therapy
▌论文网址:
https://www.sciencedirect.com/science/article/abs/pii/S2666634026000292
▌DOI:
https://doi.org/10.1016/j.medj.2026.101026
原标题:《第四军医大学唐都医院常婷团队Med:双靶点CD19/BCMA CAR-T攻克难治性重症肌无力:解码免疫“一键重启” | Cell Press对话科学家》

