急性缺血性卒中影像学诊断的现状与进展
大家好,欢迎大家访问XI区!
急性缺血性卒中(AIS)作为全球范围内导致残疾和死亡的主要原因之一,给公共卫生领域带来了沉重负担。神经影像学在急性缺血性卒中的诊断、治疗管理和预后评估中发挥着关键作用,其核心目标是筛选出适合再灌注治疗(包括溶栓和取栓)的患者,为临床决策提供精准依据。近年来,影像学技术不断发展,在识别大血管闭塞(LVO)、界定可挽救组织范围以及指导急性治疗干预等方面的能力持续提升。本文将系统综述急性缺血性卒中评估中常用的神经影像学方法,重点阐述其实际应用、最新进展及局限性,为临床实践提供参考。
急性缺血性卒中影像学检查核心要点总结表
| 影像学检查方法 | 核心优势 | 主要应用场景 | 关键局限性 | 最新进展 |
| CT平扫(NCCT) | 快速便捷、可及性高、无对比剂风险,能快速排除出血 | 急性卒中初始筛查、溶栓资格评估、计算 ASPECT评分 | 对超早期梗死(<3h)敏感性低,后颅窝梗死检出率差(41.8%),存在 “CT 迷雾现象” | 自动化ASPECTS评分系统提升一致性;基于CT净摄水率实现 “MRI 级” 梗死识别精度 |
| 双能计算机断层扫描(DECT) | 区分对比剂染色与出血,提高早期缺血改变检出率 | 血管内干预后出血鉴别、急性缺血性卒中精细评估 | 设备普及率较低,检查成本高于常规CT | 衍生虚拟平扫CT (VNCCT),可单次扫描完成血管 + 实质评估 |
| 计算机断层扫描血管造影(CTA) | 快速识别大血管闭塞(LVO),清晰显示颅内外血管解剖 | 卒中初始 “一站式” 评估、取栓患者筛选、血管病变诊断(狭窄/夹层/动脉瘤) | 对中等血管闭塞(MeVO)敏感性较低(65%),可能出现假性闭塞,有辐射和对比剂风险 | 自动化LVO检测系统(敏感性 96%/ 特异性 98%)、多期相CTA评估侧支循环、能谱CT区分梗死核心与半暗带 |
| 计算机断层扫描灌注(CTP) | 量化评估脑灌注(CBF/CBV/MTT/Tmax),界定梗死核心与半暗带 | 扩大再灌注治疗窗口、筛选可挽救组织患者、预测出血转化风险 | 软件算法差异导致结果变异性大,可能高估梗死核心或半暗带 | Tmax阈值(>6s)标准化应用;与AI结合提升灌注参数计算效率 |
| 磁共振成像(MRI) | 高敏感性检测早期缺血(DWI序列),排除卒中模拟病变 | 醒后卒中评估、发病时间不明卒中、小梗死灶检出 | 检查时间长、可及性有限,体内有金属异物者禁忌 | 6分钟快速卒中协议;AI 驱动图像重建实现超快速MRI |
| 磁共振血管造影(MRA) | 无辐射、无对比剂(TOF-MRA),评估血管狭窄/闭塞 | 无法耐受CTA的患者、血管病变随访 | 飞行时间MRA可能高估狭窄程度,难以区分近全闭塞与完全闭塞 | 对比增强MRA提升闭塞检出率;血管壁MRA(VW-MRA)明确狭窄病因 |
| 数字减影血管造影(DSA) | 血管评估 “金标准”,高空间/时间分辨率 | 血管内干预术中指导、复杂血管病变诊断(如血管炎) | 侵入性操作,有辐射/对比剂风险,需专业技术 | 术中实时评估血管再通(TICI评分),非目标血管病变检出 |
| 经颅多普勒超声(TCD) | 无创、实时监测,成本低 | 床旁血流动力学监测、LVO快速筛查、超声溶栓辅助治疗 | 结果依赖操作者,颅骨厚度影响检测成功率 | 用于超声溶栓增强溶栓效果;实时监测取栓后血管再通情况 |
注:ASPECTS = 阿尔伯塔卒中项目早期 CT 评分;CBF = 脑血流量;CBV = 脑血容量;MTT = 平均通过时间;DWI = 弥散加权成像;TOF-MRA = 时间飞跃法磁共振血管造影;LVO = 大血管闭塞;MeVO = 中等血管闭塞;TICI = 脑梗死溶栓分级。
常用影像学检查方法及应用
CT平扫(NCCT)
CT平扫自20世纪80年代问世以来,一直是急性缺血性卒中初始评估的基石。其广泛的可及性、安全性和快速执行能力,使其成为急性缺血性卒中紧急处理中不可或缺的工具。该检查的核心初始目标是排除出血并判断患者是否适合溶栓治疗,同时还能快速排除其他导致急性神经症状的病因。
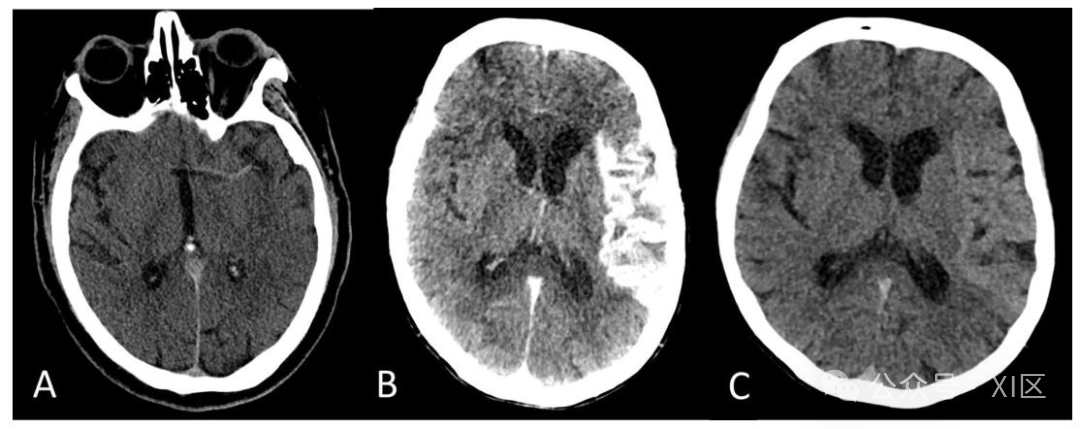
头颅CT平扫与双能头颅CT平扫图像对比
A 图为头颅CT扫描,显示左侧大脑中动脉(MCA)预期位置出现线性高密度影,符合急性血栓形成表现,即 “大脑中动脉高密度征”。B 图为左侧大脑中动脉供血区卒中患者血管内干预后的双能头颅CT平扫图像:左侧混合能量图像显示左侧岛叶及左侧颞 - 额 - 顶叶皮质出现脑回样明显高密度影;右侧虚拟平扫图像显示左侧大脑中动脉供血区轻度高密度影及灰白质分界消失,提示血脑屏障破坏、新生血管形成及自主调节功能受损,未见出血转化。
在早期缺血征象识别方面,CT平扫可发现大脑中动脉高密度征(HMCAS),表现为大脑中动脉近端密度增高,常与M1段血栓形成相关,对检测大血管闭塞的敏感性为67%,特异性为82%。此外,基底动脉、颈内动脉等也可能出现高密度征,其中基底动脉高密度征对于诊断临床表现不典型的基底动脉闭塞至关重要。岛叶皮质带消失征是由于早期细胞毒性水肿导致岛叶皮质外侧缘灰白质分界消失,常与大面积梗死和不良预后相关;基底节区早期缺血改变表现为豆状核模糊,对深部皮质下梗死的敏感性为48%;皮质梗死可通过脑沟变浅识别,敏感性为69%,同样与不良预后相关。在超急性期(6-24小时),通过调整窗宽和窗位的“卒中窗”设置,CT平扫能更清晰地检测到灰白质分界消失。
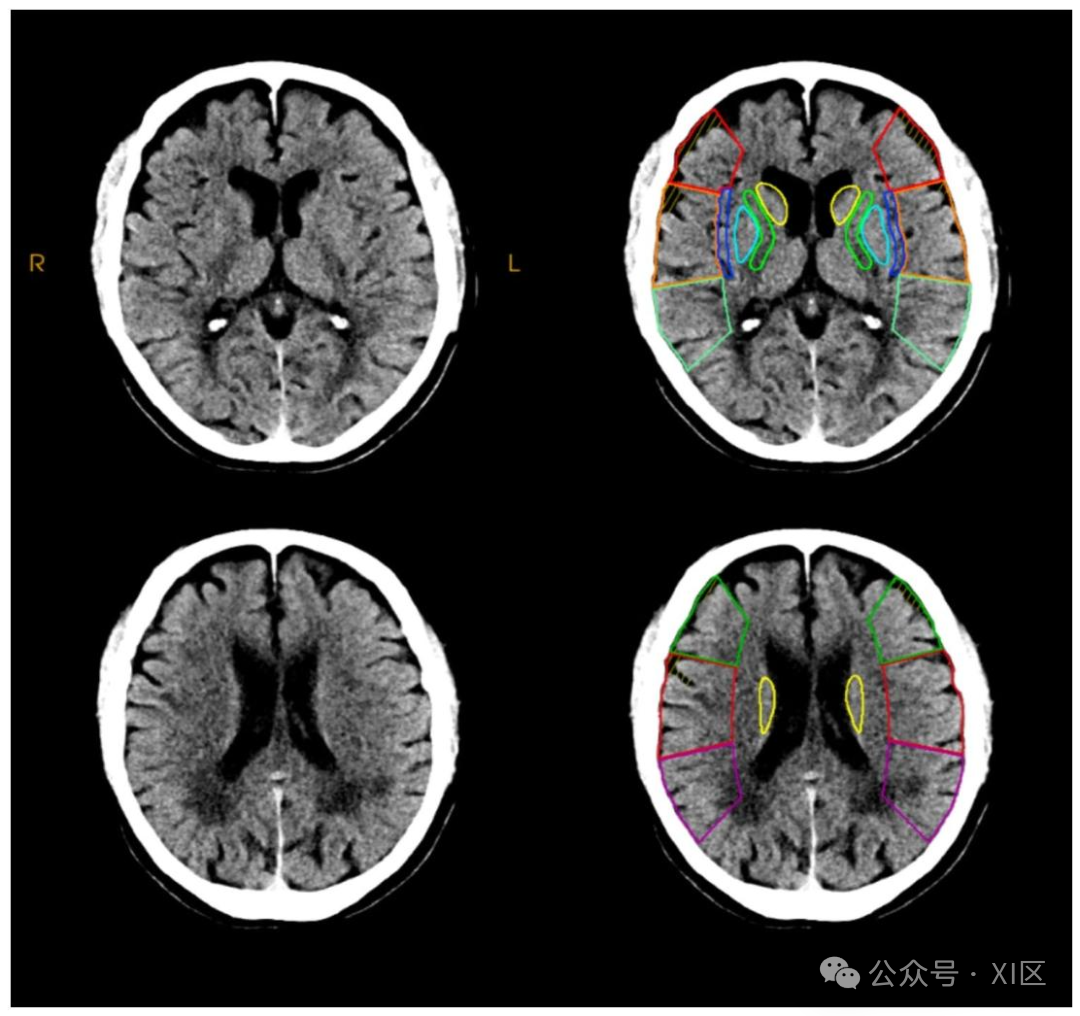
头颅CT扫描所示阿尔伯塔卒中项目早期 CT 评分(ASPECTS)示意图
该图为头颅CT扫描图像,展示了ASPECTS评估区域。该评分系统基于大脑中动脉供血区 10 个关键区域,通过判断各区域是否存在缺血损伤进行计分,为急性卒中干预决策提供重要参考。
阿尔伯塔卒中项目早期CT评分(ASPECTS)是基于CT平扫的关键评估工具,通过对大脑中动脉供血区10个区域进行评分,正常区域计1分,缺血受损区域计0分,评分越低提示预后越差、脑损伤范围越大,可为溶栓或取栓治疗决策提供重要参考。此外,CT平扫还能及时发现恶性脑水肿和占位效应的早期迹象,如脑沟、侧脑室受压或中线移位。
然而,CT平扫也存在局限性。发病3小时内的大面积皮质梗死可能无法被检测到,约40%的梗死在24小时内仍可能被遗漏,仅依靠该检查难以准确判断梗死年龄。由于脑干和小脑区域骨性结构密集、解剖复杂,易产生伪影,CT平扫对后颅窝梗死的敏感性仅为41.8%。阿尔伯塔卒中项目早期CT评分的计算存在观察者间差异,影响其可靠性,目前自动化评分系统的应用正逐步提高其一致性。此外,缺血性卒中后2-3周可能出现“CT迷雾现象”,即初始显示的低密度梗死灶变为等密度或不可见,若未被识别可能低估梗死范围。
双能计算机断层扫描(DECT)
双能计算机断层扫描通过两种不同能量的X射线获取数据,能够区分X射线衰减相似的组织,如对比剂与出血,这在患者接受血管内卒中干预后等已注射碘对比剂的场景中尤为关键,可有效鉴别血脑屏障破坏导致的对比剂染色与出血。同时,该技术还能提高急性缺血性卒中早期缺血改变的检出率。
虚拟CT平扫(VNCCT)是基于双能CTA重建得到的图像,可通过单次扫描同时完成血管和实质评估,优化急性缺血性卒中影像学检查流程。研究表明,虚拟CT平扫不劣于传统CT平扫,但目前指南仍推荐传统CT平扫作为初始影像学检查方法。
计算机断层扫描血管造影(CTA)
头颈部CTA凭借快速采集、高可及性和对大血管闭塞的高识别精度,已成为“卒中协议”成像的标准组成部分,为急性卒中干预提供指导。在DAWN试验和DEFUSE 3试验扩展血管内取栓(EVT)时间窗后,“全民CTA”协议在许多机构成为标准。该检查对前循环大血管闭塞的敏感性和特异性分别约为91%和93%,对所有大血管闭塞的敏感性和特异性分别为73%和92%,对中等血管闭塞(MeVO)的敏感性和特异性约为65%和93%。
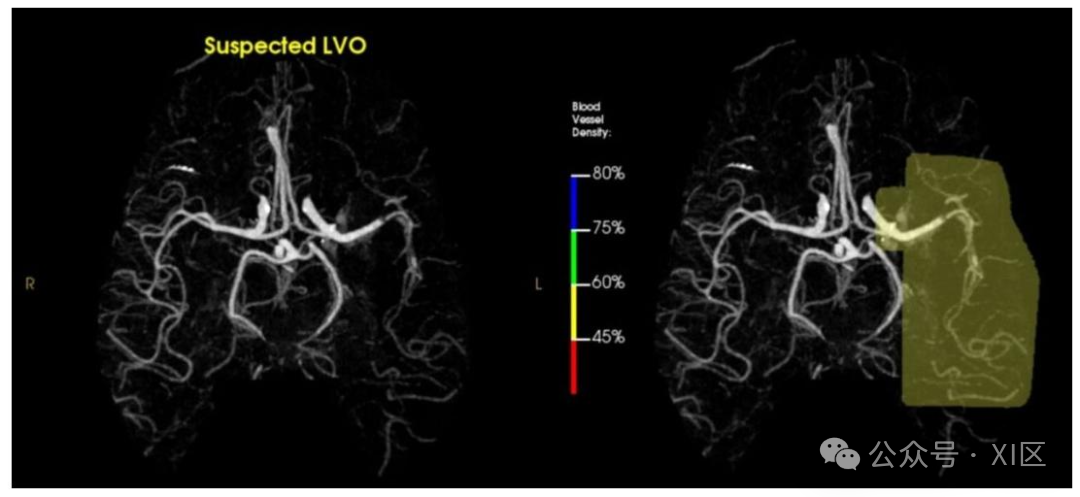
颅内CT扫描血管造影(CTA)三维重建图像
图中为颅内CTA的三维重建图像,展示了 RAPID 软件对大血管闭塞的检测结果。该技术能清晰显示颅内血管解剖结构,快速识别血管闭塞部位,为急性缺血性卒中的血管内干预提供精准指导。
CTA能清晰显示颅内外动脉循环的血管细节,有助于诊断与急性缺血性卒中相关的多种血管病变,如动脉夹层、狭窄、动脉瘤等,还可识别颅内外循环的解剖变异。尽管数字减影血管造影(DSA)被视为评估卒中血管的金标准,但研究表明,CTA检测颅内大动脉50%以上狭窄的敏感性为97.1%,特异性为99.5%,在颅内狭窄和闭塞的检测上优于磁共振血管造影(MRA),且对颅外颈动脉狭窄的筛查敏感性高。
近年来,CTA技术不断进步。自动化检测系统可快速可靠地检测大血管闭塞,特异性达98%,敏感性达96%,部分高性能系统的图像处理平均时间仅为3分18秒;基于深度学习的算法能提供聚焦视图,加速大血管闭塞检测;多期相CTA(mCTA)通过捕捉多个增强时相,改善了大血管闭塞检测和侧支循环评估,结合时变彩色图可更易评估侧支循环和远端闭塞。此外,基于CTA源图像计算的ASPECTS(CTA-ASPECTS)在预测最终梗死面积和临床结局方面优于基于CT平扫的ASPECTS,能更清晰地显示侧支循环程度和梗死范围。
CTA的局限性包括:严重颅内闭塞患者的动脉期扫描可能导致颈总动脉等近端颈动脉出现假性闭塞现象,多期相CTA可通过捕捉多个增强时相加以鉴别;对远端颅内闭塞或中等血管闭塞的评估能力有限;为获取详细图像而采用薄切片扫描时,辐射暴露问题较为突出;尽管近年证据表明对比剂诱导肾病的风险低于以往认知,但仍需警惕。
磁共振成像(MRI)
磁共振成像凭借多种序列优势,在排除卒中模仿病变、检测急性缺血性卒中以及判断发病时间和严重程度方面具有优越性。6分钟磁共振卒中协议已被证实具有可行性,包括弥散加权成像(DWI)、表观弥散系数(ADC)图、液体衰减反转恢复(FLAIR)序列、梯度回波(GRE)序列、磁共振血管造影(MRA)和灌注磁共振成像(MRP)。通过弥散加权成像和灌注加权成像(PWI)界定存活组织,磁共振成像还能将再灌注治疗窗口从传统的时间窗口扩展至组织窗口,尤其适用于醒后卒中或发病时间不明确的病例。
在急性缺血性卒中的磁共振成像时间演变方面,超急性期(数分钟内),由于细胞毒性水肿限制水分子扩散,弥散加权成像开始出现高信号,表观弥散系数图呈低信号;磁敏感加权成像(SWI)上的磁敏感血管征以及T2/FLAIR序列上因血流停滞或缓慢导致的流空信号消失、高信号也是超急性期的重要表现,其中磁敏感血管征明显提示侧支循环不良和功能预后不佳。进入晚超急性期(6小时后),T2高信号逐渐出现并持续数日,T1低信号通常在发病16小时后显现。急性缺血性卒中的T1对比增强可分为血管内增强和实质增强,前者多在发病24-48小时内出现,最早可在卒中后1小时出现,持续约1周,与血管内血流缓慢或停滞相关;后者由血脑屏障破坏导致,可在卒中后持续数周。
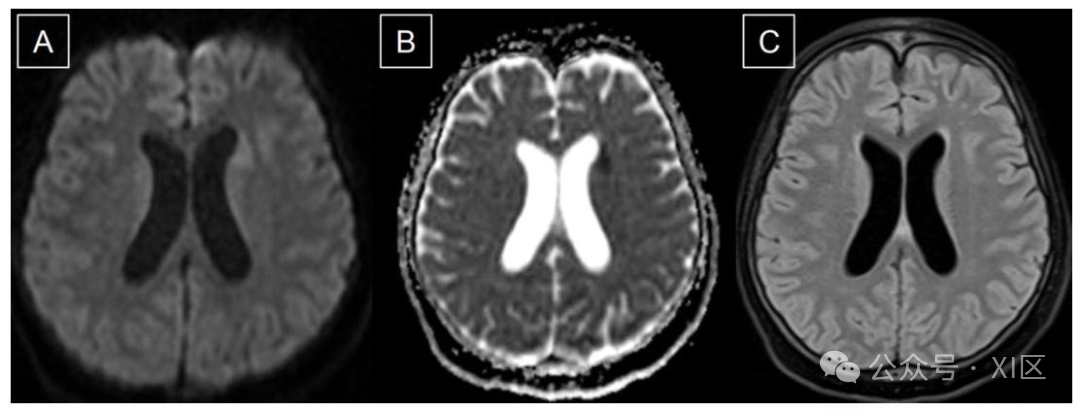
脑部弥散加权磁共振(MR)成像及相关序列对比
A 图为脑部弥散加权磁共振成像,显示左侧脑室前旁白质存在小范围高信号区;B 图为对应的表观弥散系数(ADC)图,该高信号区呈低信号,符合急性梗死表现;C 图为液体衰减反转恢复(FLAIR)序列图像,该急性梗死灶未显示明显信号改变。
请在微信客户端打开
多项研究表明,基于磁共振成像的ASPECTS(MRI-ASPECTS)或基于弥散加权成像ASPECTS(DWI-ASPECTS)的观察者间一致性高于基于计算机断层扫描 ASPECTS(CT-ASPECTS),且在预测功能结局和梗死体积方面更具优势。
磁共振成像在急性缺血性卒中应用中的局限性主要体现在可及性和检查时间上。研究表明,使用磁共振成像评估的急性缺血性卒中患者溶栓率较低,门到针时间延长,但对取栓相关结局无显著影响。体内有金属装置或异物的患者无法进行磁共振成像检查。此外,24小时全天候提供磁共振成像服务的医疗机构有限,改善其可及性有助于减少住院时间和住院率。
值得注意的是,磁共振成像阴性卒中(或称弥散加权成像阴性卒中)是临床中需要关注的现象,这类患者通常功能结局更好,残疾或死亡风险更低,但需结合临床判断进行诊断。系统综述显示,约16%的卒中患者为磁共振成像阴性卒中,另一项研究估计其患病率约为6.8%,在后循环受累和轻型卒中(NIHSS评分≤5分)中更为常见。在干预后表现方面,血管内取栓后,磁共振成像可能发现脑沟局灶性蛛网膜下腔出血,这是由于再灌注损伤和皮质小血管破裂导致,在CT平扫上也可能显现,属于良性表现,甚至可能提示预后良好。
CT灌注(CTP)与磁共振灌注(MRP)
CT灌注和磁共振灌注均为功能成像方法,用于评估可挽救脑组织,区分半暗带与梗死核心。计算机断层扫描灌注因可及性高、采集快速,正逐渐成为“卒中协议”计算机断层扫描的组成部分,将其纳入卒中检查流程可提高大血管闭塞检出率和取栓率。该检查通过在对比剂团注期间对单一位置进行连续成像,经自动化软件处理生成彩色编码图,主要提供脑血流量(CBF)、脑血容量(CBV)和平均通过时间(MTT)等参数。其中,脑血容量指单位脑组织内的血液体积,脑血流量指单位时间内通过单位脑组织区域的血液体积,平均通过时间指血液通过单位脑组织的平均时间。
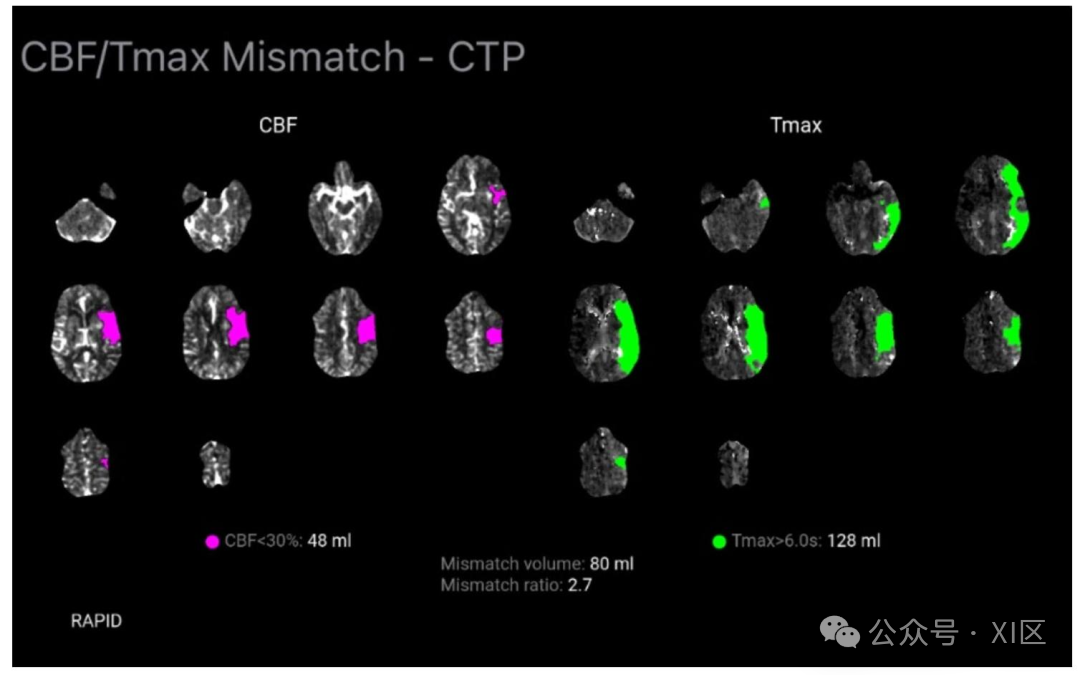
脑部计算机断层扫描灌注(CTP)图像
该图为左侧大脑中动脉梗死患者的脑部计算机断层扫描灌注图像,显示存在明显的不匹配体积。左图中,脑血流量(CBF)低于 30% 的区域以紫色标注,体积为 48 毫升;右图中,Tmax大于 6.0 秒的区域以绿色标注,体积为 128 毫升。不匹配体积为 80 毫升,提示存在大量可挽救的脑组织,适合进行血管内干预。
Tmax是对比剂团注到达大动脉至脑组织内浓度达峰的时间延迟(秒),是评估灌注延迟的敏感指标,可有效识别缺血半暗带,即使是经验不足的观察者也能轻松解读,诊断准确性高,适用于急性缺血性卒中的评估与管理。此外,Tmax还可用于筛选适合血管内干预的远端中等血管闭塞患者,并能预测溶栓后出血转化风险,Tmax>14秒提示出血风险升高。研究证实,以Tmax>6秒作为阈值,对识别半暗带具有高敏感性和特异性。总体而言,半暗带表现为Tmax/MTT延长、CBF降低、CBV量正常或增加;而梗死核心表现为Tmax/MTT延长,且CBF和CBV显著降低。
磁共振灌注的常规方法为动态磁敏感对比(DSC),可提供与计算机断层扫描灌注相同的血流动力学参数;动脉自旋标记(ASL)是另一种磁共振灌注技术,无需使用对比剂即可获取灌注参数,具有独特优势。与计算机断层扫描灌注相比,磁共振灌注的图像分辨率更高,尤其在脑干和小脑区域,且无电离辐射,但可及性更低,获取难度更大。
灌注成像在急性缺血性卒中应用中存在诸多局限性。首先,计算机断层扫描灌注的使用存在显著变异性,不同卒中中心的缺血范围评估差异较大,这主要源于灌注厂商软件算法的不同,而非采集方法的差异,未来需重点推进灌注软件算法的统一和标准化。其次,梗死核心高估(即“假性梗死核心”)现象在急性缺血性卒中中较为常见,可能导致患者被不恰当地排除在再灌注治疗之外;达峰时间和平均通过时间有时会高估半暗带范围,因无法区分缺血和低灌注区域,可能引发不必要的干预。此外,心输出量低导致全脑低灌注的患者,或癫痫发作后出现卒中样表现的患者,其灌注成像结果难以解读。
磁共振血管造影(MRA)
磁共振血管造影和CTA均可提供颅内外血管的关键信息,用于急性缺血性卒中的评估与管理。尽管CTA常作为急性缺血性卒中初始评估的首选,但在具备条件的情况下,磁共振血管造影可纳入“急性卒中磁共振协议”。其主要优势在于能与其他磁共振序列结合,在评估小梗死体积的急性缺血性卒中时,可提供比计算机断层扫描更丰富的数据。
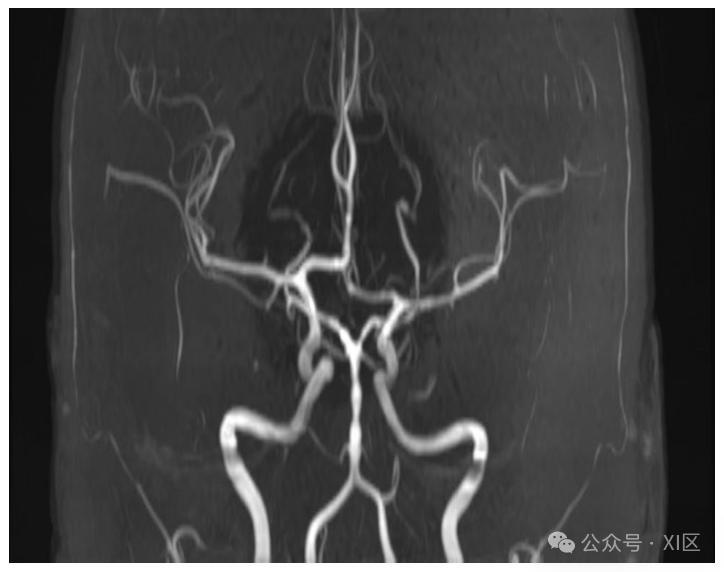
颅内磁共振血管造影(MRA)三维重建图像
图为结核性基底膜炎患者的颅内MRA三维重建图像。可见基底动脉存在多灶性狭窄和形态不规则,符合继发性基底动脉血管炎表现。该检查能清晰显示颅内血管病变特征,为病因诊断提供重要依据。
在磁共振血管造影技术中,时间飞跃法磁共振血管造影(TOF-MRA)适用于快速无对比剂血管评估或筛查;对比增强磁共振血管造影在识别血管闭塞和评估侧支循环方面优于飞行时间磁共振血管造影;动态磁共振血管造影(dMRA)对侧支循环的评估效果也优于飞行时间磁共振血管造影,且在检测不完全闭塞和血栓内前向血流方面更具优势。血管壁磁共振血管造影(VW-MRA)具有高空间和对比分辨率,采用快速自旋回波序列抑制血流信号,清晰显示动脉管壁,能详细识别斑块特征以评估其易损性,可用于判断狭窄病因(如动脉粥样硬化、血管炎、夹层等),在不明原因栓塞性卒中和隐源性卒中的病因探究中具有重要价值,有研究显示其能明确55%急性缺血性卒中患者的病因;对于疑似原发性中枢神经系统血管炎的病例,血管壁磁共振血管造影显示的同心性管壁增厚和对比增强具有重要诊断价值,敏感性为95.2%,特异性为68.8%-75%。
磁共振血管造影的局限性主要体现在飞行时间磁共振血管造影可能高估狭窄程度,导致急性缺血性卒中管理决策不当;仅依靠磁共振血管造影难以区分近全闭塞和完全闭塞。
数字减影血管造影(DSA)
数字减影血管造影通过减去造影前图像与造影后图像来增强血管可视化效果,凭借其高空间和时间分辨率,仍是诊断多种血管病变的金标准。在急性缺血性卒中中,数字减影血管造影的治疗价值不可或缺,能精准识别闭塞位置,为血管内干预提供指导,其检测大血管闭塞的阳性预测值和阴性预测值分别达91.1%和95.1%。血管内干预后,数字减影血管造影可评估血管再通程度(即脑梗死溶栓分级,TICI评分)。此外,血管内干预后对非目标血管的数字减影血管造影检查,可在4.4%的病例中发现先前未知的病变,并在3.3%的病例中改变治疗方案;该检查还能详细评估侧支循环,对预测基底动脉狭窄患者的长期结局有重要帮助。
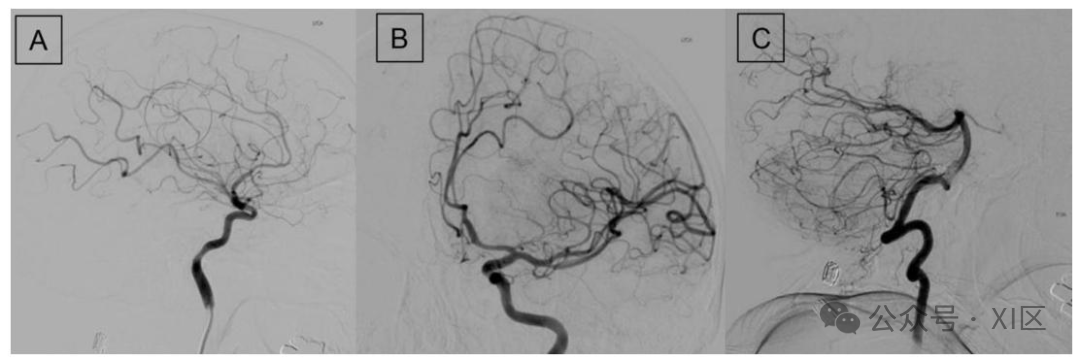
数字减影血管造影(DSA)图像
图为可逆性脑血管收缩综合征(RCVS)患者的数字减影血管造影图像。可见颅内动脉呈多灶性节段性狭窄与扩张交替出现,呈现 “串珠样” 表现,是该疾病的典型血管影像学特征。
数字减影血管造影的局限性在于其侵入性、对专业技术的需求、对比剂和辐射暴露以及有限的可及性,这些因素限制了其在急性缺血性卒中中的常规应用。
经颅多普勒超声(TCD)
经颅多普勒超声是一种廉价、无创、实时的血流动力学监测技术,具有广泛的临床和研究应用价值。其工作原理是利用超声探头发射超声波,穿透颅骨后被颅内血管内流动的血细胞反射,通过检测发射波与反射波之间的频率差异(多普勒频移)来评估血流速度。血管狭窄时,血流速度会升高以维持血流量,这一变化可被经颅多普勒超声检测到;该技术还能提供平均血流速度、收缩期峰值速度、舒张末期速度和脉动指数等参数,支持实时监测。
系统综述表明,经颅多普勒超声在急性场景下检测大血管闭塞的准确性较高,敏感性达85.9%,特异性达99.2%,在其他影像学方法不可及时可发挥重要作用。此外,经颅多普勒超声还是血管内干预后监测患者的经济有效工具,可及时发现血管再闭塞、栓塞或过度灌注等情况。与其他超声检查类似,经颅多普勒超声的结果依赖操作者的经验和技术,需要专业培训以提高检测效果。
经颅多普勒超声还具有潜在的治疗作用,超声溶栓是利用超声波的机械压力波使血栓表面暴露于循环中的溶栓药物,理论上可增强溶栓效果。多项随机对照试验和荟萃分析表明,与单纯溶栓相比,超声溶栓能使完全再通的概率翻倍,改善大脑中动脉闭塞患者的临床结局,且在67岁以下患者中效果更为显著。经颅多普勒超声是目前最常用的超声溶栓手段,有望成为急性缺血性卒中干预的辅助治疗方法,但其治疗价值仍需大规模试验进一步证实。
临床实践考量与新兴趋势
决策制定与临床背景
在日常临床实践中,需关注图像采集协议和参数等技术变量,优化图像质量的同时尽量缩短扫描时间对急性卒中评估至关重要。不同机构间的采集协议差异可能影响诊断准确性和速度,因此需标准化成像协议,包括层厚、对比剂注射时机和扫描范围等,以获得一致可靠的结果。高效的神经影像学工作流程是为卒中患者提供及时治疗的关键,将影像学与远程卒中系统、自动化分诊协议等快速决策平台相结合,可通过加速诊断和治疗启动来改善患者结局。例如,RAPID、Viz.AI等自动化图像处理工具能快速识别缺血组织和大血管闭塞,优化取栓患者筛选流程。
了解神经影像学的技术局限性对于避免误判至关重要。例如,计算机断层扫描灌注中,图像质量不佳或运动伪影可能导致缺血半暗带测量不准确;急性缺血性病变在梗死后期可能出现假性正常化,可能对组织存活能力得出误导性结论。神经影像学结果必须结合患者的临床表现进行解读,临床症状、美国国立卫生研究院卒中量表(NIHSS)评分和发病至成像时间等因素,均对影像学解读和治疗决策有重要指导意义,过度依赖影像学而忽视临床背景可能导致治疗不当。
直接血管造影室路径(DTAS)模式
为优化大血管闭塞患者的工作流程并加快血管内取栓速度,直接血管造影室路径模式被提出并开展研究。该模式绕过传统成像流程,直接将患者转运至血管造影室进行干预。多项荟萃分析表明,与传统方法相比,直接血管造影室路径能显著缩短门到再灌注时间,平均缩短约35分钟。现有证据显示,直接血管造影室路径是治疗急性缺血性卒中合并大血管闭塞的安全、经济、可行的方案。但该模式可能导致无大血管闭塞的患者接受不必要的动脉穿刺,且目前的协议存在显著异质性,其在大血管闭塞治疗中的具体定位和指南地位仍需正在进行的多中心试验进一步明确。
成人与儿童卒中的影像学差异
成人缺血性卒中的常见病因包括动脉粥样硬化、栓塞和大血管闭塞,而儿童卒中的病因多为血管炎、先天性心脏病或镰状细胞病等,这些病因在影像学上呈现独特特征,如血管炎表现为特征性的血管壁增厚,可通过血管壁成像(VWI)评估。儿童卒中的影像学检查面临诸多挑战,包括难以对不合作的儿童进行高质量成像、标准血管造影技术难以清晰显示细小血管、许多病例需要镇静等;此外,儿童卒中的病因更为多样,需要针对性的神经影像学方案来明确潜在病理机制。尽管磁共振成像(尤其是弥散加权成像)因对缺血性改变的高敏感性而成为儿童卒中的金标准,但由于辐射暴露风险,计算机断层扫描在儿童中的应用通常受到限制,仅在紧急情况下可使用CTA评估大血管闭塞。
未来进展与展望
急性缺血性卒中影像学技术正快速发展。基于计算机断层扫描的检查方法不断改进,有望在急性缺血性卒中评估中提供与磁共振成像相当的细节;先进的灌注成像技术正推动急性缺血性卒中治疗从时间窗导向转向组织存活能力导向。血管内光学相干断层扫描(OCT)在冠状动脉介入中已成熟应用,但尚未广泛用于脑血管疾病,该技术能提供斑块、血栓和血管损伤的高分辨率详细图像,具有广阔应用前景。此外,人工智能和深度学习技术在急性缺血性卒中影像学中的应用日益广泛,有望进一步缩短梗死、出血和闭塞的检测时间,提高诊断效率和准确性。
结论
神经影像学在急性缺血性卒中的评估和管理中至关重要,每种检查方法都有其独特优势和局限性。临床实践中需结合患者具体情况和医疗机构能力,选择合适的影像学方法,同时注重多模态影像学的综合应用。持续推进技术创新、标准化成像协议以及加强临床-影像结合,是优化急性缺血性卒中患者结局的关键。未来,随着影像学技术的不断进步和临床研究的深入开展,急性缺血性卒中的影像学诊断将更加精准、高效,为改善患者预后提供更有力的支持。
原标题:《急性缺血性卒中影像学诊断的现状与进展》

