Nature子刊揭示:肠道菌群分泌囊泡,直达肿瘤激活T细胞以提升癌症治疗效果!
你可能听说过“肠道菌群影响全身健康”,但你知道吗?它甚至可以“遥控”癌症疗效。
2025年5月,《Nature Communications》刊登了一项来自美国堪萨斯大学医学院的重磅研究:研究者发现,肠道中的一种常见益生菌——双歧杆菌,能释放出极微小的胞外囊泡(BEVs)。
它们如“信使”一般穿越肠道、进入血液、最终精准抵达肺癌组织,直接激活T细胞浸润,显著增强PD-1免疫治疗的效果。
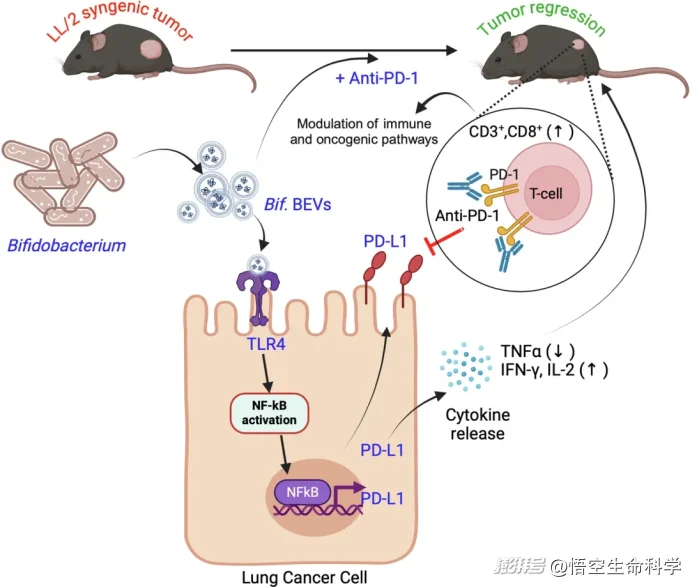
▲肠道共生双歧杆菌远程增强抗 PD-1 对肺癌的治疗效果的示意图
研究首次以实验证据证实:肠道菌群不只是调节“肠道局部免疫”,而是真正具备跨器官、跨系统调控肿瘤免疫微环境的能力。
01 从肠道出发,它们如何穿越身体边界直达肿瘤?
肠道菌群与肺癌相隔万里,但一类名为BEVs(Bacterial Extracellular Vesicles,细菌胞外囊泡)的小结构,成为“远程控制”的秘密武器。
研究团队以双歧杆菌为模型,提取其分泌的BEVs后发现:
BEVs体积极小(约100~200纳米),可穿过肠上皮屏障;
口服喂入小鼠后,BEVs经肠道→血液→肺部肿瘤组织,在8小时内精准定位到肿瘤微环境(TME);
更重要的是,它们能被肿瘤细胞主动摄取,并激活免疫相关信号通路。
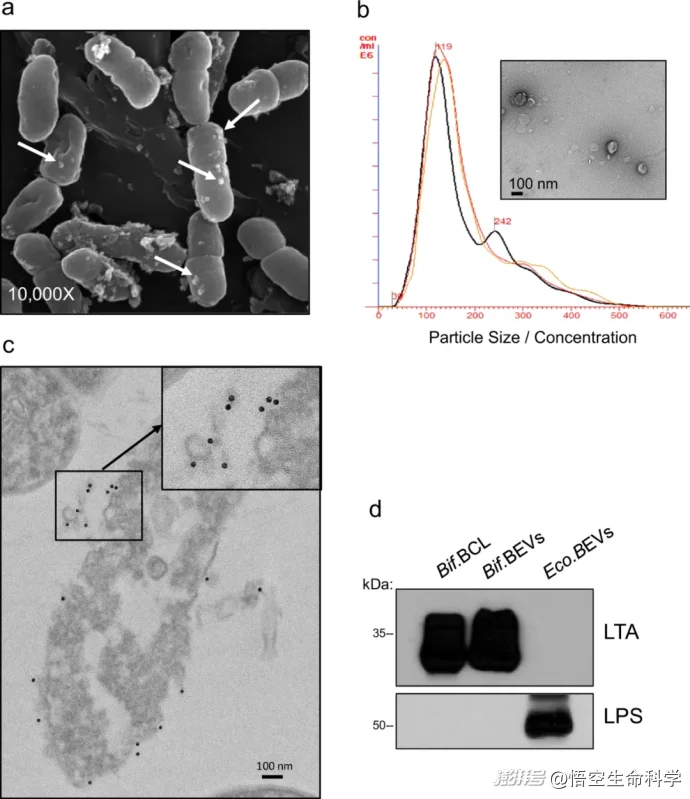
▲Bif的摄取。BEV利用动力蛋白依赖性内吞作用并调节肺癌细胞中免疫检查点的表达
这在以往是不可想象的:我们原以为益生菌只能在肠道内“做点基础工作”,没想到它们的“快递系统”如此高效,能在全身免疫防线中下达指令、调兵遣将。
这一现象,也为解答“肠道菌群如何影响远处癌症治疗”提供了坚实的细胞级机制。
02 它们激活的不只是PD-L1,而是整个T细胞战线!
不仅仅是运输到位,BEVs到达肿瘤后,还能激活多个免疫关键路径。
研究发现,BEVs被肿瘤细胞吞噬后,会释放出脂磷壁酸(LTA)等信号分子,通过TLR4-NF-κB信号通路促使肿瘤细胞上调PD-L1,并激活局部免疫炎症环境。
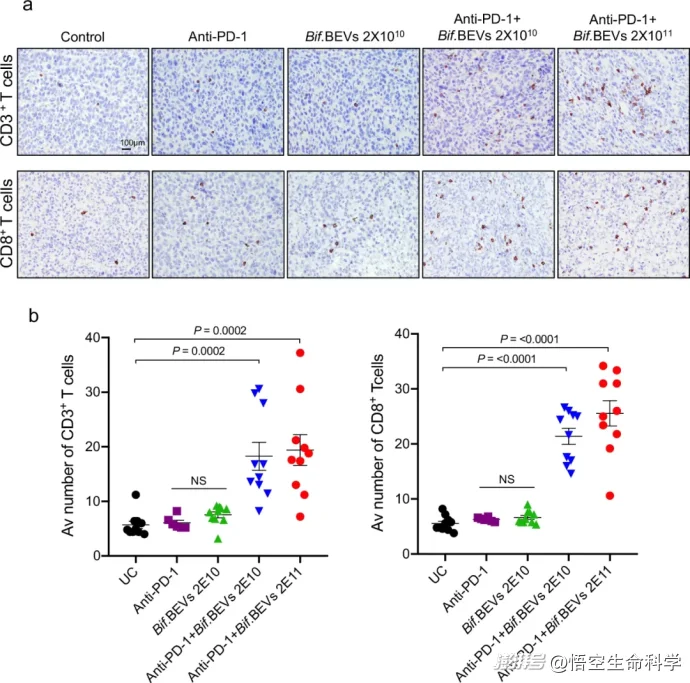
▲Bif 的组合。BEV和抗PD-1增强肿瘤浸润T淋巴细胞
更重要的是:
CD8+细胞毒性T细胞显著增加,免疫系统对肿瘤的“识别与进攻能力”提升;
肿瘤组织内IL-2与IFN-γ水平升高,T细胞扩增与细胞毒活性增强;
TNF-α下调,有助于避免免疫过度疲劳或抑制T细胞的毒副反馈。
这些变化构成了真正意义上的“免疫重新布阵”,不仅提高免疫检查点抑制剂(PD-1抗体)的治疗效果,也为T细胞提供了更健康的“作战微环境”。
而所有这些,竟然只是一个肠道细菌分泌的小小泡泡引发的连锁反应。
03 联合PD-1治疗,肠道囊泡能将“无应答者”变“部分应答者”
那么,BEVs真的能提升免疫治疗效果吗?小鼠实验给出了肯定答案。
研究团队在LL/2小鼠肺癌模型中做了精密对比:
单独使用PD-1抗体,疗效有限;
单独口服BEVs,略有作用但不显著;
联合使用PD-1抗体 + BEVs,肿瘤体积缩小显著,T细胞浸润增强,且剂量越高疗效越强。
不仅如此,组织切片检测显示,联合组肿瘤增殖指标Ki-67明显下降,免疫治疗效果被“点燃”。
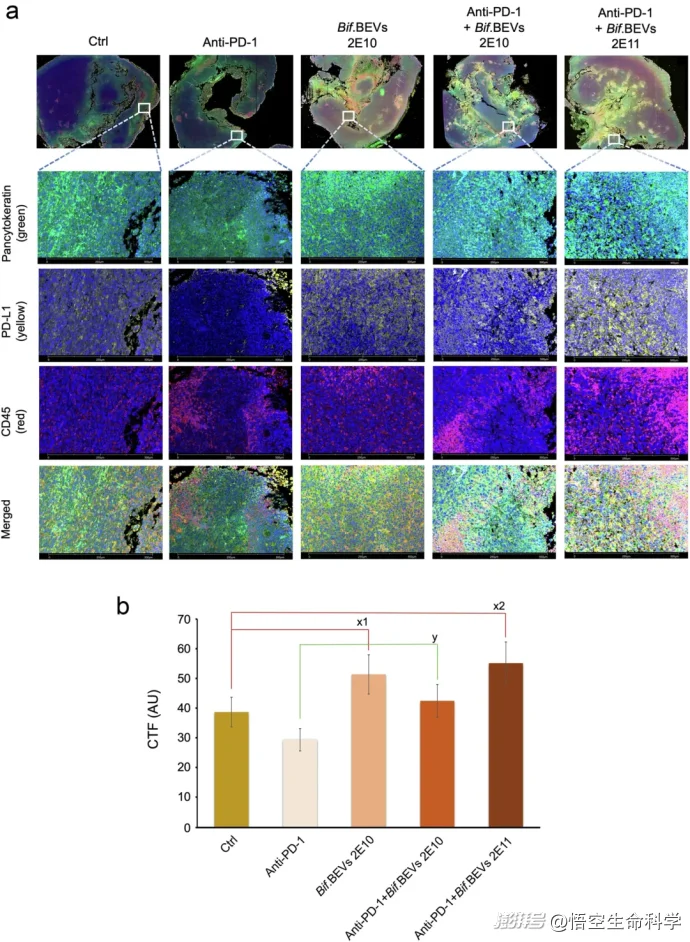
▲Bif.BEV上调肿瘤细胞中PD-L1的表达
这意味着什么?
对于那些在临床中PD-1疗法“无应答”的肺癌患者,调节肠道菌群或补充BEVs,或许能成为一把“打通免疫堵点”的钥匙。
这不仅是基础研究的突破,更可能是下一代辅助疗法的起点。
04 益生菌不再只是“调理肠胃”,而是抗癌“助攻高手”
你吃过益生菌吗?或许你从未想到,它能成为抗癌的一部分。
这一研究为益生菌领域带来了三重颠覆性认知:
1、益生菌并不只是“活菌”起效,更重要的可能是它们的分泌物(囊泡);
2、肠道菌群不仅影响肠道,也能穿越器官屏障,精确干预肺部、肿瘤等远端组织;
3、合理干预肠道菌群或补充BEVs,可能成为“口服免疫调节剂”,提高ICIs疗效。
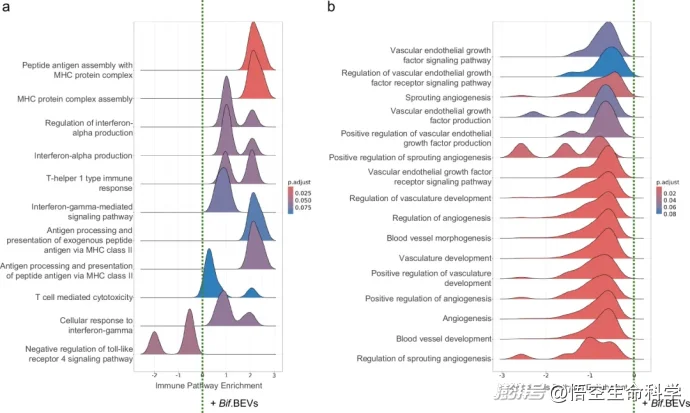
▲Bif.BEV 调节关键的免疫和致癌途径
这也揭示出一个全新的抗癌路径:不一定非要攻破肿瘤本身,有时换一个“遥控器”反而更高效。
随着未来益生菌制剂、BEVs技术、微生态免疫辅疗的兴起,个体化免疫治疗或将迈入“菌群定制”的新纪元。
05 真正决定疗效的,或许不是药物,而是你体内的“微生态密码”
肠道与肺之间,隔着千山万水,但也只隔着一层“屏障”。
科学家们正逐步揭示:决定免疫疗效的关键,不仅仅是药物有多强,而是你体内是否还有一支“信号军团”在默默出击。
Nature子刊这项研究的意义,远不止发现一个新机制,更是为提升免疫治疗应答率、减少资源浪费、实现个体化精准治疗,提供了新的战略思路。
参考文献:
Preet, R., Islam, M.A., Shim, J. et al. Gut commensal Bifidobacterium-derived extracellular vesicles modulate the therapeutic effects of anti-PD-1 in lung cancer. Nat Commun 16, 3500 (2025). https://doi.org/10.1038/s41467-025-58553-4

