CRMed:南方医科大学廖旺军团队揭示肠癌肝转移进化和耐药机制
原创 Cell Press CellPress细胞科学
 医学
医学Medicine
2024年12月4日,南方医科大学南方医院肿瘤内科廖旺军教授团队联合香港科技大学王吉光教授团队在Cell Press细胞出版社旗下期刊Cell Reports Medicine在线发表了题为“Genetic and microenvironmental evolution of colorectal liver metastases under chemotherapy”的研究论文。通过肠癌肝转移的动态多组学数据,揭示了结直肠癌肝转移在贝伐珠单抗联合化疗治疗过程中的进化和耐药规律。
结直肠癌肝转移(colorectal cancer liver metastasis, CRLM)是结直肠癌最常见的远处转移形式,化疗药物的耐药性显著降低了治疗效果,严重影响患者的预后。尽管贝伐珠单抗(Bevacizumab, BVZ)为CRLM治疗提供了一定的帮助,但药物耐药性问题仍未得到有效解决。因此,探索CRLM在药物治疗过程中的演化机制,研究原发耐药和继发耐药的规律,成为当前CRLM领域的重要研究方向。
针对这一科学问题,廖旺军教授、石敏教授和王吉光教授团队通过动态标本的生物组学数据揭示了在贝伐珠单抗联合化疗过程中CRLM进化和耐药的关键机制。研究通过对49例CRLM患者的115个动态取样标本进行多组学分析和后续的体内外实验验证。研究结果全文在Cell Reports Medicine发表。南方医科大学南方医院肿瘤内科廖旺军教授(华南理工大学附属第六医院肿瘤医学中心主任)、香港科技大学王吉光教授为本文共同通讯作者,南方医科大学南方医院肿瘤内科主任石敏教授、黄娜副教授、香港科技大学杨影茜博士、南方医科大学南方医院肿瘤内科曾东强副教授、香港科技大学莫宗超博士为本研究共同第一作者。
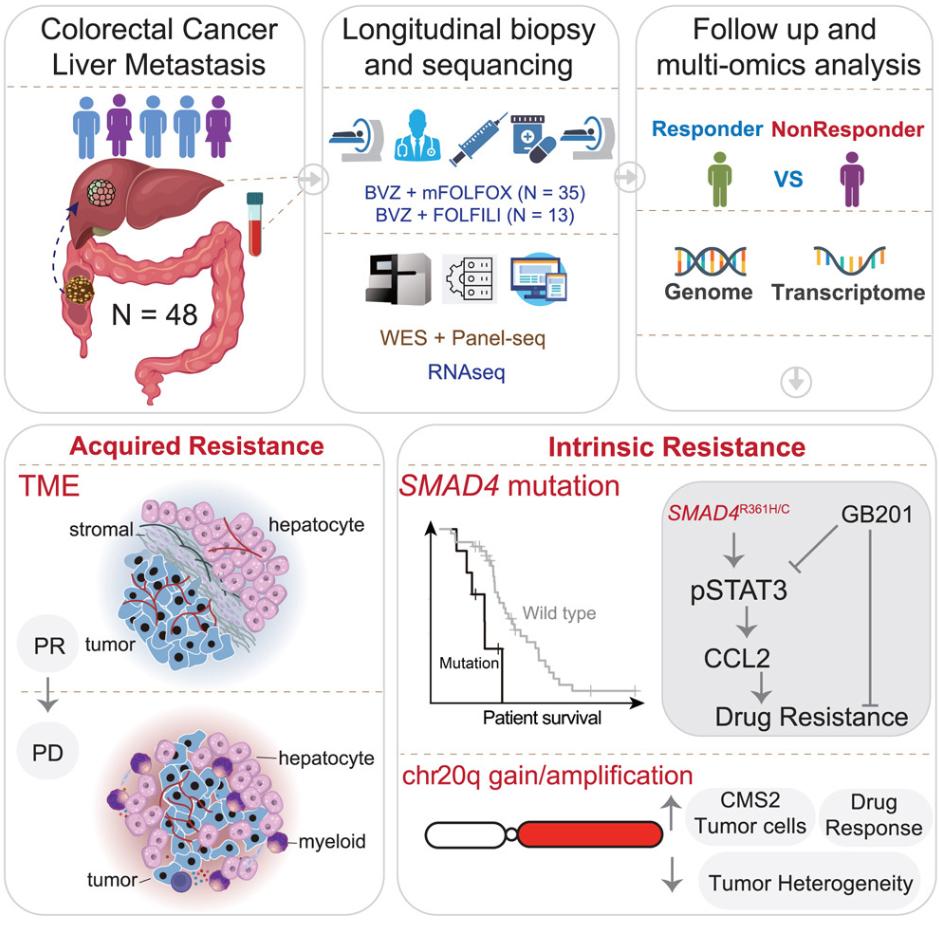
在这项研究中,团队发现尽管92%的肿瘤在基因组层面变化不大,但在转录组水平上存在显著差异。研究进一步揭示了原发耐药和获得性耐药的不同机制,并发现肝细胞和髓系细胞浸润分别在38.5%和23.1%的获得性耐药中起着重要作用。特别值得注意的是,SMAD4基因突变和20号染色体拷贝数增加与结直肠癌肝转移的内在耐药性密切相关。通过基因干扰实验,研究人员发现SMAD4R361H/C突变可通过STAT3信号通路引起贝伐珠单抗和5-氟尿嘧啶(5-FU)耐药。更为重要的是,研究团队在SMAD4R361H/C突变癌细胞中,联合使用STAT3抑制剂GB201,可有效恢复贝伐珠单抗和5-氟尿嘧啶的治疗效果。
该研究揭示了CRLM在化疗过程中的演化动力学及其微环境的变化,提出了克服药物耐药性的策略,为临床治疗提供了新的理论依据和治疗思路。该研究成果为进一步开发克服药物耐药性的新疗法提供了重要启示,有望为CRLM患者带来新的治疗希望。
 作者专访
作者专访Cell Press细胞出版社特别邀请本文通讯作者廖旺军教授进行了专访,请他为大家进一步解读。
CellPress:
近年来结直肠癌肝转移的研究现状如何?
廖旺军教授:
结直肠癌肝转移(CRLM)是结直肠癌患者中最常见的远处转移形式。随着医疗技术的进步,CRLM的诊断和治疗得到了显著改善,但其药物耐药性问题仍然是临床治疗中的主要挑战。传统的化疗方案联合贝伐珠单抗或西妥昔单抗存在耐药问题,尤其在肝转移的情况下,药物耐药性显著影响治疗效果。为此,我们通过多组学技术、肿瘤免疫微环境分析等手段,探索CRLM的进化和耐药分子机制,重点关注肿瘤细胞的基因组变异、免疫逃逸机制以及微环境重塑等方面。近年来,新的靶向治疗和免疫治疗策略也在研究中取得一定进展,但由于肝脏的免疫抑制微环境和耐药机制的复杂性,许多治疗方法尚未达到理想的效果。因此,深入研究CRLM的耐药分子机制并开发新的治疗策略依然是结直肠癌领域的研究重点。
CellPress:
本研究对指导结直肠癌肝转移治疗有哪些具体的意义?
廖旺军教授:
本研究的主要意义在于揭示了CRLM在贝伐珠单抗(BVZ)联合化疗过程中耐药性发展的关键机制。通过多时间点样本的分析,研究发现肝细胞和髓系细胞的浸润特征在CRLM获得性耐药性中扮演重要角色,这表明肿瘤微环境中的细胞重编程而非肿瘤细胞的基因突变是耐药的主要推动因素。此外,研究还揭示了SMAD4突变与化疗耐药性之间的关联,SMAD4R361H/C突变通过激活STAT3信号通路介导了贝伐珠单抗和5-氟尿嘧啶的耐药性。通过药筛和基础研究,我们发现联合STAT3抑制剂GB201与贝伐珠单抗及5-氟尿嘧啶联合使用能够显著恢复治疗效果,为克服CRLM的药物耐药性提供了新的治疗策略。这一发现为临床治疗方案的个性化制定提供了理论依据,尤其是针对具有SMAD4R361H/C突变的患者,可能会从GB201联合治疗中获益。
CellPress:
本研究还有哪些亮点?
廖旺军教授:
1. 多时间点样本的系统分析:本研究通过收集多时间点的患者样本,深入探讨了CRLM在贝伐珠单抗联合化疗过程中的肿瘤和微环境演变,揭示了耐药性发生的动态变化。
2. 耐药机制的解析:研究发现,肝细胞和髓系细胞的浸润模式是CRLM获得性耐药性的主要因素,而不是肿瘤细胞的基因突变。这一发现挑战了传统对耐药性的理解,为今后研究肿瘤微环境在药物耐药性中的作用提供了新的视角。
 通讯作者介绍
通讯作者介绍 廖旺军
廖旺军教授
廖旺军 教授 主任医师 教授 博士生导师 博士后合作导师
l 南方医科大学南方医院肿瘤内科主任医师
l 华南理工大学附属第六医院肿瘤医学中心主任
l 广东省医学教育协会肿瘤学专业委员会主任委员
l 广东省医学会肿瘤内科学分会副主任委员
l 广东省抗癌协会化疗专业委员会副主任委员
l 中国抗癌协会临床化疗专业委员会常委
l 中国抗癌协会靶向治疗专业委员会常委
主持国家自然科学基金6项,以通讯作者身份在Cell Reports Medicine, Med, Cell Reports Methods, Cancer Immunology Research等国际期刊发表高质量论文80余篇,h-index:49,累计被引11000次,其中ESI高被引论文5篇,hot paper 1篇,AACR最佳论文1篇,Cancer Immunology Research年度最高被引论文1篇,单篇最高被引710次;获国家发明专利9项,胃癌领域的研究获2022年、2023年中华医学科技三等奖,入选爱思唯尔World’s Top 2% Scientists 2023年、2024年榜单。
 王吉光
王吉光副教授
王吉光 副教授 博士生导师
香港科技大学夏利莱夫人生命科学副教授
香港科技大学生命科学部和化学及生物工程学系副教授
2019年获颁国家自然科学基金优秀青年科学家基金,2021年获颁钟南山青年科技创新奖。除了获得一些中国最负盛名的科学和创新奖项外,他还在 Cell、Nature、Nature Genetics、Science Translational Medicine、Nature Communications等学术期刊发表了30多篇论文。
 石敏
石敏教授
石敏,教授,主任医师,博士生导师,博士后合作导师。南方医科大学南方医院肿瘤内科副主任,南方医科大学南方医院肿瘤内科主任医师。广东省临床医学学会肿瘤转化医学专业委员会主任委员,广东省医师协会肿瘤内科医师分会副主任委员,广东省医师协会肿瘤重症专业委员会副主任委员,广东省医学教育学会肿瘤学专业副主任委员,广东省抗癌协会肿瘤靶向治疗专业委员会副主任委员,主持国家自然科学基金4项,广东省科技计划3项,横向科学课题基金8项,以骨干成员参与国家重点研发计划1项。以第一作者(共同一作)或通讯作者(共同通讯)在Cell Metabolism、Molecular Cancer、Cancer Communications、Cancer Research、Cancer Immunology Research、Biomaterials 、Cancer Letters、Oncogene等期刊发表SCI论文。
相关论文信息
论文原文刊载于CellPress细胞出版社
旗下期刊Cell Reports Medicine上
▌论文标题:
Genetic and microenvironmental evolution of colorectal liver metastases under chemotherapy
▌论文网址:
https://www.sciencedirect.com/science/article/pii/S2666379124006098
▌DOI:
https://doi.org/10.1016/j.xcrm.2024.101838

