Nature子刊:周荣斌/江维团队发现新型代谢免疫检查点——GPR34,带来癌症免疫治疗新策略
编辑丨王多鱼
排版丨水成文
以PD-1抗体为代表的肿瘤免疫治疗近年来取得了较大进展,改变了肿瘤的治疗模式,但目前响应率不到30%,对肝癌、结直肠癌等效果尤其不佳,亟需发展新的肿瘤免疫治疗策略和靶点。
自然杀伤(NK)细胞在肿瘤免疫中发挥重要作用,具有应答快、抑瘤谱广、通用性好、毒性小等特点,正在成为全球竞争的新赛道,但是由于肿瘤局部独特的微环境,常规NK细胞(conventional NK,cNK)存在“进入肿瘤组织难”、“进入后功能被抑制”等瓶颈问题。除了cNK外,在肝脏、肠道等组织存在大量的1型固有样淋巴细胞(type 1 Innate Lymphoid cell,ILC1),ILC1也被称为组织驻留NK细胞,近年来被发现同时具有促肿瘤和抗肿瘤的活性,但由于其与cNK细胞在表型上具有很大的相似性,目前缺乏靶向ILC1的干预手段,其在肿瘤免疫中的功能尚不明确。
2024年10月2日,中国科学技术大学生命科学与医学部、合肥综合性国家科学中心大健康研究院周荣斌教授与中国科学技术大学生命科学与医学部江维教授、王夏琼副研究员等在 Nature Immunology 期刊发表题为:GPR34 is a metabolic immune checkpoint for ILC1-mediated antitumor immunity 的研究论文,
该研究报道了肿瘤来源的脂质代谢物溶血磷脂酰丝氨酸(LysoPS)可通过其受体GPR34抑制ILC1的抗肿瘤活性,而拮抗GPR34受体可以诱导强效的ILC1介导的抗肿瘤免疫从而抑制肝癌、结直肠癌等实体肿瘤生长。
 在这项新研究中,研究团队通过构建tdTomato-GPR34报告小鼠,发现GPR34在ILC1中高表达,而在cNK细胞上不表达,提示GPR34可以作为一个新的区分ILC1和cNK的标志物。进一步利用多种不同的皮下瘤和结肠癌肝转移的原位瘤模型,研究团队发现,GPR34全身基因缺陷或ILC1条件缺陷均能增加肿瘤中ILC1的比例、数目和抗肿瘤活性,并抑制肿瘤生长,表明GPR34通过抑制ILC1的抗肿瘤活性来促进肿瘤生长。
在这项新研究中,研究团队通过构建tdTomato-GPR34报告小鼠,发现GPR34在ILC1中高表达,而在cNK细胞上不表达,提示GPR34可以作为一个新的区分ILC1和cNK的标志物。进一步利用多种不同的皮下瘤和结肠癌肝转移的原位瘤模型,研究团队发现,GPR34全身基因缺陷或ILC1条件缺陷均能增加肿瘤中ILC1的比例、数目和抗肿瘤活性,并抑制肿瘤生长,表明GPR34通过抑制ILC1的抗肿瘤活性来促进肿瘤生长。接下来,研究团队探究了GPR34调控ILC1介导的抗肿瘤免疫的机制。通过质谱检测,发现GPR34配体LysoPS在肿瘤间质液积累。体外实验表明LysoPS以GPR34依赖的方式通过cAMP-PKA-CREB途径抑制ILC1的活化。敲低肿瘤细胞上LysoPS合成酶ABHD16A的表达可以降低肿瘤间质液中LysoPS的水平并抑制了肿瘤的生长。此外,抑制肿瘤中LysoPS的产生可增加肿瘤中ILC1的数量、比例以及抗肿瘤活性。这些结果表明,肿瘤来源的LysoPS通过GPR34抑制ILC1介导的肿瘤免疫从而促进肿瘤生长。
进一步研究发现,不管是在皮下肿瘤模型还是肝转移模型中,利用抑制剂阻断GPR34均可抑制肿瘤生长,且GPR34抑制剂与抗TIGIT抗体联合使用可提高肿瘤治疗的效率。
最后,研究团队探讨了LysoPS-GPR34-ILC1通路在人类癌症中的临床相关性,发现GPR34 mRNA在结肠腺癌、头颈癌或肝细胞癌患者肿瘤组织中的ILC1样细胞上高表达,而在cNK细胞上表达较低,且ABHD16A和GPR34的表达与癌症患者ILC1的抗肿瘤活性呈负相关性。
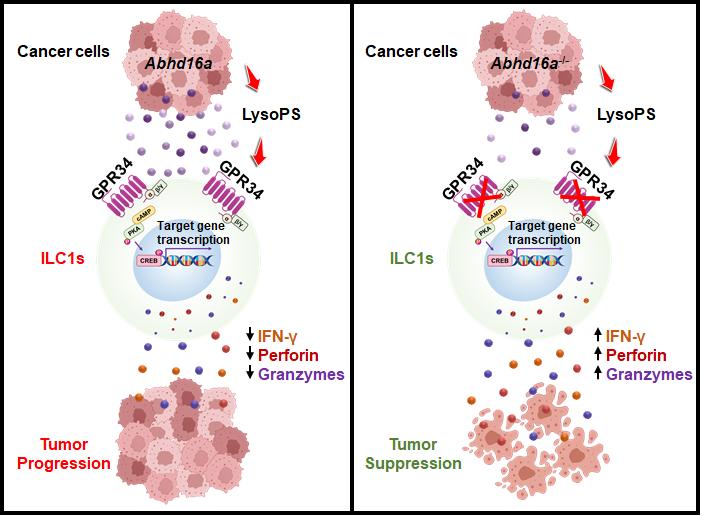 综上所述,该研究发现,肿瘤来源的脂质代谢物LysoPS可通过其受体GPR34抑制ILC1的抗肿瘤活性,而拮抗GPR34可增强ILC1的抗肿瘤活性并抑制肿瘤生长。
综上所述,该研究发现,肿瘤来源的脂质代谢物LysoPS可通过其受体GPR34抑制ILC1的抗肿瘤活性,而拮抗GPR34可增强ILC1的抗肿瘤活性并抑制肿瘤生长。该研究的创新性体现在:
1)率先证明靶向ILC1细胞(组织驻留NK细胞)可以诱导抗肿瘤免疫并抑制肿瘤生长,提示靶向组织驻留的免疫细胞对实体肿瘤可能为一种潜在的有效策略;
2)发现危险信号感应受体GPR34为一个新的代谢免疫检查点。
论文链接:
https://www.nature.com/articles/s41590-024-01973-z

