基于多源数据驱动的百合地黄汤及其活性成分抗抑郁肠-脑互作研究
肠道微生物群在抑郁症的发病机制中起着至关重要的作用,通过肠道微生物群-脑轴(GMBA)维持宿主的稳态作为治疗靶点。百合地黄汤(LBRD)及其主要活性成分毛蕊花糖苷(Verb)可改善抑郁症患者的脑和胃肠功能。然而,在使用LBRD或Verb治疗抑郁症中,肠道和大脑通过GMBA双向通信的机制仍不清楚。
基于此,2024年3月11日山东中医药大学马柯教授研究团队在Phytomedicine(中科院医学1区,IF=7.9)杂志发表了“Co-decoction of Lilii bulbus and Radix Rehmannia Recens and its key bioactive ingredient verbascoside inhibit neuroinflammation and intestinal permeability associated with chronic stress-induced depression via the gut microbiota-brain axis”揭示了百合地黄汤及其主要生物活性成分毛蕊花糖苷通过肠道微生物-脑轴抑制与慢性应激性抑郁相关的神经炎症和肠道通透性。

本研究旨在探讨百合地黄汤通过肠脑双向沟通缓解抑郁症的作用,并研究GMBA的可能途径。通过HPLC和转录组学分析,确定参与抗抑郁作用的关键分子和化合物。进一步通过行为试验、神经元形态和突触树突超微结构观察LBRD和Verb在慢性应激诱导抑郁模型中的抗抑郁作用,并在皮质酮(CORT)刺激的神经细胞损伤模型中检测其神经保护功能。LBRD和Verb通过逆转肠道微生物群紊乱和抑制肠道通透性受损或血脑屏障渗漏引起的炎症反应,改善了抑郁样行为和突触损伤。此外,在体外抑制模型中对皮质酮诱导的细胞毒性具有神经保护作用。本研究阐明了LBRD通过重塑GMBA稳态对抑郁症的多成分、多靶点、多途径治疗作用,进一步验证了肠道菌群与Verb和LBRD的抗抑郁作用之间的因果关系。

图一 LBRD制备过程中化学成分变化分析
作者分析发现LBRD及其冻干粉的成分主要包括碳水化合物、皂苷、环烯醚萜、类黄酮、酸、酯、氨基酸、多肽和生物碱。采用高效液相色谱法定性测定LBRD中FA和Verb的含量。经鉴定,这两种化合物均为LBRD的主要成分,保留时间与标准化合物一致。Verb可作为LBRD的质量标记物。接下来,作者研究了Verb是否具有与LBRD相似的抗抑郁作用。
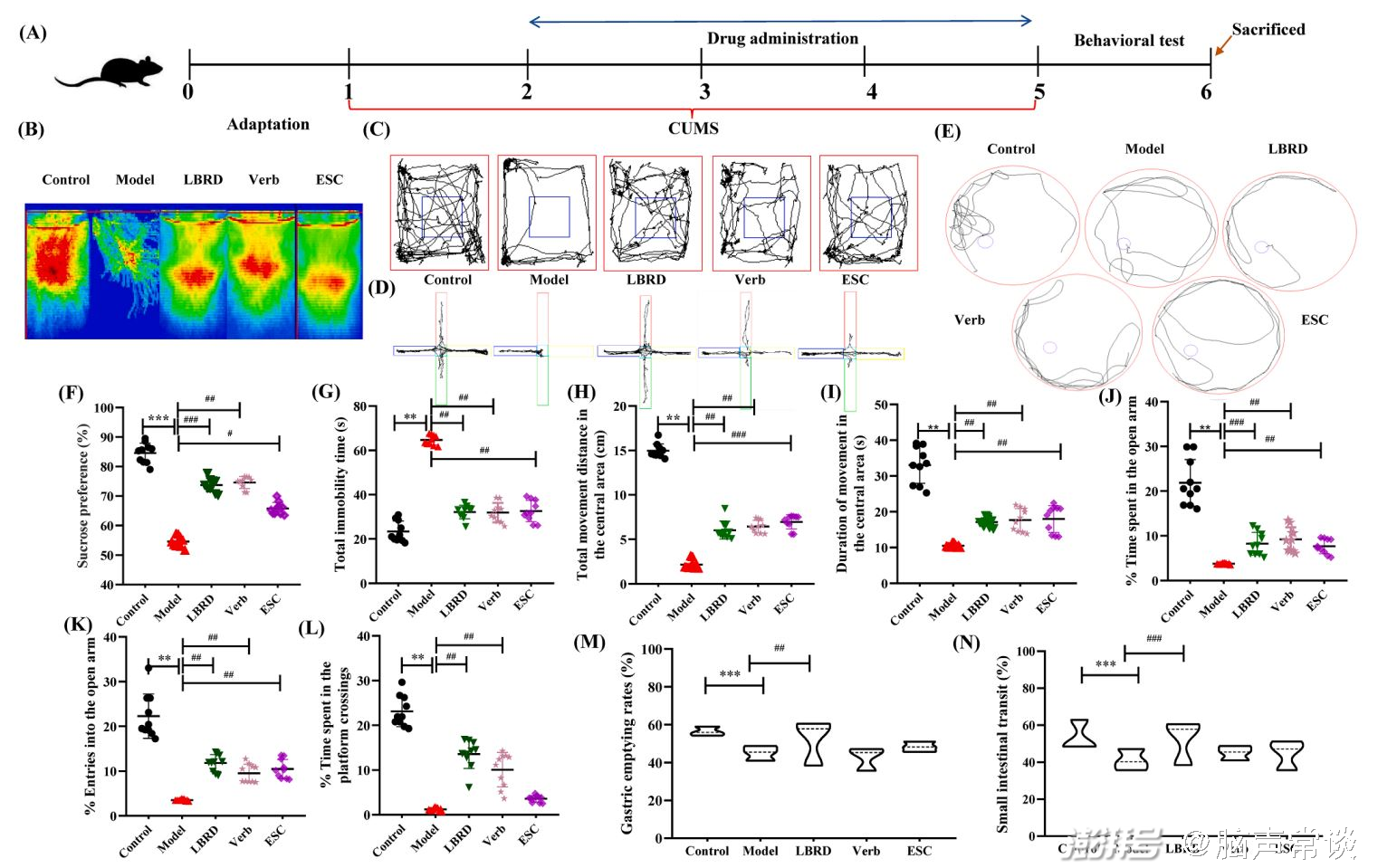
图二 LBRD和Verb可改善CUMS诱导小鼠的抑郁、焦虑样行为和消化系统功能
作者首先通过测试选择了6.25 g/kg LBRD和60 mg/kg毛蕊花苷作为最有效的给药剂量。CUMS造模小鼠表现出焦虑和抑郁反应,包括糖水偏好降低,强迫游泳实验中不动时间增加,旷场实验中运动活动和探索行为减少。与模型组相比,LBRD、Verb和艾司西酞普兰治疗均能减轻上述表型。在CUMS干预四周后,Morris水迷宫测试中穿越平台的时间缩短,表明LBRD和Verb治疗能有效改善空间记忆和工作记忆能力。此外,小鼠还表现出消化系统功能减弱,胃排空延迟,小肠推进力减少。与模型组比较,LBRD治疗可显著改善大鼠胃肠功能指数。这些结果表明,LBRD的作用与一系列抗抑郁作用有关,而毛蕊花苷和艾司西酞普兰对促进消化系统性能没有效果。
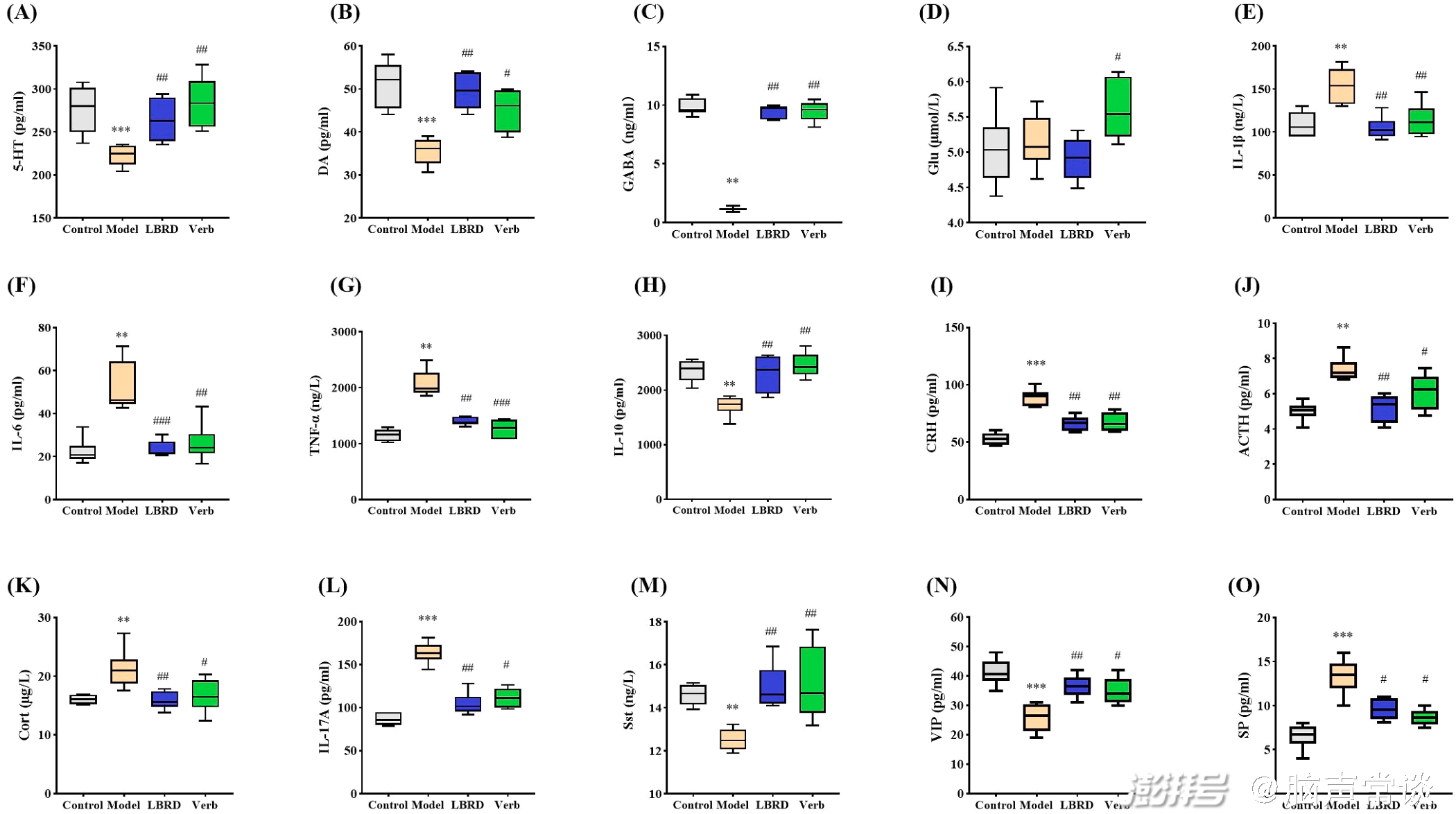
图三 LBRD和Verb治疗对小鼠CUMS诱导的抑郁模型中神经递质、炎症细胞因子和脑肠肽产生的影响
抑郁症常伴有神经递质、炎症、循环应激激素水平的异常变化。与治疗控制条件相比,CUMS治疗显著降低了5-羟色胺(5-HT)、多巴胺(DA)、γ-氨基丁酸(GABA)、白细胞介素(IL)-10和增强IL-1β、IL-6、IL- 17A、TNF-α、促肾上腺皮质激素释放激素(CRH)、促肾上腺皮质激素(ACTH)、血清激素。与CUMS诱导的抑郁样治疗组相比,连续21天口服LBRD或Verb可有效预防抑郁样改变。此外,CUMS诱导模型与对照组的兴奋性神经递质谷氨酸(Glu)含量无显著性差异。然而,用Verb处理的CUMS小鼠的Glu水平显著降低。经LBRD或Verb处理的CUMS小鼠结肠黏膜中生长抑素(Sst)、血管活性肠肽(VIP)水平显著升高,但SP水平降低。综上所述,这些数据表明LBRD或Verb可以通过产生神经递质、激素、炎症细胞因子和脑肠肽来调节脑肠轴来缓解情绪症状,从而缓解抑郁和焦虑。

图四 LBRD和Verb对皮质酮诱导的神经毒性的影响
作者接下来评估LBRD和Verb在高浓度皮质酮诱导的细胞毒性中的神经保护作用。200、400、600和800 μM CORT均显著降低了N2a细胞活力。600 μM皮质酮治疗导致细胞活力下降至约50 %。因此,作者选择了600 μM CORT进行后续实验。10%的血清LBRD可有效逆转CORT诱导的细胞活力下降。此外,在100 μmol/l剂量下,Verb孵育的细胞活力无显著变化。有趣的是,12.5、25、50和100 μmol/lVerb以剂量依赖的方式显著降低了CORT诱导的细胞毒性。在CORT诱导的抑郁细胞模型中,5-HT、GABA和IL-1β水平显著降低,但乳酸脱氢酶(LDH)活性、Glu和IL-10水平升高。这些变化与CUMS诱导的抑郁小鼠的变化一致,并被含LBRD和Verb治疗逆转。这些结果表明,LBRD和Verb对皮质酮诱导的细胞毒性具有明显的神经保护作用。
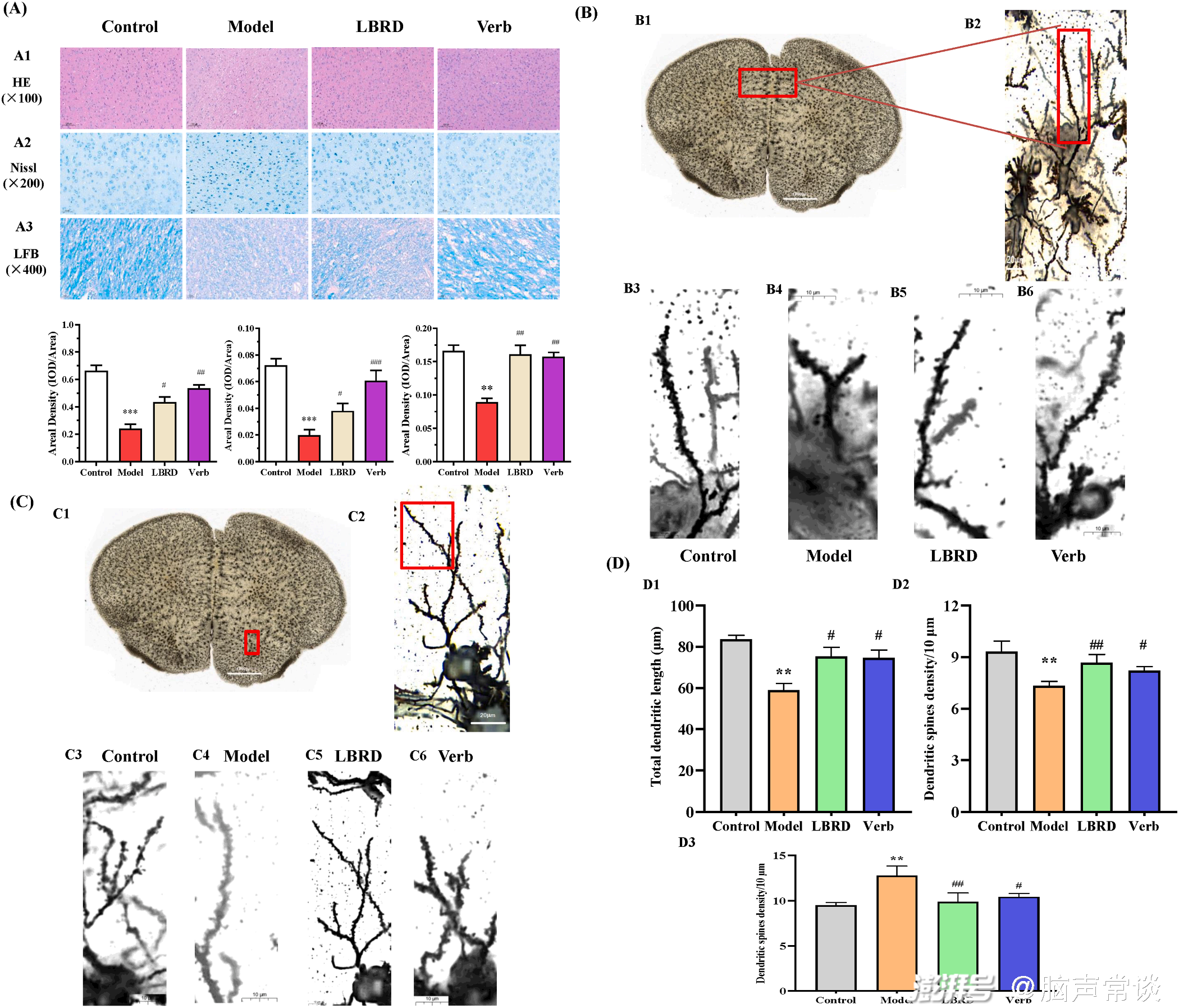
图五 LBRD和Verb治疗对小鼠CUMS诱导抑郁模型神经元形态和突触可塑性的影响
在小鼠CUMS诱导的抑郁模型中,mPFC细胞表现出一种无组织的状态,细胞极性略有改变。LBRD和Verb给药后,神经元形态有一定改善:细胞排列紧密,细胞膜、细胞质和核膜结构更清晰。结果提示,LBRD和Verb治疗可减轻神经纤维损伤。为了更密切地研究LBRD和Verb对小鼠突触可塑性稳态的影响,作者进行了高尔基染色实验。mPFC被分为三个不同的区域,即前扣带皮层(ACC)、前边缘皮层(PL)和边缘下皮层(IL)。CUMS显著降低了PL区域的总树突长度和脊柱密度,LBRD和Verb治疗逆转了CUMS诱导的mPFC神经元树突棘密度的变化。然而,与对照组相比,CUMS暴露导致NAc中的MSNs树突的脊柱密度显著增加。与CUMS组相比,LBRD和Verb治疗逆转了这种增加。
总结:
累积轻度应激引起的异常炎症细胞因子和神经肽的产生导致情绪回路内谷氨酸能和伽马氨基丁酸能传递失调,引发胃肠道功能障碍,对认知功能和情绪产生负面影响。LBRD治疗可缓解肠道微生物群破坏,调节肠道屏障和血脑屏障通透性,减少情绪神经通路中的肠道炎症和免疫炎症反应,修复神经元损伤,修复突触可塑性。总的来说,这些作用调节外周血和脑区域的促炎细胞因子和神经肽水平,最终纠正中枢神经系统神经递质缺陷,特别是E/I神经递质失衡,并抑制免疫和炎症反应。LBRD和Verb通过GMBA调节多个靶点和信号通路调节肠道和大脑之间的双向通信,实现抑郁症患者多系统功能的平衡。本研究为探讨LBRD和Verb靶向GMBA治疗抑郁症的药效学基础和机制提供了参考。
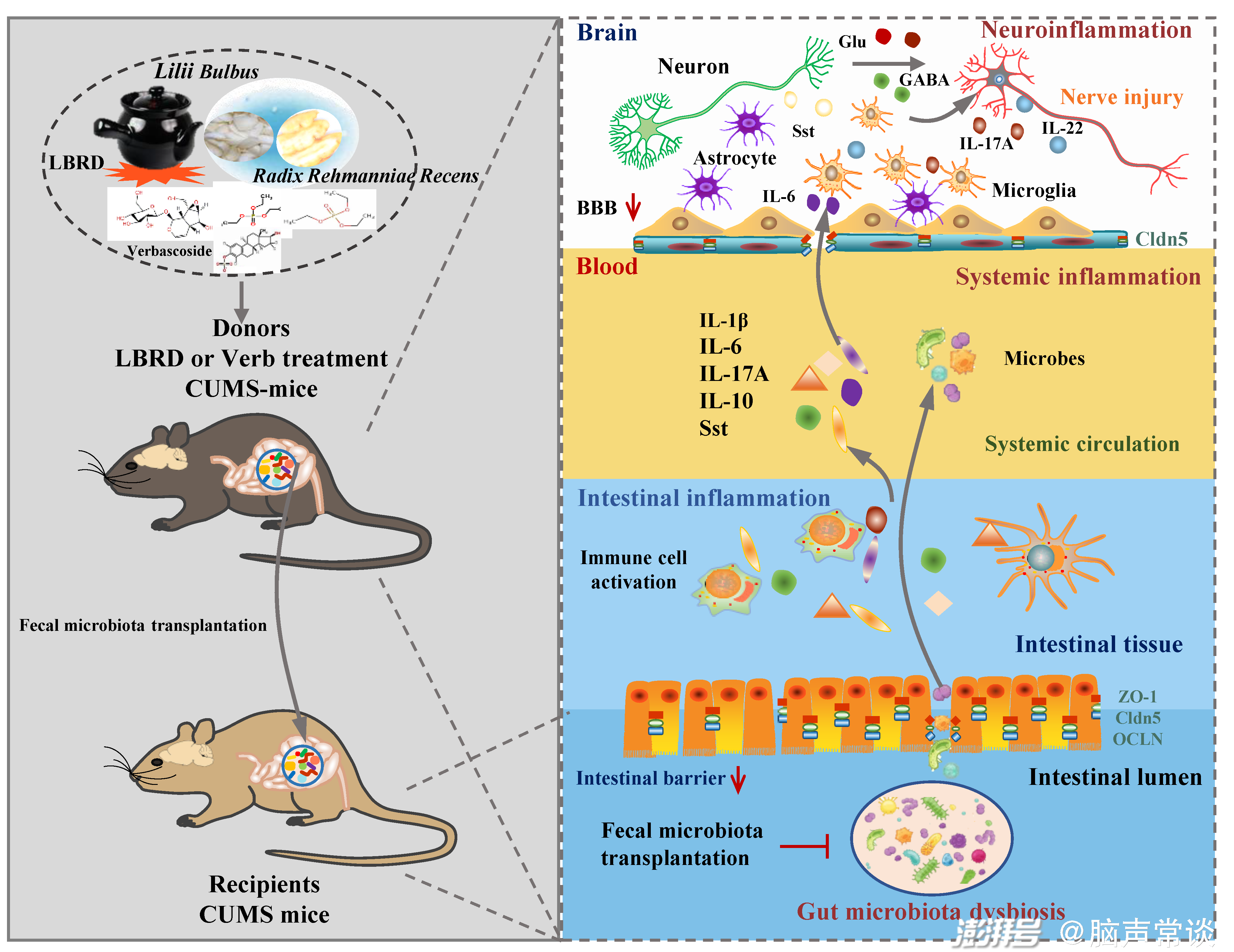
图六:LBRD与Verb经多途径干预肠脑互作发挥抗抑郁功效
文章来源:https://doi.org/10.1016/j.phymed.2024.155510

