贵州医科大学左石/陈腾祥发现肝细胞癌靶向治疗策略
原创 转网
 本文为转化医学网原创,转载请注明出处
本文为转化医学网原创,转载请注明出处作者:Rainbow
导读:肝细胞癌(HCC)是肝癌最常见的亚型,约占所有肝癌病例的75%。
3月27日,贵州医科大学左石、陈腾祥共同通讯在期刊《Cell Death Discovery》上在线发表题为“NAP1L1 regulates BIRC2 ubiquitination modification via E3 ubiquitin ligase UBR4 and hence determines hepatocellular carcinoma progression”的研究论文,研究结果为开发靶向NAP1L1治疗肝细胞癌的药物提供了新的理论依据。
 https://www.nature.com/articles/s41420-024-01927-2
https://www.nature.com/articles/s41420-024-01927-2研究背景
01
原发性肝癌是全球第七大常见肿瘤,也是癌症相关死亡的第二大原因,其发病率逐年增加。肝细胞癌(HCC)是肝癌最常见的亚型,约占所有肝癌病例的75%。肝细胞癌(HCC)的进展与肿瘤细胞的凋亡逃逸密切相关,这促进了癌细胞的长期存活和异常增殖,是多药耐药发展的重要机制。激活或恢复肿瘤细胞凋亡是治疗肿瘤的有效策略。肿瘤细胞的凋亡逃逸涉及多条信号通路和表观遗传修饰,包括关键蛋白的翻译后调控。泛素化在泛素-蛋白酶体系统中是重要的翻译后修饰,负责调控与凋亡相关蛋白的降解和周转。
NAP1L1是核小体组装蛋白1样蛋白家族的成员,具有高度保守的中心结构域、一个晶体结构域和两个N端结构域。它主要分布在细胞质中,其次分布在细胞核中。几项研究表明,NAP1L1是潜在的促肿瘤因子,参与了恶性肿瘤(如肝细胞癌、结直肠癌和乳腺癌)的发展进程。阐明NAP1L1对肝细胞癌细胞不同恶性特征的影响可能有助于理解NAP1L1的生理功能。
BIRC2通过与肿瘤坏死因子受体相关因子结合来抑制细胞凋亡,并已被确定为肿瘤细胞异常增殖、多药耐药和免疫逃逸的关键驱动因素。BIRC2介导的细胞凋亡逃避在HCC的发生中起关键作用。泛素化的失调与BIRC2的异常降解和癌细胞的凋亡逃逸有关。研究BIRC2稳定在HCC进展中的作用对于了解HCC细胞凋亡逃逸机制非常重要。
研究发现
02
之前已经证实,NAP1L1的异常高表达通过募集HDGF来调节c-Jun的功能,增强了CCND1的表达,并促进了HCC细胞的增殖。在这项研究中,研究人员发现NAP1L1不影响HCC细胞的迁移和侵袭能力,而是通过E3泛素连接酶UBR4影响BIRC2蛋白的稳定性,调节细胞凋亡的发生并决定HCC的进展。总之,这项研究揭示了一种新的机制,NAP1L1通过UBR4影响BIRC2的泛素化,并调节细胞凋亡以确定HCC的进展。该机制代表了靶向NAP1L1治疗以NAP1L1或BIRC2高表达为特征的HCC的有前景的策略。
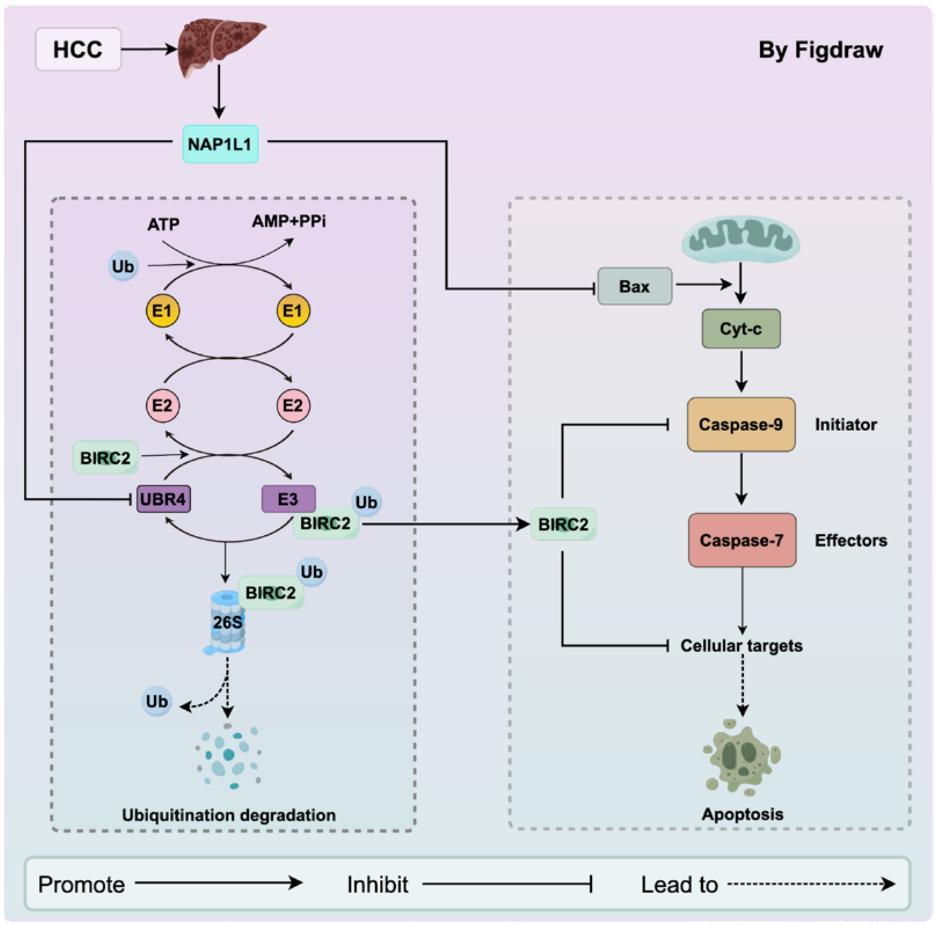 研究结论
研究结论03
综上所述,研究结果为开发靶向NAP1L1治疗肝细胞癌的药物提供了新的理论依据。
参考资料:
https://www.nature.com/articles/s41420-024-01927-2
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。

原标题:《抑制肿瘤进展!贵州医科大学左石/陈腾祥发现肝细胞癌靶向治疗策略》

