Science子刊:发现肥胖治疗新靶点
原创 生物世界
撰文丨王聪
编辑丨王多鱼
排版丨水成文
自1975年以来,全球肥胖症患病率已经增长了三倍,而最近,《柳叶刀》发布的最新数据显示,目前全世界肥胖人数已超过10亿,而且,儿童和青少年肥胖率正在快速增长。肥胖症是多种严重非传染性疾病的风险因素,包括2型糖尿病、心血管疾病及癌症。
长效胰高血糖素样肽1(GLP-1)受体激动剂(例如司美格鲁肽),以及联合GLP-1受体和葡萄糖依赖性胰岛素多肽(GIP)受体双重激动剂(例如替尔泊肽)的成功开发和上市了肥胖治疗中的重大突破,但这些药物也面临着一系列挑战。除了依从性问题之外,有相当比例的患者在治疗后未能达到>5%的减重效果,并且大多数患者在停药后会出现明显的体重反弹。
因此,在基于肠促胰岛素的减肥药物取得巨大商业成功的同时,对具有不同作用模式的新型减肥药物的需求也在不断增长。
2024年3月1日,哥本哈根大学的研究人员在 Science Advances 期刊发表了题为:Targeting postsynaptic glutamate receptor scaffolding proteins PSD-95 and PICK1 for obesity treatment 的研究论文。
该研究发现并证实,靶向突触后谷氨酸受体支架蛋白PSD-95和PICK1可治疗肥胖症,能够选择性地减少体重和脂肪,并且在治疗停止后体重减轻仍能持续,表明了含有PDZ结构域的突触后谷氨酸受体支架蛋白代表了以前未知的治疗肥胖的药物靶标类别。
 在过去的十年里,全基因组关联分析(GWAS)揭示了许多可能导致肥胖发病的信号通路。值得注意的是,通过遗传学研究确定的许多基因和通路在大脑内富集或仅表达于大脑中,这强调了中枢神经系统(CNS)在肥胖病理生物学机制中的关键作用。
在过去的十年里,全基因组关联分析(GWAS)揭示了许多可能导致肥胖发病的信号通路。值得注意的是,通过遗传学研究确定的许多基因和通路在大脑内富集或仅表达于大脑中,这强调了中枢神经系统(CNS)在肥胖病理生物学机制中的关键作用。在肥胖的遗传研究中,与AMPA和NMDA受体相关的谷氨酸能信号转导和突触后可塑性相关的基因尤其丰富,这表明谷氨酸能神经递质系统在调节能量平衡的稳态机制中起着重要作用。但这些通路在肥胖治疗中的治疗价值仍需仔细审查。
在啮齿动物中的研究证实了干扰NMDA受体信号通路的潜在减肥益处,此外,有证据支持拮抗AMPA受体可以减轻食物驱动行为的观点。然而,AMPA和NMDA受体在中枢神经系统(CNS)中广泛表达,这些受体的化学调节剂通常存在脱靶效应。为了避免这些问题,科学家们开始探索靶向细胞内受体蛋白复合物的治疗靶点,以实现对突触后受体信号的精确干扰。
AMPA和NMDA受体都直接与细胞内支架蛋白相互作用,这些支架蛋白参与了膜上谷氨酸受体的锚定和运输。许多这些支架蛋白包含PDZ结构域(PSD-95/disc large/ZO-1)。含PDZ结构域的蛋白质支持突触后谷氨酸受体复合物的形成和稳定,并成为多种中枢神经系统疾病(例如卒中和神经病理性疼痛)的有前途的治疗靶点。然而,这类蛋白质在肥胖发病机制中的参与及其对减重的治疗潜力尚未得到研究。
在这项研究中,研究团队使用英国生物样本库(UK Biobank)GWAS对体重指数(BMI)和身体脂肪百分比(BF%)进行汇总统计分析,确定了与AMPA和NMDA受体相互作用的蛋白质的编码基因。DLG4和与PICK1基因位点在BF%和/或BMI方面达到全基因组显著关联。
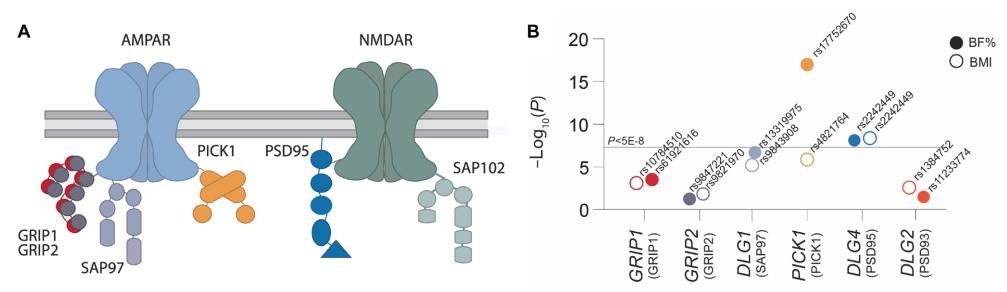 为了进一步评估突触后密度蛋白-95(PSD-95,由DLG4基因编码)和PICK1在能量稳态中的功能作用,使用二聚体多肽靶向抑制PSD-95和PICK1,证明了抑制PSD-95和PICK1在肥胖小鼠中诱导了延长的减重效果。
为了进一步评估突触后密度蛋白-95(PSD-95,由DLG4基因编码)和PICK1在能量稳态中的功能作用,使用二聚体多肽靶向抑制PSD-95和PICK1,证明了抑制PSD-95和PICK1在肥胖小鼠中诱导了延长的减重效果。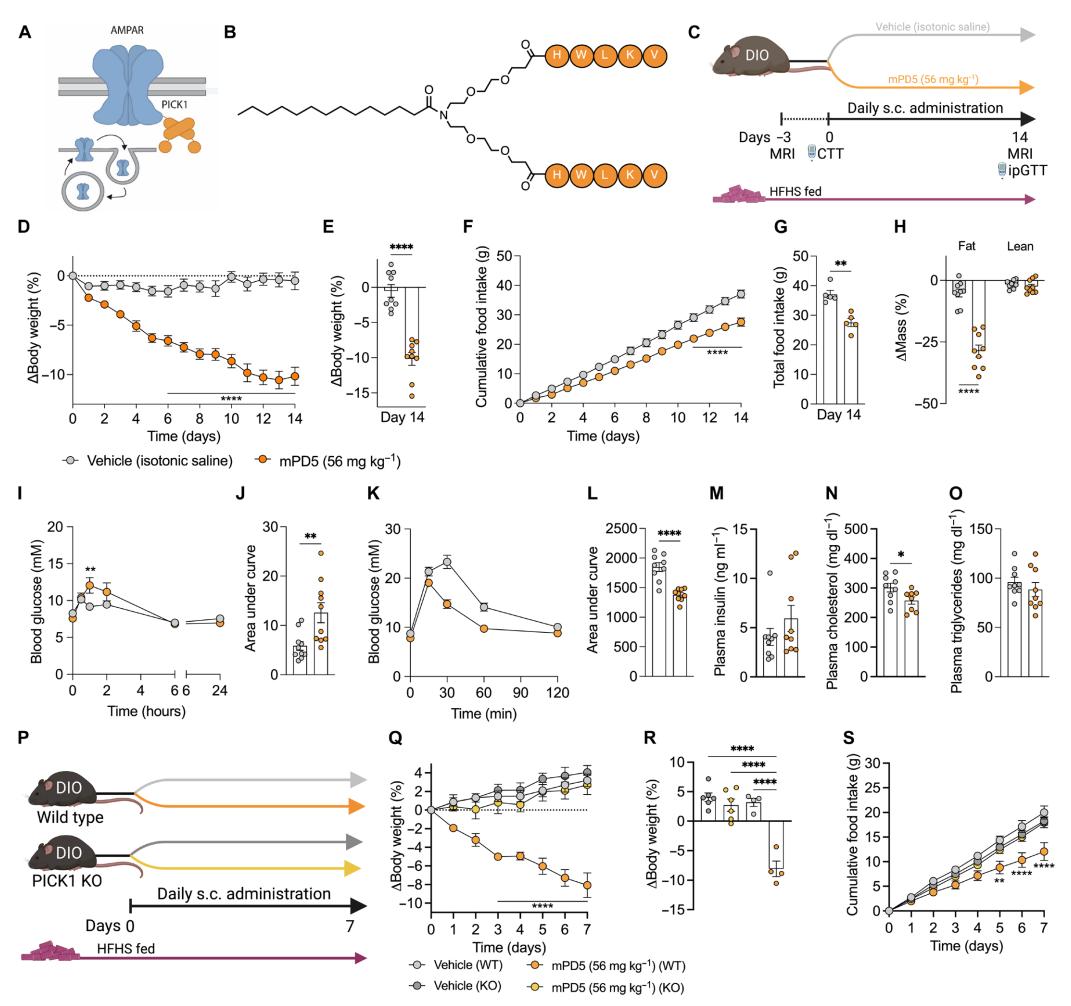
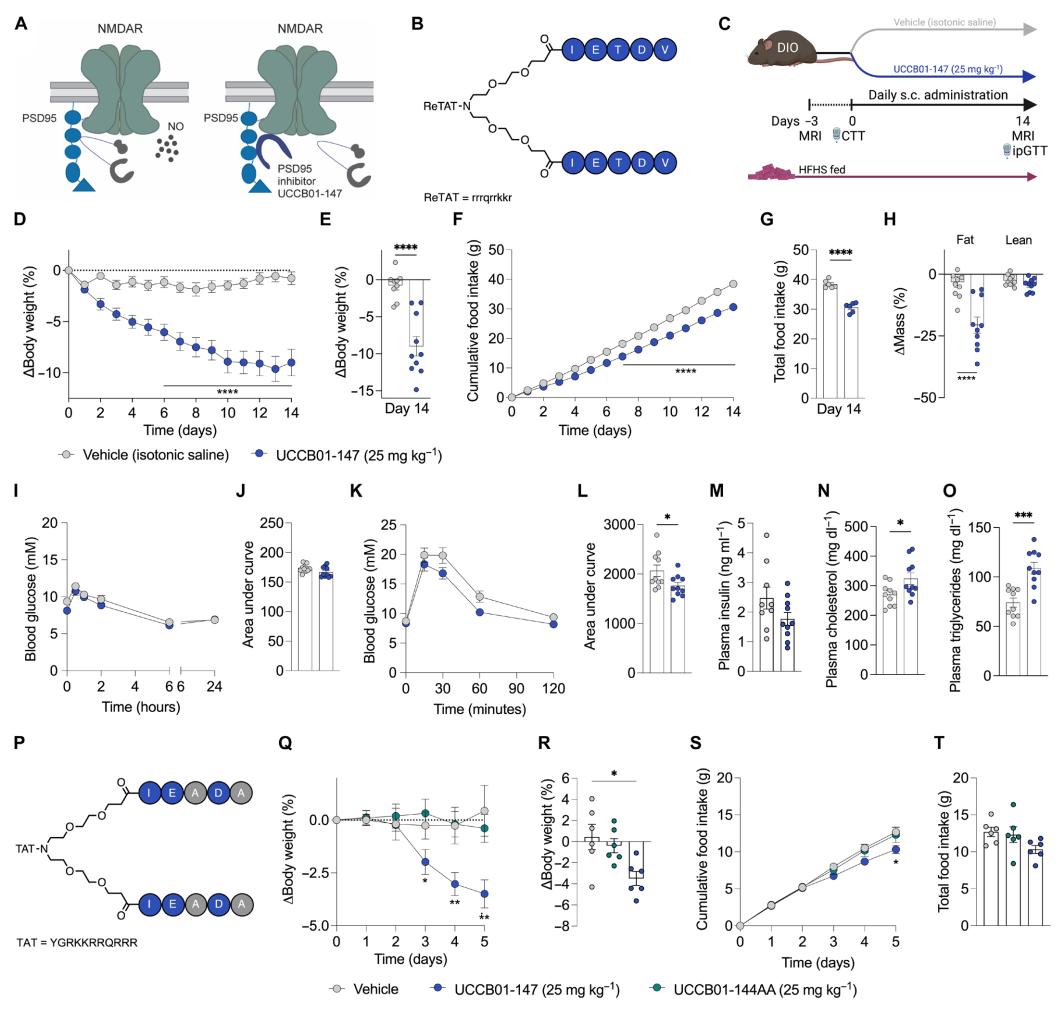 这些结果表明,谷氨酸受体支架蛋白PICK1和PSD-95与肥胖具有遗传关联,而对其PDZ域的药理学靶向治疗,是实现长效减重的有前途的新方法。
这些结果表明,谷氨酸受体支架蛋白PICK1和PSD-95与肥胖具有遗传关联,而对其PDZ域的药理学靶向治疗,是实现长效减重的有前途的新方法。总的来说,该研究将人类基因组数据与啮齿类动物的体内药理学相结合,以识别和功能验证PSD-95和PICK1在体重调节中的意义。并进一步证明了PICK1和PSD-95的二聚体多肽抑制剂可选择性地减少体重和脂肪,并且在治疗停止后体重减轻仍能持续。表明了含有PDZ结构域的突触后谷氨酸受体支架蛋白代表了以前未知的治疗肥胖的药物靶标类别。
论文链接:
https://www.science.org/doi/10.1126/sciadv.adg2636

