多种合并症,老年UC患者如何治疗安全又有效?
仅供医学专业人士阅读参考
老年UC合并糖尿病、LTBI、双侧股骨头无症状坏死患者,维得利珠单抗助力达标
溃疡性结肠炎(UC)是一种慢性非特异性炎症性肠病(IBD),其病程迁延反复,发病率在我国呈逐年增长趋势[1,2]。UC可发生在任何年龄,主要呈现双峰型发病高峰,第一高峰出现在15~30岁之间,第二较明显的高峰在50~70岁之间。但随着全球人口老龄化的日益加深,老年发病的UC患者呈上升趋势。老年患者合并症多,病情复杂,对治疗方案安全性要求显著增加,需全面评估选择兼顾疗效及安全性的疾病管理方案。
本期我们邀请上海吴淞中心医院消化内科沈祥国医生,分享了1个经典案例,看看维得利珠单抗如何有效治疗,老年UC反复发作合并多种合并症的患者。
作者简介
沈国祥 医生
上海吴淞中心医院 消化内科
主方向为炎症性肠病临床诊疗
擅长胆胰疾病诊疗,熟练消化内镜操作
近两年在多项全国IBD案例比赛中均晋级全国总决赛并获奖
发表SCI、核心论著多篇,参与编译著作2部
主持宝山区科协基金一项
CCCF认证医师
典型案例
患者男,68岁。
外院诊疗病史
2020年6月29日某医院肠镜:插镜至回末、距肛缘2~10cm黏膜充血、水肿、触之易出血,散在糜烂浅溃疡形成,黏膜细颗粒状失去光泽,直肠散在点状充血,被诊断为UC。
2020年7月,因“反复腹痛黏液脓血便8年,加重伴腹泻半月”外院住院诊疗。完善全面筛查,但出院小结未见腹部CT/MR检查,未见TSPOT、PPD、结核抗体检查结果。只有胸部CT提示“两侧肺尖陈旧性结核灶”,且餐后血糖异常升高。诊断为UC E2 中度;脑梗死个人史;2型糖尿病。予以地塞米松、康复新、庆大霉素灌肠,美沙拉嗪口服 3g 每天一次(qd)联合肛栓 0.5g 每晚一次(qn)进行治疗,症状好转后出院。
2020年9月,患者症状反复,且显著加重,腹痛腹泻黏液血便达6-8次/日,在外院行肠镜检查。结果显示:插镜至回末,距肛缘28cm以下至直肠可见黏膜弥漫充血水肿、糜烂、自发性出血,大量白色分泌物,血管纹理消失,结肠袋消失。直肠黏膜充血、近肛门口可见少量白色分泌物。诊断为UC E2 活动期 Mayo 3分。患者述外院准备行系统性激素治疗,先予以异烟肼预防性治疗2周余停药,原因不详,激素灌肠2月后停用,否认静脉/口服激素;虽然使用甲硝唑灌肠,但该院本次出院小结,无机会感染证据及相关诊断;患者诉后续继续美沙拉嗪口服联合肛栓治疗。
2021年6月行外院肠镜复查,插镜至回末,直肠近肛缘轻度炎症。诊断为直肠轻度炎症。
2021年7-9月,患者因血便,在某医院肛肠科按照“痔疮”治疗,无效,外院再次复查肠镜。结果显示:插镜至回末,距肛缘25-10cm可见黏膜连续糜烂充血、多发小溃疡,可见陈旧性出血斑,血管纹理消失,余结直肠黏膜光滑,黏膜下血管纹理清晰。诊断为UC E2。未调整治疗方案,未住院,继续美沙拉嗪治疗。
经过外院反复治疗,患者自述只进行了前后共计约4个月激素灌肠,否认系统性激素用药,之后均为莎尔福 3g qd 口服,0.5g qn 纳肛,后激素自行停药。
2022年1月因UC症状第一次入院
现病史:
患者于2022年1月入院我科,排便每日4~5次不成型便,伴有脓血,无发热、无肠外表现。
既往史:
28岁(40年前)结核病史,TSPOT/PPD阳性,潜伏性肺结核感染(LTBI),自述已治愈,未复发。58岁时曾因“脑梗死”住院治疗,治疗后恢复可,无明显后遗症;否认食物药物过敏史,否认其他传染病史,否认遗传、免疫、肿瘤家族史。既往因服用阿司匹林出现上消化道溃疡伴出血,后停用。
辅助检查
粪常规:红细胞 15-20个,白细胞 15-20个,钙卫蛋白 511.02ug/g,隐血及转铁蛋白阳性;
炎症指标:CRP 0.6mg/L;ESR 19mm/H;
血常规:WBC、PLT未见明显异常;糖化血红蛋白 7.2%。
肿瘤指标/CMV/HSV/EBV/自身抗体及抗肝抗体谱/抗O/类风湿因子/免疫球蛋白/补体C3、C4/HLA-B27/细胞因子/粪培养及寄生虫筛查均未见明显异常。
结核检查:T-SPOT、结核抗体IgG、IgM均阴性(异烟肼治疗后14个月);TSPOT:结核分枝杆菌γ干扰素释放试验(T-N) 0.28(<0.35 IU/mL);结核分枝杆菌特异性T细胞γ干扰素释放试验阴性(-)。
20220110肠镜检查:插镜至回末,距肛缘28~10cm可见四壁黏膜鹅卵石样表现、散在溃疡、小片状糜烂、可见新鲜血迹及脓性分泌物,10cm至肛缘四壁黏膜散在红斑、充血水肿明显(图1)。诊断为UC、E2、活动期、乙状结肠Mayo 3分、直肠Mayo 2分。
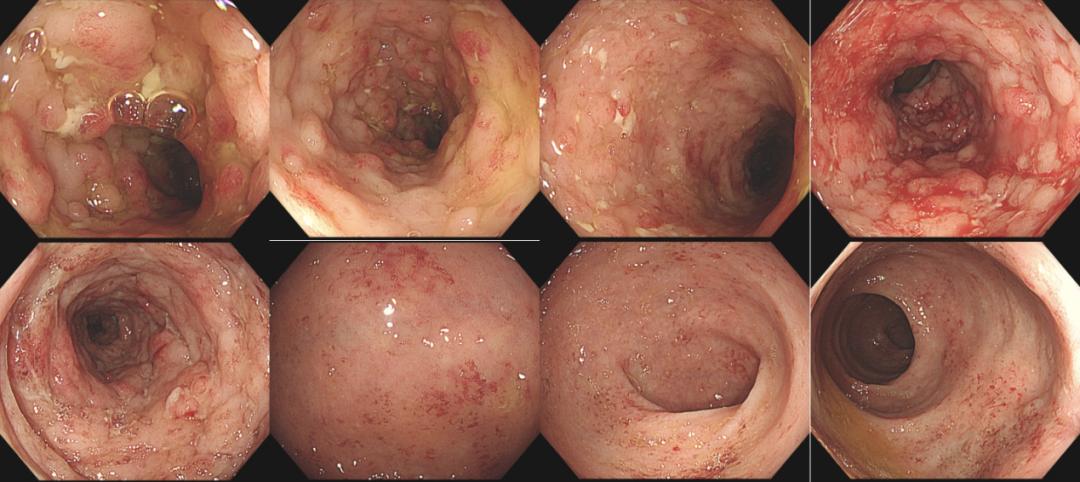
图1 入院时肠镜检查图
胸部CT:两肺上叶纤维条索灶及钙化灶。两肺上叶气肿伴肺大泡,左肺下叶结节,主动脉及冠脉硬化(图2)。
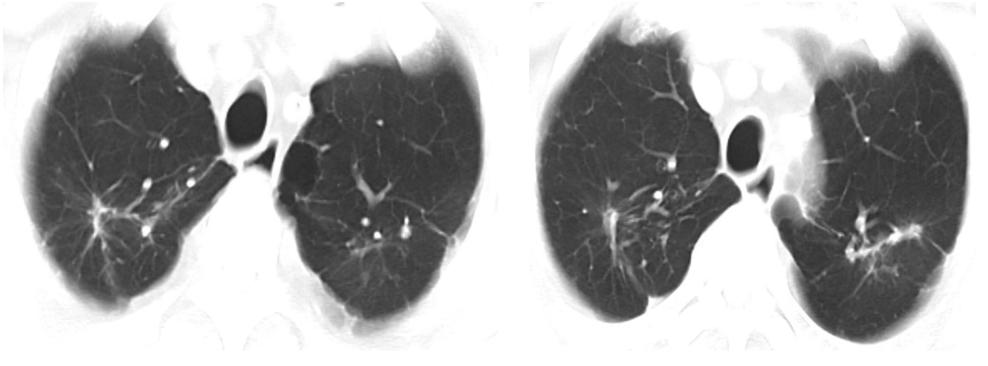
图2 入院时胸部CT
CTE:乙状结肠局部肠壁增厚伴周围多发稍大淋巴结,考虑炎性病变可能大;前列腺点状钙化灶。阑尾稍增粗。
胃镜:胆汁返流性胃炎,糜烂性胃炎,十二指肠球部假憩室。
盆腔MRI:肛周、会阴软组织未见明显异常,增强未见明显异常强化。所见盆腔内未见明显积液,未见明显肿大淋巴结。附见:双侧股骨头斑片状异常信号影,呈T1WI低、T2WI高信号影,增强后强化(图3)。结论:肛周、会阴软组织未见明显异常。双侧股骨头异常信号影,怀疑股骨头坏死。
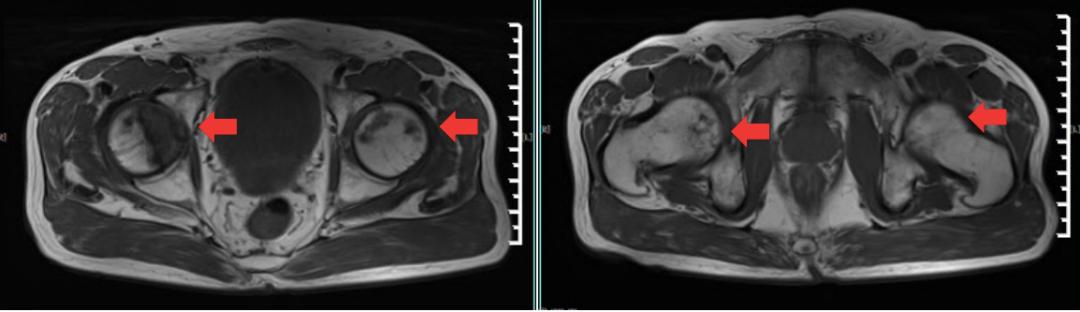
图3 盆腔MRI
骨密度检查:显示骨量减少。
股骨头CT:右侧股骨头变形、塌陷,右侧股骨头骨质内见囊性骨吸收破坏区,部分边缘硬化,左侧股骨头局部密度增高,余双侧髋臼骨质增生,关节在位,关节间隙未见明显异常(图4)。检查结论:右股骨头坏死改变,左股骨头局部密度增高,建议进一步MRI检查。
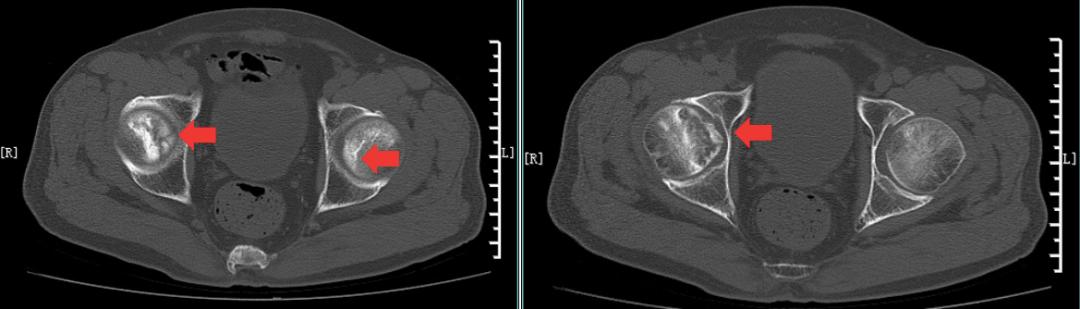
图4 股骨头CT
诊断:
UC(E2 慢性复发型 活动期;Mayo总评分10分;Mayo内镜直肠2分,乙状结肠3分);合并双侧股骨头无症状坏死;2型糖尿病;LTBI;脑梗死个人史。
治疗方案:
美沙拉嗪 4g qd po,美沙拉嗪灌肠液 4g qn;补充维生素D钙片;骨科会诊,建议严密随访,严禁负重,必要时手术更换股骨头。
美沙拉嗪灌肠液灌肠10天后,复查粪常规,未见红白细胞,隐血阳性;粪钙卫蛋白降至316ug/g,由于TSPOT目前阴性,外送完善粪艰难梭毒素检测后,2022年1月19日,第一次维得利珠单抗300mg静滴,过程顺利;
患者最终于2022月1月20日出院,嘱继续美沙拉嗪口服联合灌肠治疗,随访后视情况逐步停药;2月17日,粪钙卫蛋白 33.2ug/g,CRP 4.6mg/L;2月28日完成第三次维得利珠单抗治疗;第一次注射一周内排便逐步减少至每日1次成型黄色便。
诱导期结束启动异烟肼单药预防性抗痨
诊疗计划:
20220228按计划入院行第三次维得利珠输注。本次入院前,2月下旬起夜受凉后出现反复干咳。
辅助检查:
20220228 肺部低剂量CT平扫+冠状位重建:左肺下叶炎症,左肺下叶结节,建议抗炎后复查。两肺上叶纤维条索灶及钙化灶,考虑陈旧性结核可能。两肺上叶气肿伴肺大泡。胸膜局部增厚。主动脉及冠脉硬化(图5)。
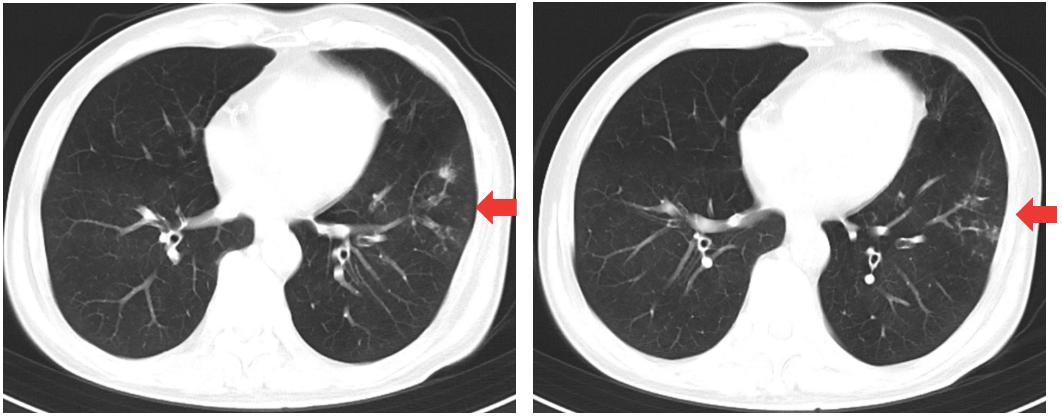
图5 二次入院肺部CT
20220302 诱导期结束TSPOT监测:结核分枝杆菌γ干扰素释放试验(T-N) 0.75↑(<0.35 IU/mL);结核分枝杆菌特异性T细胞γ干扰素释放试验阳性(+)。
治疗方案调整:
按计划行第三次维得利珠单抗治疗,诱导期结束同步开始联合异烟肼0.3g/d预防性抗痨。呼吸科会诊,咳嗽及左下肺炎症考虑普通肺炎,予以莫西沙星0.4g qd口服。
转归:
咳嗽症状显著改善。3月22日门诊复查左肺下叶炎症显著好转(图6)。
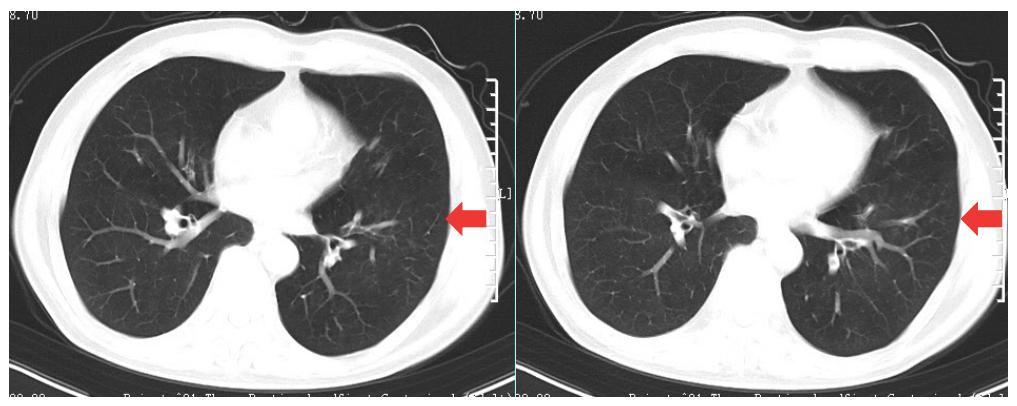
图6 复查肺CT
20220430 粪常规,发现隐血试验阳性↑,转铁蛋白:阳性;钙卫蛋白:34.85ug/g。
20220703完成第五次输注,病情稳定:TSPOT定期监测 结核分枝杆菌γ干扰素释放试验(T-N) 0.76↑ (< 0.35 IU/mL);结核分枝杆菌特异性T细胞γ干扰素释放试验 阳性(+)。与20220302 TSPOT检测值(0.75)无明显变化,LTBI状态稳定。
20220704 肠镜检查(图7):提示粘膜愈合
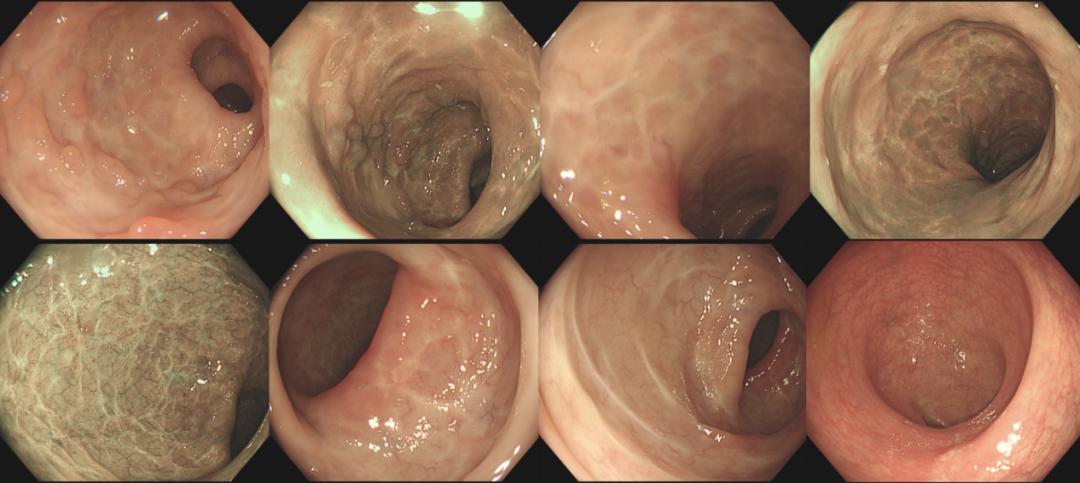
图7 2022年7月4日肠镜复查
目前完成第八次维得利珠单抗输注,无任何不适主诉。
案
例
总
结
该老年患者合并多种基础疾病,糖尿病、LTBI、双侧股骨头无症状坏死,激素治疗存在绝对及相对禁忌,抗肿瘤坏死因子-α(TNF-α)治疗LTBI复发风险较大;既往UC治疗中使用了长期激素灌肠、美沙拉嗪口服联合局部治疗并已优化,但是并不能有效控制病情,导致UC频发、早期复发。最终在生物制剂维得利珠单抗治疗下UC症状得到良好控制,肠镜达成黏膜愈合。
此外,我们在临床筛查中已发现多例UC患者合并无症状股骨头坏死,多伴有骨质疏松,国外文献亦有无激素暴露IBD合并骨坏死案例,早期规范化筛查,早发现及预防可有效避免致残。本病例提示我们,任何时候,在上激素前,都要筛查骨密度、股骨头,且如有相应临床症状,需针对腰椎/外周关节进行筛查。
专家点评
”
徐灿教授
上海市长海医院
UC具有诊断难、治疗难、防复发难、长期管理难等特点,属于消化系统难治性病种[3]。老年UC在临床上并不少见,这些患者通常高龄,合并症多,病情更为复杂[4]。本例患者充分印证了这一点,3年内反复入院治疗,治疗方案为美沙拉嗪口服联合局部治疗,激素灌肠治疗,但效果不理想,UC频频复发。对此,2019年美国胃肠病学会(ACG)指南提出,对于中重度活动性UC患者,可将激素和生物制剂“平行选择”[5]。
然而,回顾患者的病历,其合并的股骨头坏死是激素治疗的绝对禁忌;同时,糖尿病为激素治疗相对禁忌;LTBI还会显著增加激素治疗的风险。此外,长期激素灌肠不能除外激素经结直肠吸收产生系统性副作用风险,故激素不适合本例患者。于是,患者的治疗选择指向生物制剂。而2021年美国胃肠病协会(AGA)老年IBD患者专家共识[6]指出,“老年患者不推荐系统性激素治疗,该类患者中维得利珠单抗及乌司奴单抗应为更加优先的推荐。”
那么,在众多的生物制剂中,维得利珠单抗是如何脱颖而出的?
首先,患者3年来病情反复,在控制症状的同时,要力争降低复发的可能性。既往研究证明,达到持续性症状缓解和内镜黏膜缓解的UC患者,临床复发的风险较低(1年复发风险11.8%)[7]。而维得利珠单抗在临床缓解和黏膜愈合方面,积累了充分的循证医学证据,即使是老年患者,也足够强效。
GEMINI 1研究显示,维得利珠单抗促进UC黏膜愈合的疗效在第6周诱导期即显示出与安慰剂相比的显著优势(40.9% vs 24.8%,P=0.001)[8];VARSITY研究结果证实了维得利珠单抗相比阿达木单抗具有更优的临床缓解和黏膜愈合的疗效(31.3% vs 22.5%和39.7% vs 27.7%,P<0.01)[9]。另一项临床试验数据则表明,维得利珠单抗治疗UC、克罗恩病(CD)患者的有效性在老年患者和年轻患者之间相似[10],提示维得利珠单抗在老年患者中也可获得同样的疗效。
其次,患者合并多种疾病,还存在结核菌潜伏性感染,治疗的安全性格外重要。维得利珠单抗是目前唯一的肠道选择性生物制剂,能够精准靶向作用于肠道,疗效确切且可避免其他系统性生物制剂产生的问题如感染、肿瘤风险增加等[11]。荟萃分析显示,接受抗TNF药物治疗的IBD患者,其结核病风险是对照人群的2到2.5倍[12]。相比之下,维得利珠单抗就更为安全。2017年Gut上的一项研究证实,维得利珠单抗治疗不增加感染和严重感染风险[13]。
种种证据表明,维得利珠单抗是本患者目前的最优选择。实践证明,维得利珠单抗也确实取得了满意的疗效,第一次注射一周内,患者排便逐步减少至每日1次的成型黄色便。治疗近半年后,肠镜下达成黏膜愈合,且多种合并症病情稳定。相信在后续的治疗中,患者会进一步获益,告别反复,自在生活。
”
专家简介

徐灿 教授
上海市长海医院消化内科主任医师、教授
中华医学会消化内镜分会超声内镜学组副组长
中国抗癌协会肿瘤内镜学专委会超声内镜学组副组长
AEG亚洲超声内镜联盟委员
中华医学会消化病学分会幽门螺杆菌学组委员
中华医学会消化病学分会胃肠激素及黏膜屏障学组委员
中华炎症性肠病多学科联合诊治联盟常务委员
中华医学会消化病学分会炎症性肠病学组消化内镜俱乐部委员
中国医师协会内镜医师分会消化内镜专委员会委员
中国医师协会胰腺病专委会青年委员
中国医师协会内镜医师培训学员培训导师
中国声学学会生物医学超声工程分会委员
上海市医学会消化内镜分会青委会副主任委员
上海市医学会炎症性肠病学组委员
中国医学装备协会消化病学分会第一届委员会炎症性肠病学组委员
海峡两岸医卫交流协会消化病学专委会青年委员
参考文献:
[1]Devendra D,et al.World J Gastroenterol.2015,21(12):3644–3649.
[2]Wang YF,et al.J Dig Dis.2010,11(2):76-82
[3]张涛,等.世界中西医结合杂志.2021,16(05):972-976.
[4]陈申旭,马等.当代医学.2021,27(09):42-44.
[5]RubinDT,et al.Am JGastroenterol,2019,114(3):384-413.
[6]Ananthakrishnan AN,et al. Gastroenterology. 2021 Jan;160(1):445-451..
[7]Jangi S, et al. Journal of Crohn's and Colitis, 2021, 15(4): 567-574.
[8]FeaganBG,et al. N Engl J Med. 2013; 369(8): 699-710.
[9]SandsBE, et al. N Engl J Med. 2019; 381(13): 1215-1226.
[10]Ananthakrishnan AN,et al.Gastroenterology.2021;160(1):445-451.
[11]周青杨,钱家鸣.中华消化杂志.2020(02);141-144.
[12]Gut Liver. 2020 Nov 15;14(6):685-698
[13]Colombel JF, et al. Gut. 2017.66(5):839-851.

