两天四款新冠疫苗宣布获批紧急使用,多家企业竞速新冠治疗药物
在疫情防控措施持续优化的同时,多款新冠疫苗获批紧急使用,新冠药物研发也在提速。
12月4日至5日两天,神州细胞(688520)、万泰生物(603392)、三叶草生物(02197.HK)和威斯克生物四家公司宣布新冠疫苗获批紧急使用。12月6日,万泰生物证代向澎湃新闻记者表示,公司已建成的鼻喷新冠疫苗产能为1亿支/年,后续产能要看市场情况。拥有HY3000预防新冠多肽鼻喷药物的翰宇药业(300199)则表示,具体上市时间需要根据临床试验的进度而定,“预计产量基本上可以满足市场需求。”
12月6日,新冠防治概念跌幅靠前,疫苗股下挫,截至收盘,康希诺(688185)跌3.25%,报180.80元/股;万泰生物(603392)跌8.20%,报137.45元/股;神州细胞(688520)跌8.40%,报68.15元/股;康泰生物(300601)微跌0.23%,报34.08元/股;沃森生物(300142)跌0.56%,报39.21元/股。港股方面,三叶草生物(02197.HK)跌9.69%,报4.1港元/股;康希诺生物(06185.HK)跌5.82%,报82.6港元/股。
新冠特效药概念股同样低迷,截至收盘,拓新药业(301089)跌2.55%,报75.61元/股;翰宇药业(300199)跌5.65%,报17.55元/股;众生药业(002317)跌5.62%,报28.69元/股;长江健康(002435)跌5.42%,报5.24元/股;复星医药(600196)跌4.45%,报34.81元/股。
两天四款新冠疫苗宣布获批紧急使用
11月11日,国务院应对新型冠状病毒肺炎疫情联防联控机制综合组发布了《关于进一步优化新冠肺炎疫情防控措施 科学精准做好防控工作的通知》。其中提及“有序推进新冠病毒疫苗接种。加快开展具有广谱保护作用的单价或多价疫苗研发,依法依规推进审批”。
据证券时报报道,随着前述四款新冠疫苗获批紧急使用,国内已经有13款新冠疫苗获得国家药监局批准附条件上市或纳入紧急使用。
万泰生物鼻喷新冠疫苗 厦门大学官网 图
12月5日,万泰生物发布公告称,其与厦门大学、香港大学合作研发的鼻喷流感病毒载体新冠肺炎疫苗经国家卫健委提出建议,国家药监局组织论证同意紧急使用。万泰生物称,这是国内首款鼻喷新冠肺炎疫苗获批紧急使用,也是全球最早进入临床试验以及迄今唯一在三期临床试验中验证了安全性和广谱有效性的黏膜免疫新冠疫苗。
12月6日,澎湃新闻记者以投资者身份询问万泰生物鼻喷新冠疫苗年产能情况,万泰生物证代表示,公司已建成的鼻喷新冠疫苗产能为1亿支/年,另外鼻喷疫苗产业基地建设项目是公司非公开发行股票的募投项目之一,产能规模为2.4亿支/年。
“后续产能如何还要看市场情况,我们与康希诺是不同的技术路径,从各项数据来看,我们的疫苗在安全性等各方面还是很有保障的,60岁以上人群保护率不低于中青年群体。”该人士说。

三叶草生物官网 图
三叶草生物是一家处于临床试验阶段的全球生物制药公司,致力于开发新型疫苗和生物疗法。
三叶草生物方面向澎湃新闻记者表示,其公司新冠疫苗SCB-2019(CpG1018/铝佐剂)经国家有关部门评估后被纳入紧急使用。数据显示,相较于安慰剂受试者,接种SCB-2019新冠疫苗能降低新冠病毒在家庭成员中的传播风险。
三叶草生物并未披露疫苗的具体产能情况,从公司官网来看,三叶草生物拥有两个生产基地,分别为长兴商业化生产基地和成都中试生产基地。另据其去年披露的招股书显示,三叶草生物的潜在最大产能能够每年自主生产超过10亿剂SCB-2019。

神州细胞官网 图
神州细胞专注于单克隆抗体、重组蛋白、疫苗等生物药产品的研发和产业化。其在12月4日晚间公告,公司自主研发的重组新冠病毒2价(Alpha/Beta 变异株)S三聚体蛋白疫苗(项目代号:SCTV01C)被纳入紧急使用。神州细胞的半年报披露,公司已对该疫苗的研发投入1.5亿元。
12月3日晚,北京发布微信公众号发布了《北京经开区4项举措统筹疫情防控和经济社会发展》,其中提到,神州细胞疫苗已经获批紧急使用,正在加快组织生产。不过,该消息并未指出具体的疫苗品种。
神州细胞公告称,SCTV01C仍在临床研究阶段。“虽然 SCTV01C被纳入紧急使用,其未来的市场销售仍将面临较为激烈的竞争态势,并同时受国内外疫情的发展变化、新冠疫苗接种率、公司生产能力等多种因素影响,后续商业化前景仍存在不确定性。”神州细胞方面称。
值得关注的是,除上述三家上市公司新冠疫苗获批紧急使用外,威斯克生物/川大华西研发的重组新型冠状病毒疫苗(Sf9细胞)威克欣也纳入紧急使用,这也是中国首个获批紧急使用的昆虫细胞技术平台生产的重组蛋白新型冠状病毒疫苗。

威斯克生物官网 图
官网信息显示,威斯克生物是一家集疫苗研发、生产和销售于一体的创新型生物医药企业,除此次紧急获批的产品外,还在同步开展鼻喷重组变异新型冠状病毒疫苗(Sf9细胞) 、新型口服抗新冠病毒药物、mRNA新冠疫苗的研发。目前试验结果显示三款产品均具有良好的体内安全性和体内活性。
一位疫苗从业人士告诉澎湃新闻记者,新冠疫苗纳入紧急使用并不代表它能取代正式的审评审批程序。参照行业既往经验,企业从取得紧急使用批件到推向市场供基层使用,中间还需要经过相关政府机构的指导和准入流程。“比如,制定价格,进入疾控信息系统、如何接种、招标采购等这些都需要时间。”该人士说。
根据《中华人民共和国疫苗管理法》第二十条规定,出现特别重大突发公共卫生事件或者其他严重威胁公众健康的紧急事件,国务院卫生健康主管部门根据传染病预防、控制需要提出紧急使用疫苗的建议,经国务院药品监督管理部门组织论证同意后可以在一定范围和期限内紧急使用。
多家药企推动新冠疫苗上市进程
除前文所述获批紧急使用的新冠疫苗外,康希诺生物的(688185.SH)吸入用重组新型冠状病毒疫苗也正在全国推进。自10月26日,上海启动吸入式新冠疫苗后,北京、天津、江苏、浙江和海南等地也陆续将吸入式新冠疫苗面向全人群接种。
产能方面,康希诺在11月25日发布的公告中提及,公司研发生产的吸入用重组新型冠状病毒疫苗克威莎®雾优®作为加强针被纳入紧急使用后,目前达到每天产能150万人份,潜在最大运力达每天100万人份,具体发运的执行以国家及各地疾控的指令为准。
在投资者互动平台上,康希诺方面表示,根据公司吸入用新冠疫苗的产品说明书,0.5mL/瓶产品为3次人用剂量;1.5mL/瓶产品为14次人用剂量。截至11月18日,吸入用新冠疫苗已公开的接种点数量超过1000个,目前吸入用新冠疫苗的商业化进程正在推进。
康泰生物(300601.SZ)公告显示,在国内已有5款新冠疫苗产品获得附条件批准上市,有4款获得紧急使用批准,有3款被列入世界卫生组织的紧急使用清单。11月18日,康泰生物公告称,其研发的新型冠状病毒灭活疫苗(Vero细胞)已完成III期临床试验的关键性数据分析。该产品于2021年5月在国内被纳入紧急使用。
康泰生物在公告中解释,根据国家关于疫苗注册管理的相关规定,新型冠状病毒灭活疫苗在完成Ⅲ期临床研究工作后,还需经过综合审评、生产现场核查等程序,后续该疫苗申请新药上市及药品审评审批的进度及结果等因素具有一定的不确定性。
12月1日,沃森生物(300142.SZ)在投资者问答平台称,该公司与艾博生物合作研发的新冠mRNA疫苗III期临床试验数据整理及统计分析工作持续进行中,公司将根据国家监管部门的规定和要求,积极推动相关新冠疫苗的上市进程。
国信证券在研报中指出,参考发达国家加强针政策推进历程,我国大体沿着“老年人/高危人群→成人→儿童及青少年”三类人群逐步推进,国内各年龄组人群接种率仍有上升空间。近期,多款国产新冠疫苗取得临床/审批进展,建议关注新冠疫苗加强针推广和在研管线进展。
开源证券则指出精准防控新形势下,医疗消费有望迎来行业复苏。开源证券认为,2022年医药行业受疫情扰动严重,消费医疗、医疗服务、中药表现受损,在政策边际向好的情况下,2023年有望迎来复苏行情。
不过也有分析人士认为,从部分企业产业线看,商业化产品较少,若未在加强免疫上获批,市场份额可能并不乐观。
新冠治疗药物研发加速
不只是新冠疫苗,新冠治疗药物的研发进度也在提速。西南证券12月5日发布的研报显示,全球5款新冠口服药获批上市,10款药物处于临床Ⅲ期(包括老药新用和Ⅱ/Ⅲ期,其中2款药物获得EUA)。
从国内市场来看,辉瑞新冠口服药Paxlovid(奈玛特韦片/利托那韦片)今年2月获批在中国上市,随后真实生物的阿兹夫定于7月获批上市,成为首款获批的国产新冠口服药。此外,默沙东Molnupiravir已递交NDA,君实生物(688180.SH)的口服核苷类抗SARS-CoV-2药物VV116(JT001)、开拓药业(9939.HK)的普克鲁胺、先声药业(2096.HK)的新冠小分子药物SIM0417等正在开展Ⅲ期临床试验。
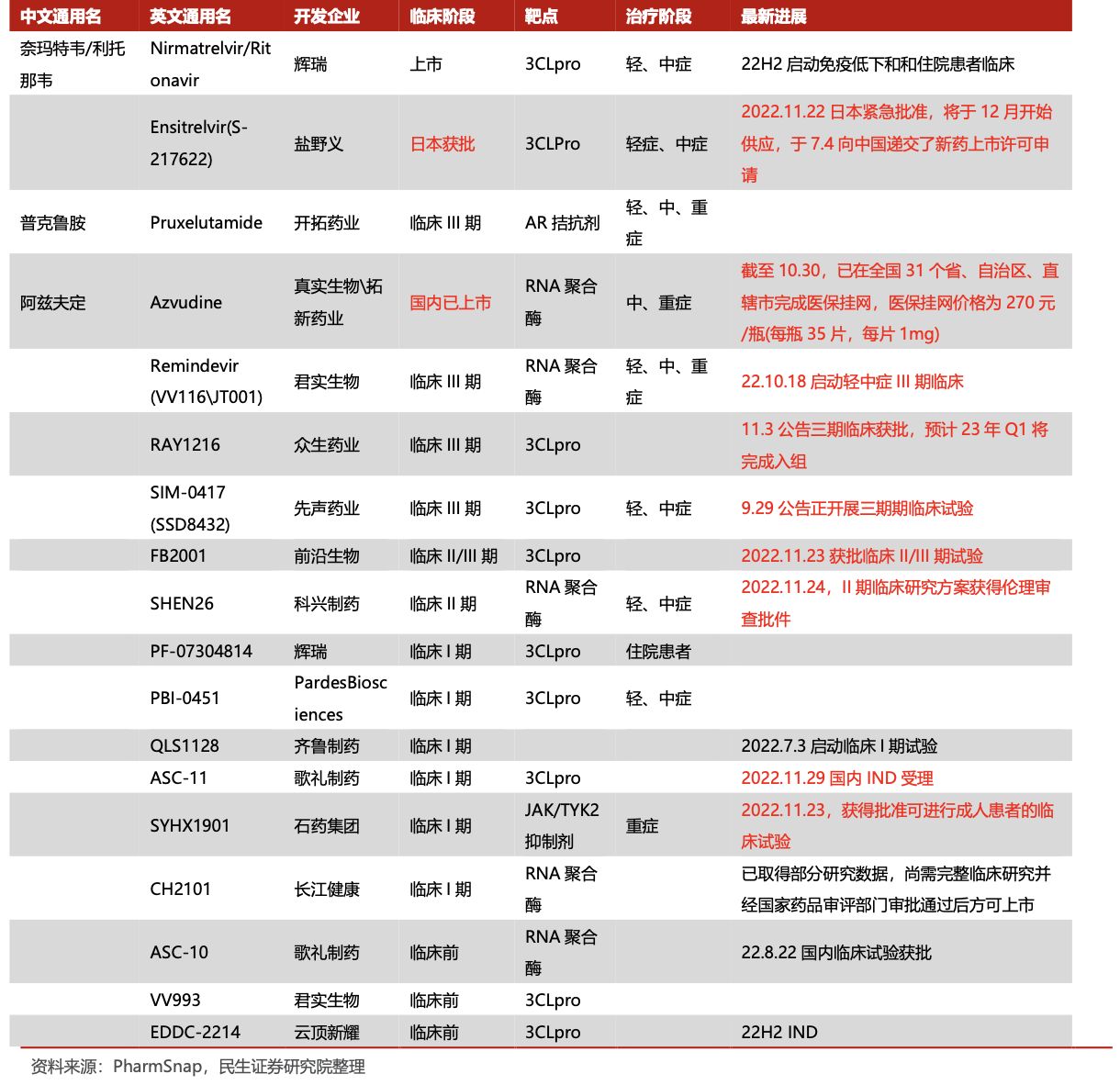
来源:民生证券11月14日研报
随着防疫政策的优化,针对新冠病毒的雾化吸入剂、小分子口服药也迎来新进展,多家公司先后拿下临床试验批文。
11月30日,悦康药业(688658.SH)宣布其广谱冠状病毒膜融合抑制剂多肽药物( YKYYO17雾化吸入剂)获得国家药品监督管理局临床试验批准,该产品的申请适应症为治疗新型冠状病毒感染。悦康药业介绍,多肽药物吸入制剂是创新型高端制剂,通过吸入肺部递送的方式实现多肽药物的高效利用,使得多肽类药物发挥全身疗效,具有广阔的应用前景。该公司半年报显示,截至2022年6月,悦康药业已累计为此产品的研发投入约1904万元。
同日,华润双鹤(600062.SH)公告称,全资孙公司北京双鹤润创科技有限公司收到了国家药监局颁发的CX2101A《药物临床试验批准通知书》,批准该药品开展用于治疗新型冠状病毒肺炎的临床试验。CX2101A是作用于新冠病毒RdRp(RNA依赖性RNA聚合酶)的小分子化合物,使用最新一代前药技术BEPro。前期研究发现该技术能够有效改善药物口服利用度和药代动力学特性,未来可以此为核心技术进一步开发新的抗病毒和抗肿瘤产品。
11月29日,歌礼制药(1672.HK)在港交所公告称,新冠口服候选药物蛋白酶(3CLpro)抑制剂ASC11新药临床试验申请已获国家药监局受理。歌礼制药介绍,ASC11是利用包括分子模拟对接在内的多种专有技术自主研发的口服小分子候选药物。
此外,新冠预防用药也受到关注,近期多家公司获批临床,为上市进行准备。
12月5日,翰宇药业(300199.SZ)公众号发布消息称,抗新冠广谱预防多肽药物HY3000鼻喷雾剂Ⅱ期临床试验正式启动。同日,翰宇药业在投资者问答平台称,公司会与临床牵头单位南方医科大学珠江医院,以及分中心南方医科大学南方医院、中山大学孙逸仙纪念医院一起快速推动,力争HY3000鼻喷雾剂早日上市。
12月6日中午,澎湃新闻记者以投资者身份询问翰宇药业相关产品的进展情况。对方表示,HY3000鼻喷雾剂的具体上市时间需要根据临床试验的进度而定。生产方面,“公司除了自建生产线,还与外部合作商签订排产计划,预计产量基本上可以满足市场需求”。对方还表示,HY3000鼻喷雾剂的Ⅱ期临床试验完成后,可以申请紧急上市,但最终结果仍视药监局是否审批而定。
11月28日,中国生物(1177.HK)宣布,其重组全人源抗新冠病毒单克隆抗体鼻用喷雾剂(F61鼻用喷雾剂)于11月25日获得国家药品监督管理局临床试验批件,用于新冠病毒高暴露风险人群的预防。据该公司介绍,F61鼻用喷雾剂对新冠病毒各变异株均具有广谱及高中和活性,可直接作用于鼻咽部上呼吸道局部,在鼻粘膜上形成一道保护膜。新冠病毒入侵时,这层保护膜可阻止其与宿主细胞结合,特异性阻断新冠病毒入侵。
