新型分子标记物实现可预测的帕金森病细胞治疗结果,已签技术转让协议
据中科院脑科学与智能技术卓越创新中心微信公众号消息,6月15日,《The Journal of Clinical Investigation》期刊在线发表了题为《人类中脑多巴胺能神经细胞分化标志物预测帕金森病细胞治疗结果》的研究论文。
在该研究中,科学家们解析了中脑多巴胺能神经分化的单细胞转录组图谱,发现了中脑多巴胺能神经祖细胞的特异性表面蛋白分子,并且应用它们来获得高纯度的目的供体细胞,实现稳定且可预测的帕金森病细胞治疗结果。
该研究由中国科学院脑科学与智能技术卓越创新中心(神经科学研究所)、灵长类神经生物学重点实验室、上海脑科学与类脑研究中心陈跃军研究组完成。

全球疾病负担(Global Burden of Disease)的统计数据显示,预计 2030 年全球将有约930万 帕金森病(Parkinson’s Disease,PD)患者,其中中国约有494万。帕金森病给患者自身带来极大痛苦,也给家庭和社会造成沉重负担。帕金森病主要是源于中脑黑质致密部多巴胺能神经元的退行性病变和丢失,造成了纹状体多巴胺含量显著性减少,从而引起肌张力增高、运动迟缓、静止性震颤、和步态异常等运动功能障碍。临床上尚无治愈帕金森病的有效方案,目前的治疗方法主要是对症治疗,包括以左旋多巴为代表的药物治疗和深部脑刺激。然而药物治疗只在早期阶段有效,而脑深部刺激只适用于部分病人,随访成本高,且会引起抑郁症等副作用,因此急需开发新的治疗策略和方法。
细胞替代疗法(细胞治疗)被认为是有前景的PD治疗策略。细胞治疗通过移植外源神经细胞补充丢失的多巴胺能神经元,进而恢复脑内多巴胺释放水平,解救患者运动功能障碍。人多能干细胞,包括人胚胎干细胞和人诱导多能干细胞,可以通过体外分化产生可移植的中脑多巴胺能神经祖细胞,为细胞治疗提供了大量的可再生的细胞资源。目前包括中,美,日,澳在内的很多国家相继开展了基于人多能干细胞技术的PD细胞治疗临床试验,然而仍然有很多问题需要解决。(1)体外分化得到的移植用供体细胞(donor cells)存在高度异质性;(2)供体细胞移植后,脑内移植物中的目标神经元(多巴胺能神经元)的比例通常较低(不超过10%);(3)移植物的细胞组成未知。因此,如何获得标准化的神经细胞产品,以确保移植后稳定且可预测的治疗效果,仍然是帕金森病细胞治疗在临床上更广泛和更安全应用面临的主要挑战。
为了解决上述问题,研究者们首先绘制了人多能干细胞向中脑多巴胺能神经细胞分化的单细胞转录组图谱,发现多巴胺能神经细胞的体外分化过程模拟了多个但相邻的人胎脑区域的发育过程,包括腹侧中脑、中脑-后脑边界(MHB,也称为峡部)和腹侧后脑,其中只有部分腹侧中脑细胞可以进一步分化为中脑多巴胺能神经元,而其它脑区的细胞则主要分化为GABA能神经元、谷氨酸能神经元、运动神经元和5-羟色胺能神经元。这一结果解释了人多能干细胞向中脑多巴胺能神经细胞分化产生异质性细胞类群的原因。
研究者进一步重建了人中脑多巴胺能神经细胞的分化轨迹,发现了代表早期或晚期多巴胺能神经祖细胞的特异性表面蛋白分子,CLSTN2和PTPRO,并且这些表面蛋白分子可以用来预测体外分化得到的异质性神经祖细胞群终末分化为中脑多巴胺能神经元的效率(图1A)。研究者从异质性神经祖细胞群中分选富集了分别表达这些表面分子蛋白的神经祖细胞,并移植到PD模型小鼠脑内,发现分选的神经祖细胞移植后可产生高度富集的中脑多巴胺能神经元,比例可高达 80%,其中大部分(约90%)的多巴能神经元为黑质中脑多巴胺能神经元亚型-PD 患者脑内主要缺失的多巴胺能神经元亚型。移植物中的多巴胺能神经元可以整合到宿主环路并特异性支配宿主的背侧纹状体。进一步的研究发现,与未分选组相比,分选组的多巴胺能神经细胞具有更高的治疗效力,表现为对宿主纹状体更强的多巴胺能神经支配和只需要移植少量细胞(常规治疗细胞剂量的10%)就可以达到治疗效果(图1B)。
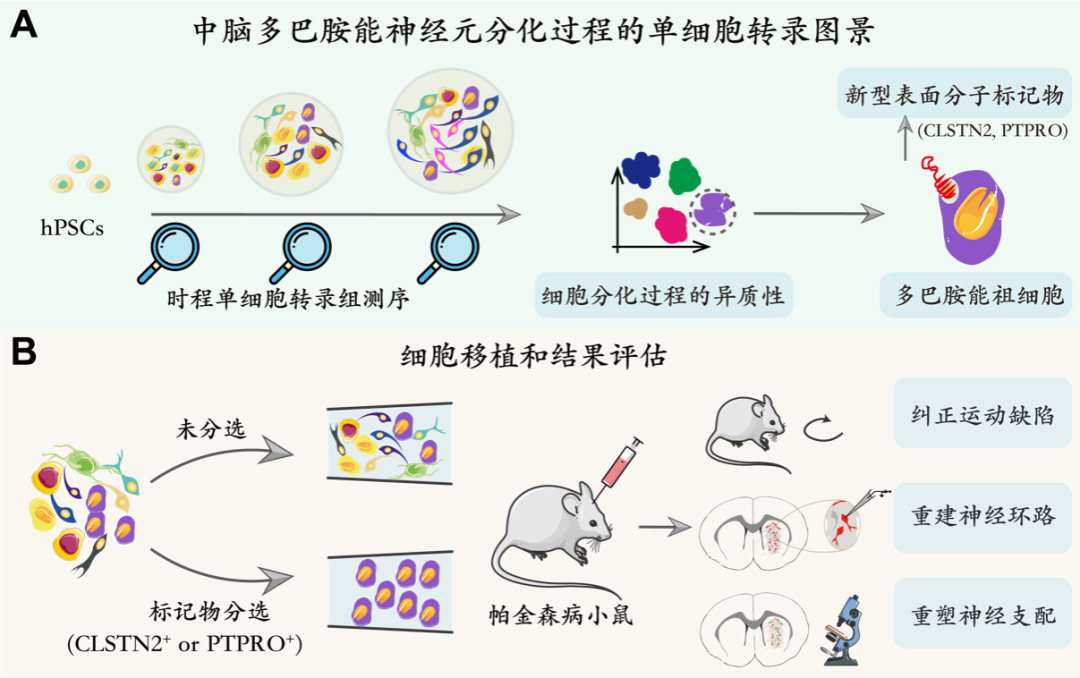
图1 |(A)通过对人类中脑多巴胺能体外分化过程进行时程单细胞转录组,解析了培养物的细胞类型异质性,并找到新型多巴胺能祖细胞的表面分子标记物。(B)将未分选的神经祖细胞与标记物分选的神经祖细胞(CLSTN2+ 或 PTPRO+)移植到帕金森病小鼠模型中,通过行为学、电生理、组织学染色等手段评估移植结果。(C)通过解剖帕金森病小鼠脑中的移植物并进行单细胞转录组的分析,发现新型标记物后的移植物具有稳定可预测的移植物结果,目标神经元(即中脑多巴胺能神经元)高度富集,非目标神经元大部分被剔除。
同时对移植物进行单细胞测序分析发现,未分选组的移植物中中脑多巴胺能神经元比例低,且含有多种类型的非目的神经元,其中包括明确能够造成副作用的五-羟色胺能神经元。而分选组中中脑多巴胺能神经元被高度富集,非目标神经元类型大多被剔除(图2A)。同时,不同分子标记物分选的移植物具有高度一致的神经元组成(图2B),提示移植高度富集的多巴胺能神经祖细胞可以获得稳定且可预测的移植结果。
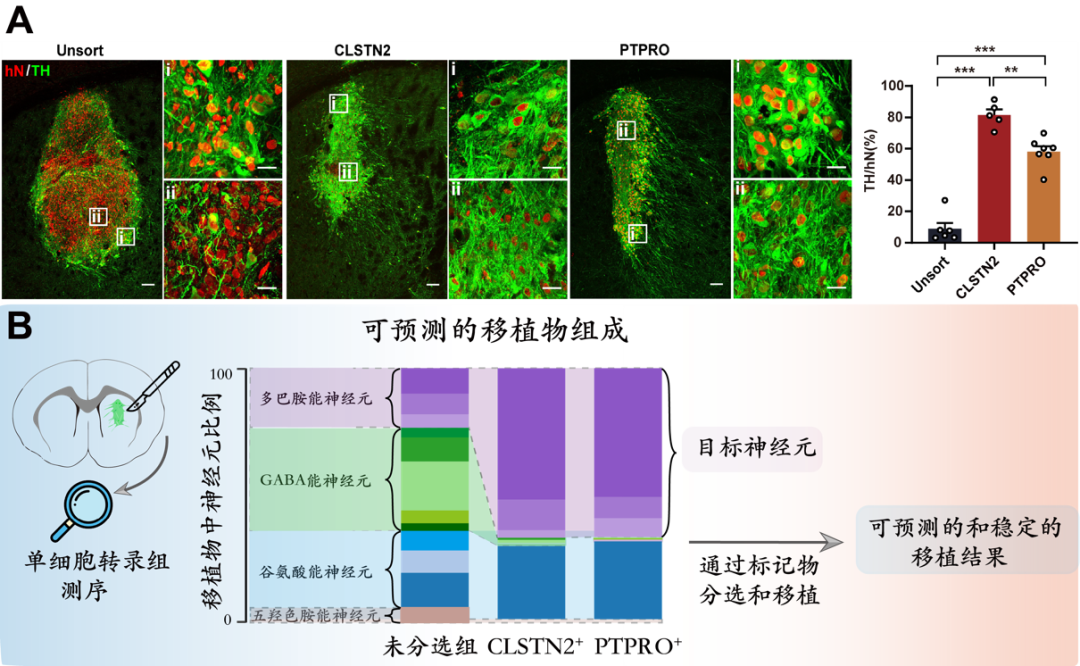
图2 |(A)未分选的祖细胞,CLSTN2+ 祖细胞和 PTPRO+ 祖细胞衍生的移植物,用人源细胞核(hN)和多巴胺能神经元标记物 TH 免疫染色的典型图以及移植物中 TH+ 神经元比例的量化。比例尺,100μm。(B)通过解剖帕金森病小鼠脑中的移植物并进行单细胞转录组的分析,发现新型标记物后的移植物具有稳定可预测的移植物结果,目标神经元(即中脑多巴胺能神经元)高度富集,非目标神经元大部分被剔除。
该研究绘制的体外分化和体内移植物的单细胞转录组图谱为中脑多巴胺能神经细胞分化过程中细胞异质性的产生和移植物中非目标细胞的来源提供了更全面的理解。同时研究者建立了一种获得高度纯化的供体细胞的方法,这些供体细胞移植后可以获得稳定且可预测的细胞治疗结果。这一研究为实现更有效更安全的帕金森病细胞替代疗法迈出了重要的一步。
该研究由脑智卓越中心博士研究生许培博、博士研究生何慧与博士后高琴琴在陈跃军研究员指导下完成,周盈盈、吴子彦、张晓、孙琳钰、胡港、管倩、游致文、章馨月、郑文平和复旦大学脑科学研究院熊曼研究员为本研究提供了重要帮助,斯坦福大学Aaron Gitler教授和脑智中心梁智锋研究员对论文修改给与了宝贵建议。该研究得到科技部、中科院、上海市、基金委的支持。该成果已申请知识产权保护,并与第三方公司签署里程碑付款模式的技术转让协议,协议总金额超过4000万元人民币。
