《自然》:是谁定下了胰岛素敏感度的生物钟?
原创 图图 神经现实 收录于话题#神经前研 | NeuroHub141个
 文献:Ding, G., Li, X., Hou, X. et al. REV-ERB in GABAergic neurons controls diurnal hepatic insulin sensitivity. Nature (2021).
文献:Ding, G., Li, X., Hou, X. et al. REV-ERB in GABAergic neurons controls diurnal hepatic insulin sensitivity. Nature (2021).DOI:https://doi.org/10.1038/s41586-021-03358-w
导读作者:图图| 封面:Lorenza Cotellessa
“生物钟”,想必大家已经很熟悉了吧,我们日出而作日入而息,猫主子们到了早上七八点就跳到床上蹭蹭你的脸,意思是“到时间了,铲屎的,快给主子我奉上新鲜的早餐”,这些都依赖着我们身体自带的生物钟。我们通过它去感受外界环境的周期性变化,并调节自身生理内在新陈代谢等节律,从而更好地适应地球生活。那么,作为新陈代谢的主要器官——肝脏,他的律动自然也是被昼夜变化的鼓点强烈控制,规律有效地调节我们的糖代谢来补充机能。
通常,觉醒状态下,我们肝脏对胰岛素更为敏感(在刚刚觉醒时达到顶峰)。肝细胞更容易感知胰岛素(糖耐量高),对肝脏糖异生的抑制作用较强,从而更好地面对即将发生的吃吃喝喝。而在夜间睡眠期间,我们无法从外界通过进食获取糖和能量,此时肝细胞则会减弱对胰岛素的应答(糖耐量低),增加糖原异生保持血糖含量稳定,避免机体在睡梦中出现低血糖的现象。
然而,如果身体对胰岛素的应答出现异常,例如在部分2型糖尿病患者中都发现了“黎明现象”(extended dawn phenomenon)——在夜间或白天大部分时间内血糖控制还算平稳,但在黎明甚至之后的时间段中即使空腹也会呈现高血糖。这很有可能说明患者身体中胰岛素敏感的昼夜节律调节发生紊乱,肝脏无法在合适地时间发挥合适地功能。那么,这种胰岛素敏感度的昼夜节律又是如何形成的呢?是否可以通过人为调节这种节律来控制糖尿病患者的血糖呢?
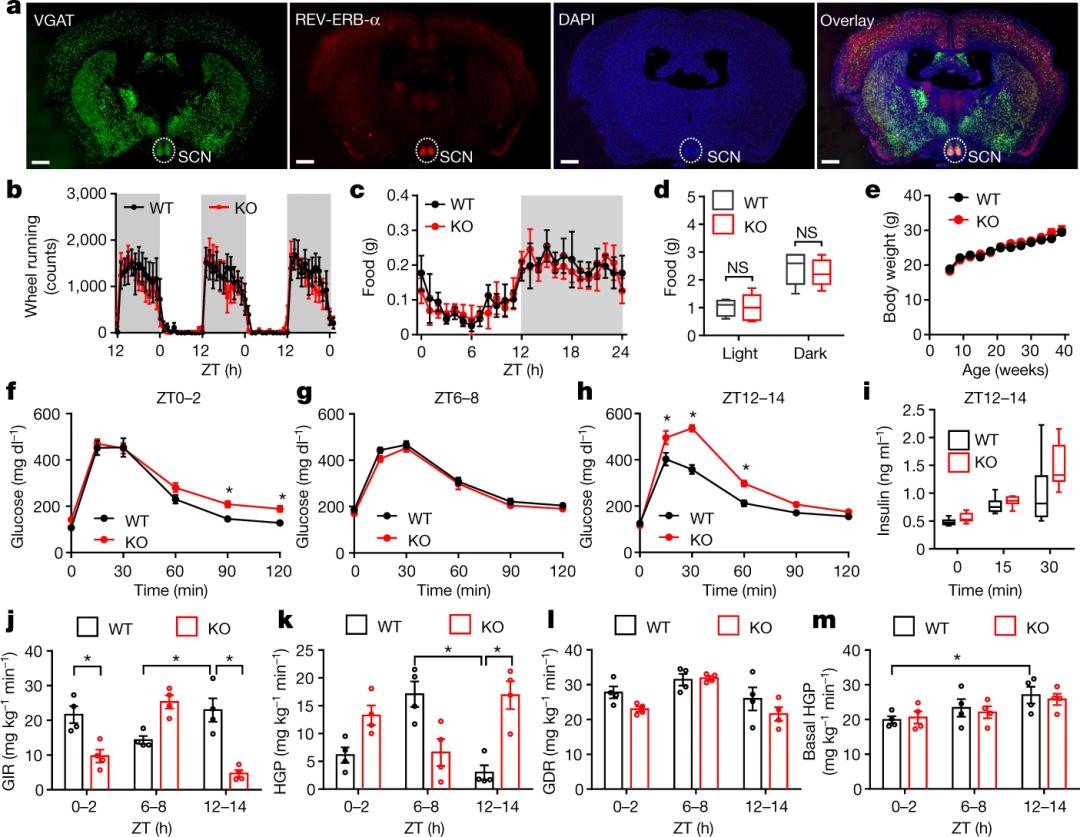
 近日,美国贝勒医学院孙正教授和山东大学齐鲁医院陈丽教授团队合作揭示了:下丘脑视交叉上核(suprachiasmatic nucleus,SCN)区GABA神经元(SCNGABA neuron)的REV-ERB基因可以控制胰岛素抑制肝脏糖异生的昼夜节律。之前已有报道指出REV-ERB-α和REV-ERB-β属于核受体家族(统称REV-ERB),它们可以通过直接结合到基因的启动子处调节基因的表达,是重要的生物节律调节药物靶点。研究人员发现,REV-ERB-α主要富集于SCN(主要是由GABA能神经元组成),并且REV-ERB-α和REV-ERB-β都表现出强烈的昼夜节律,会在环境钟6-9时(Zeitgeber time(ZT)6–9)达到顶峰(ZT0代表熄灯,ZT12代表灯亮),所以他们想知道REV-ERB-α和REV-ERB-β在SCNGABA神经元中到底扮演着什么角色。
近日,美国贝勒医学院孙正教授和山东大学齐鲁医院陈丽教授团队合作揭示了:下丘脑视交叉上核(suprachiasmatic nucleus,SCN)区GABA神经元(SCNGABA neuron)的REV-ERB基因可以控制胰岛素抑制肝脏糖异生的昼夜节律。之前已有报道指出REV-ERB-α和REV-ERB-β属于核受体家族(统称REV-ERB),它们可以通过直接结合到基因的启动子处调节基因的表达,是重要的生物节律调节药物靶点。研究人员发现,REV-ERB-α主要富集于SCN(主要是由GABA能神经元组成),并且REV-ERB-α和REV-ERB-β都表现出强烈的昼夜节律,会在环境钟6-9时(Zeitgeber time(ZT)6–9)达到顶峰(ZT0代表熄灯,ZT12代表灯亮),所以他们想知道REV-ERB-α和REV-ERB-β在SCNGABA神经元中到底扮演着什么角色。研究人员发现特异性敲除REV-ERB-α和REV-ERB-β在GABA能神经元的表达(knockout mice),这些小鼠虽然没有出现异常的发育或节律运动/进食等,但是由他们生物钟决定的糖代谢却不然,在ZT0–2和ZT12–14中都出现了一定程度的糖耐量损伤。鉴于注射葡萄糖后,小鼠血液中会呈现正常程度的胰岛素水平增加,说明之前观察到的糖代谢异常很有可能来自于对胰岛素的敏感度而非产量受损。接着,胰岛素-葡萄糖钳夹结果显示knockout小鼠在ZT0–2和ZT12–14主要由于高水平糖异生导致葡萄糖输注率(glucose infusion rate)明显减少,对照组小鼠则在系统性胰岛素敏感度、胰岛素抑制肝糖生成的敏感性和基本肝脏生糖方面都表现出非常显著的昼夜节律,都会在觉醒时刻(ZT12–14)达到巅峰。这暗示着REV-ERB对胰岛素抑制肝糖生成的敏感性的节律调节非常重要。
 - Ding et al., Nature -
- Ding et al., Nature -那么具体REV-ERB是如何影响肝糖生成的敏感性的节律呢?研究人员发现,对照组中SCNGABA神经元的放电活动与之前观察到的糖代谢节律一致,而正常情况中ZT12–14时本应“休息”的神经元在knockout小鼠却中异常活跃,主要与增强的兴奋性突触后电流(mEPSC)的振幅有关。更进一步,他们用RNA-seq分析了各基因表达在ZT12–14的变化,发现主要是编码与神经递质有关的细胞表面蛋白的基因表达发生了改变,例如Rgs16和一些Takusan家族基因。这些基因均可被REV-ERB调控,所以他们表达水平的时间分布与REV-ERB也非常一致,而在knockout小鼠中这些基因的节律表达则受到明显的扰乱。
但是SCNGABA神经元活动为何可以调控肝脏糖代谢呢?研究人员人为激活SCNGABA神经元会使小鼠的糖耐量大打折扣,也就是说SCNGABA神经元过度活跃,小鼠即使处于觉醒状态也会葡糖糖不耐受。当然反之,抑制SCNGABA神经元则会极大程度地提升糖耐量,这也是为什么正常小鼠在ZT12–14觉醒时间段SCNGABA神经元较低,促进糖耐量升高,进入“嗷嗷待哺”状态。
有意思的是,研究人员在knockout小鼠SCNGABA神经元中诱导了外源REV-ERB的节律性表达,控制诱导表达的时间从而控制外源REV-ERB的节律。如果与内源节律一样,小鼠在觉醒期的糖耐量有显著增高,能有效改善小鼠的糖代谢异常,反之则未见奇效。这说明REV-ERB在SCNGABA神经元中的表达节律对小鼠糖代谢调节至关重要。那么,这个现象是否可以解释糖尿病患者的“黎明现象”呢?随后,研究者们监测并分析了2型糖尿病患者们的外周血淋巴细胞,发现有黎明现象组和无黎明现象组中,REV-ERB及多个与生物钟有关的基因的表达模式都存在显著差异,这无疑说明了那些有“黎明现象”的糖尿病患者很有可能是因为体内激素感知及调节的生物钟紊乱而导致糖代谢异常。
总的来说,该研究详细地剖析了胰岛素敏感性节律的神经调控和分子机制,为2型糖尿病患者出现的黎明现象提出了新的理解,给将来临床的治疗开辟了新的道路。
原标题:《《自然》:是谁定下了胰岛素敏感度的生物钟?》

