原创 庄文卓 细胞世界
蛋白糖基化指的是糖分子与蛋白质分子结合的过程,是一种生物化学过程。这个过程在细胞中广泛发生,对于维持生物体的正常功能和调节细胞内信号传导具有重要作用。
具体来说,蛋白糖基化是一种非常重要的蛋白质后修饰方式。在这种修饰中,糖基通过酶的催化与蛋白质上的某些残基形成共价连接——通常是糖苷键。糖基化可以通过多种方式与蛋白质相连,如N-糖基化、O-糖基化、C-糖基化等。糖基化对蛋白质的理化性质和生物功能都可以产生重大影响,单糖和糖链结构的多样性又很适合作为标签,所以糖基化在生物体中很普遍。在所有的已知蛋白质中,约有50%是被糖基化的,而人类基因组中至少1%的基因参与聚糖生物合成。
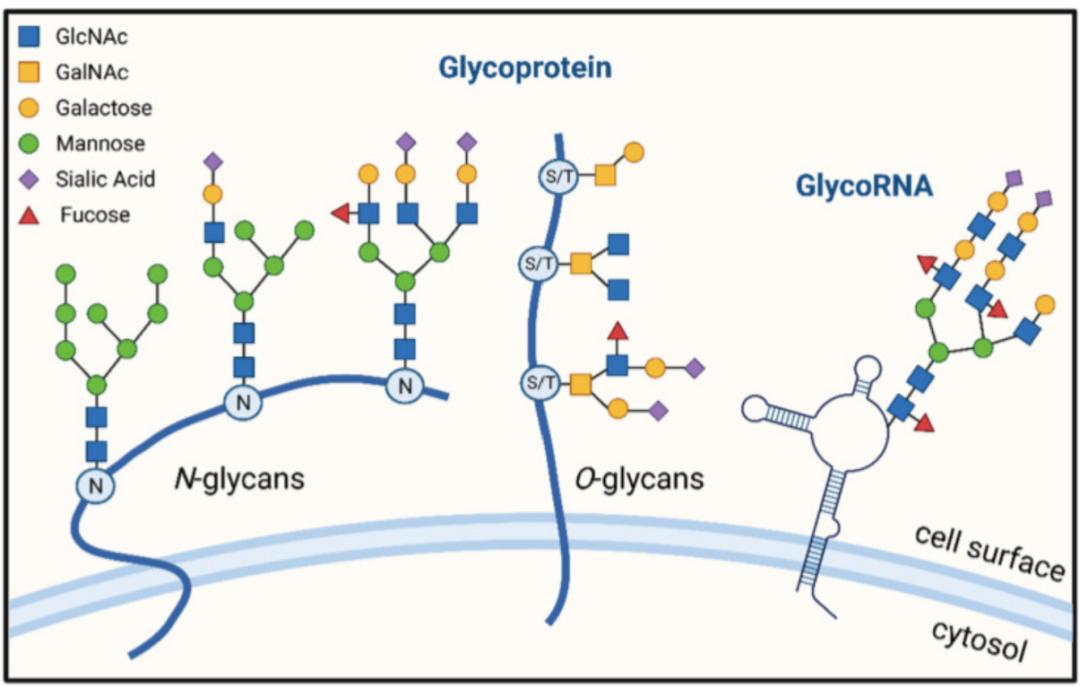
蛋白糖基化的分类
01
蛋白糖基化的角色意义
在许多重要的生物学过程中,蛋白糖基化都扮演着关键角色。例如:
细胞信号传导调节 一些细胞信号分子(如生长因子、激素等)与蛋白质结合时可能会发生糖基化,这会影响它们在细胞内的传递和作用。这种糖基化修饰可以改变蛋白质的活性、稳定性和降解速率,从而调节细胞的功能和代谢。
细胞黏附和识别 在细胞黏附和识别过程中,蛋白糖基化起着重要作用。细胞表面的糖基化蛋白可以与其他细胞或基质中的分子结合,介导细胞间相互作用和信号传递,这对细胞的黏附、迁移和发育过程至关重要。
蛋白质稳定性和功能 蛋白糖基化还可以影响蛋白质的稳定性和功能。糖基化修饰可以改变蛋白质的折叠状态、降解速率和与其他分子的相互作用,从而调节蛋白质的功能和寿命。

糖基化改变对癌症进展、细胞粘附和转移的影响
02
糖基化与炎症性疾病
促炎细胞因子(如肿瘤坏死因子TNF-α、白细胞介素IL-1β等)在炎症过程中发挥着重要作用,它们可以激活多种炎症信号通路,包括NF-κB(核因子-κB)和MAPK(丝裂原激活蛋白激酶)等途径。这些信号通路的激活促进了炎症性反应,并导致炎症细胞的活化和炎症因子的释放。
在炎症性疾病中,促炎细胞因子的存在可能会影响糖苷酶和糖基转移酶的表达。这些酶类的活性和表达水平可以调节黏蛋白的糖基化程度,从而影响细胞表面的黏附分子、信号传导受体等的糖基化水平。这种糖基化修饰的改变可能影响细胞信号传导途径,特别是NF-κB和MAPK信号通路的活性,进而调节炎症的程度和持续性。
通过调节糖基化水平,促炎细胞因子可能影响细胞信号转导的复杂网络,加剧或减轻炎症反应。这一过程在炎症性疾病的病理生理过程中具有一定的重要性。

炎症过程中N-糖基化途径:先天免疫反应的潜在调控机制
03
糖基化与肿瘤
PD-1和PD-L1是肿瘤免疫治疗中的重要靶点。
其中,PD-1是一种膜表面受体,主要表达在T细胞、B细胞和NK细胞等免疫细胞上,可以通过与PD-L1和PD-L2等配体结合,抑制T细胞的活化和增殖,从而发挥免疫抑制作用;PD-L1是一种膜表面分子,主要表达在肿瘤细胞、免疫细胞和非免疫细胞等多种细胞上,可以通过与PD-1结合,抑制T细胞的活化和增殖,从而发挥免疫逃逸作用。
研究表明,PD-L1的糖基化修饰可以影响其与PD-1的结合亲和力,从而影响PD-1/PD-L1信号通路的激活和免疫逃逸的发生。例如,PD-L1的N-糖基化修饰可以增强其与PD-1的结合亲和力,从而增强PD-1/PD-L1信号通路的免疫抑制作用。此外,PD-L1的糖基化修饰还可以影响其在肿瘤细胞中的表达和稳定性,从而影响肿瘤细胞的免疫逃逸和PD-1/PD-L1抗体治疗的疗效。
目前,糖基化修饰对PD-1/PD-L1信号通路的调控机制还需要进一步的研究。
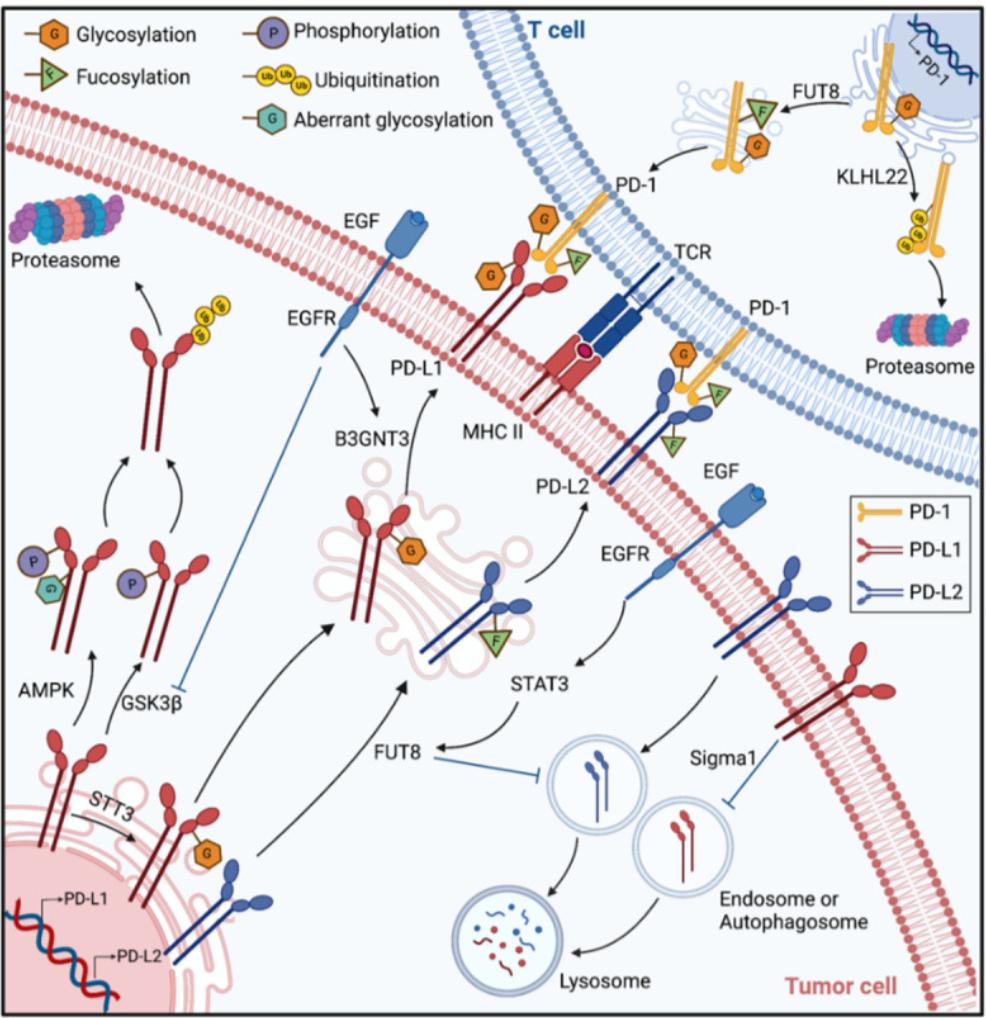
糖基化修饰对PD-1/PD-L1信号通路的影响
总而言之,糖基化是一种非常重要的蛋白质后修饰方式,对蛋白质的理化性质和生物功能都可以产生重大影响。糖基化的研究对于人类健康和疾病的预防和治疗具有重要意义,也可以帮助我们更好地理解生命的起源和演化。
作者简介:
庄文卓 苏州大学教授,研究方向为肿瘤细胞生物学
参考文献
1.Pirillo A, Svecla M, Catapano AL, et al. Impact of protein glycosylation on lipoprotein metabolism and atherosclerosis. Cardiovasc Res. 2021 Mar 21;117(4):1033-1045.
2.Eichler J. Protein glycosylation. Curr Biol. 2019 Apr 1;29(7):R229-R231.
3.Lumibao JC, Tremblay JR, Hsu J, et al. Altered glycosylation in pancreatic cancer and beyond. J Exp Med. 2022 Jun 6;219(6):e20211505.
4.Zhou X, Motta F, Selmi C, et al. Antibody glycosylation in autoimmune diseases. Autoimmun Rev. 2021 May;20(5):102804.
5.Thomas D, Rathinavel AK, Radhakrishnan P. Altered glycosylation in cancer: A promising target for biomarkers and therapeutics. Biochim Biophys Acta Rev Cancer. 2021 Jan;1875(1):188464.
原标题:《【科学普及】蛋白质糖基化与疾病》
