近期,兰州大学孙旺盛教授课题组报道了DMSO/蓝光诱导硫酚对色氨酸侧链吲哚C-2位的精准修饰,构建了结构丰富多样的C-S骨架。该策略可对含有色氨酸活性肽(如:Xenopsin, Leuprorelin, Polistes Mastoparan, Endomorphin-1, Melittin, Daptomycin, GLP-1(7-37)等)进行多样性修饰;同时,还对DMSO在该反应中扮演的角色进行了研究。该方法兼容水相条件,无金属参与,为多肽后期多样性修饰研究提供有益的技术储备和方法支撑。
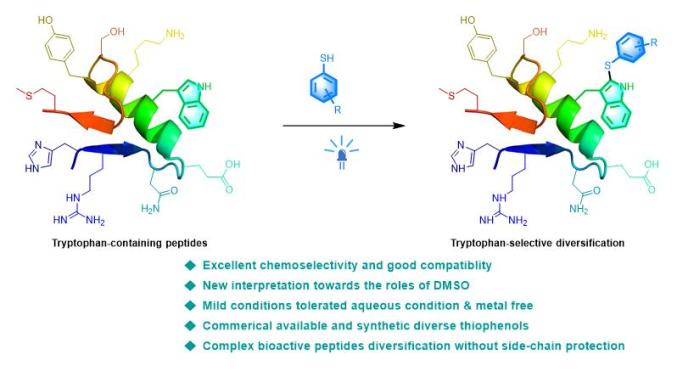
多肽/蛋白质的化学修饰是研究结构、功能、定位、成药性等的有力工具,由于多肽/蛋白质对外部条件的敏感性,对其进行化学修饰必须满足条件温和、选择性高、生物兼容性好等条件。在化学、生物医药等领域广泛应用的“点击化学”和“生物正交化学”,虽然能满足上述要求,但是多肽/蛋白质中几乎不含炔烃、叠氮、四嗪、反式环辛烯等反应弹头,在大分子上额外引入这些反应元件面临极大挑战。所以,基于多肽/蛋白质自身含有的结构单元,原位定点修饰是极佳的选择。色氨酸是一个非常理想的电子转移体和自由基受体。目前已报道的方法主要是碳基修饰的结构,且存在着反应条件苛刻、生物兼容性差、多样性受限的问题。而杂原子与色氨酸偶联的结构常见于一些天然分子中,如:Phalloidin,α-amanitin,celogentin C等,但是构建此类结构的方法仅有个别文献报道。受到Phalloidin和α-amanitin结构的启发,该工作在色氨酸吲哚C-2位构建独特的C-S结构,并应用于含有色氨酸活性肽的定点修饰。
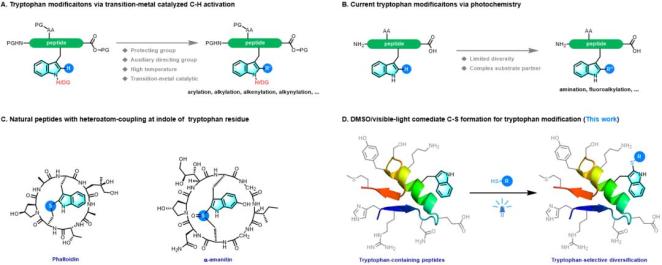
本文亮点:
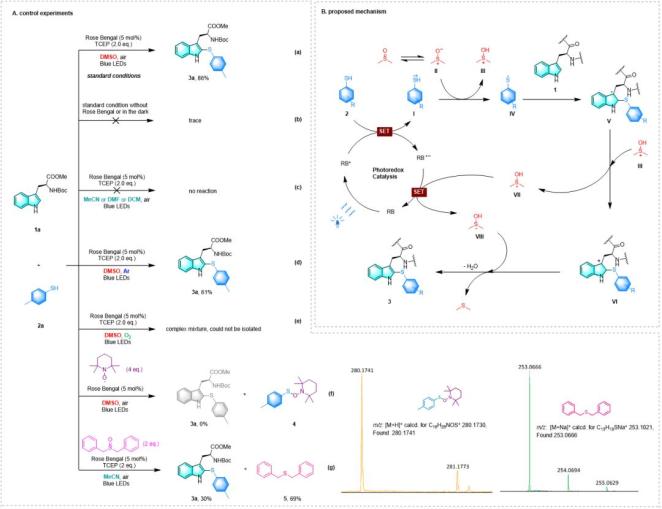
1、通过条件筛选和优化,作者发现DMSO在该过程中起到重要作用,无论是作为溶剂还是倍量加入,均能促进反应。而无DMSO存在时,该反应不能顺利进行。通过控制对照实验,作者推测了如图3所示的反应机理。
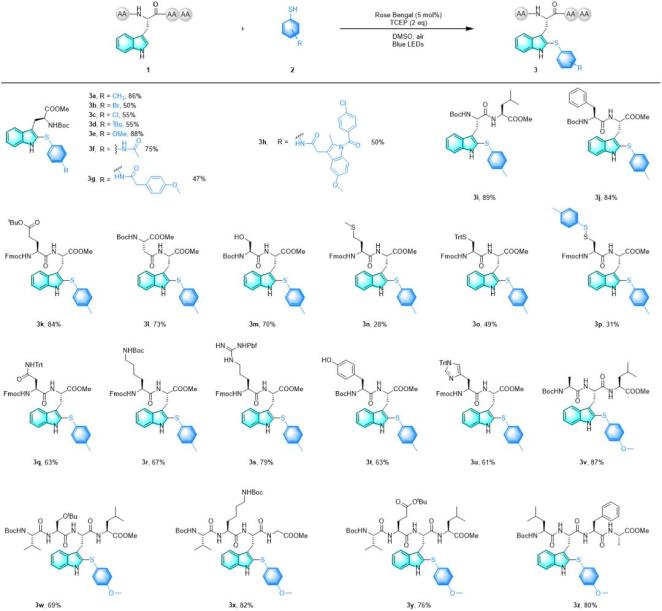
2、在最优条件下,作者应用该策略对含有色氨酸的寡肽进行了修饰。半胱氨酸的侧链裸露时,能得到双修饰的产物;当SH被保护时,仅修饰在色氨酸的吲哚C-2位。其它保护的氨基酸在该反应中均能兼容。(图4)
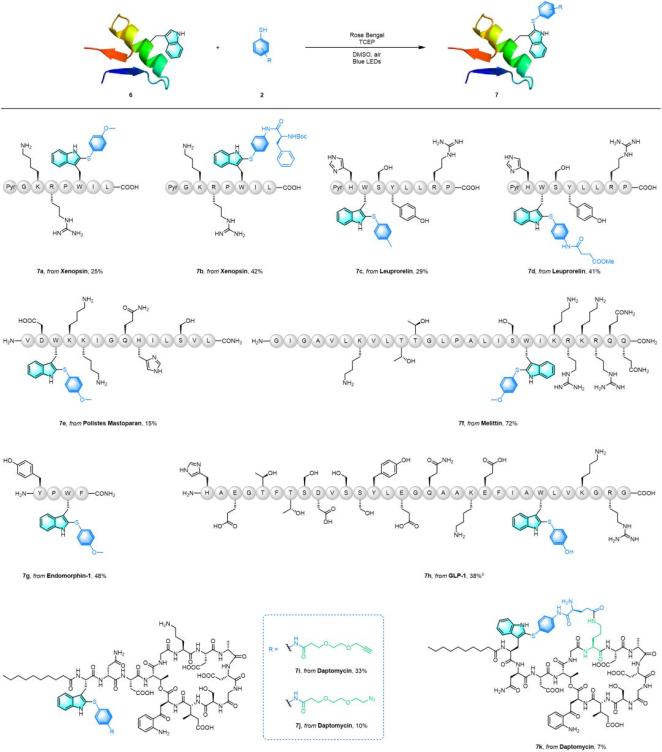
在实现了对寡肽的修饰后,该方法被应用于生物活性多肽Xenopsin, Leuprorelin, Polistes Mastoparan, Endomorphin-1, Melittin, GLP-1(7-37), Daptomycin等的精准修饰,可携带炔烃、叠氮、氨基酸等功能结构,能以可观的分离产率获得目标产物。特别是通过分子内的修饰,成功构建了双环达托霉素类似物(7k)。(图5)
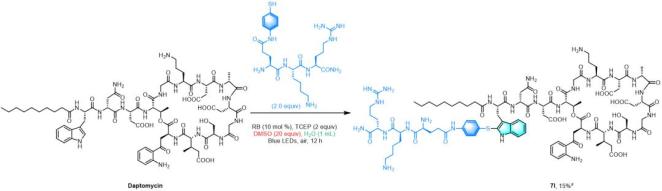
由于小分子芳基硫酚的水溶性较差,作者尝试在三肽(H2N-Glu-Lys-Arg-CONH2)的谷氨酸侧链上连接硫酚结构,该分子具有很好的水溶性。于是,在水作为溶剂的条件下,加入20倍量的DMSO便可实现寡肽与达托霉素的偶联(图6)。
总结与展望:
综上所述,作者围绕色氨酸硫化修饰,开发一套生物兼容性好、选择性高、底物多样性丰富的基于色氨酸的多肽原位定点修饰方法,实现了多种活性多肽的多样性修饰;并从化学合成的角度,探究了该过程的反应机理。该方法为多肽后期修饰研究提供有益的理论依据和技术支撑,在多肽、蛋白质等生物大分子修饰方面具有广阔的应用前景。
文章详情:
Dimethyl Sulfoxide/Visible-Light Comediated Chemoselective C–S Bond Formation Between Tryptophans and Thiophenols Enables Site-Selective Functionalization of Peptides
Guangjun Bao, Peng Wang, Jingyue Li, Xinyi Song, Tingli Yu, Jiao Zhang, Yiping Li, Zeyuan He, Ruiyao E, Xiaokang Miao, Junqiu Xie, Jingman Ni*, Rui Wang* and Wangsheng Sun*
Cite this by DOI:
10.31635/ccschem.023.202303130
文章链接https://doi.org/10.31635/ccschem.023.202303130
扫码在线阅读
扫描或长按左侧二维码,
在线阅读全文

Chemsoc
原标题:《CCS Chemistry | 兰州大学孙旺盛教授课题组:DMSO/蓝光诱导的基于色氨酸的多肽精准功能化修饰》
