原创 Cell Press CellPress细胞科学

Life science
日趋不平衡的全球碳循环和气候变化已经对人类生活和生态系统的可持续发展产生了极大的影响,如何实现碳中和、碳平衡和提高粮食产量是我们目前臻待解决的问题。蓝细菌(也称为蓝藻)是地球上最古老的微生物之一,也是全球生物固碳的关键成员之一。羧酶体作为一种特殊的细菌微室结构,是蓝细菌及许多非光合自养菌中重要的固碳细胞器,也是微生物体内二氧化碳浓缩系统的核心元件。近日,英国利物浦大学整合生物研究所刘鲁宁教授在Cell Press细胞出版社旗下Trends in Microbiology期刊发表了题为“Advances in the bacterial organelles for CO2 fixation”的综述论文,系统地总结了近年来该团队及国内外同行在羧酶体的基础研究和工程化构建领域的最新进展,并提出了该领域的关键生物问题和展望。同时,该文章被选为Trends in Microbiology 2022年6月期刊的封面论文。

细菌二氧化碳浓缩机制
为了降低Rubisco对O2的结合并提升固碳效率,蓝细菌进化出了一种高效的二氧化碳浓缩机制(CO2-concentrating mechanism)(图1),可以吸取环境中二氧化碳和碳酸氢根(HCO3-)并浓缩在Rubisco酶活性中心的周围,从而确保了高的光合催化效率。这种二氧化碳浓缩机制也使得蓝细菌成为全球水环境中最重要的有机物初级生产者,贡献了海洋中一半以上的初级生产量。
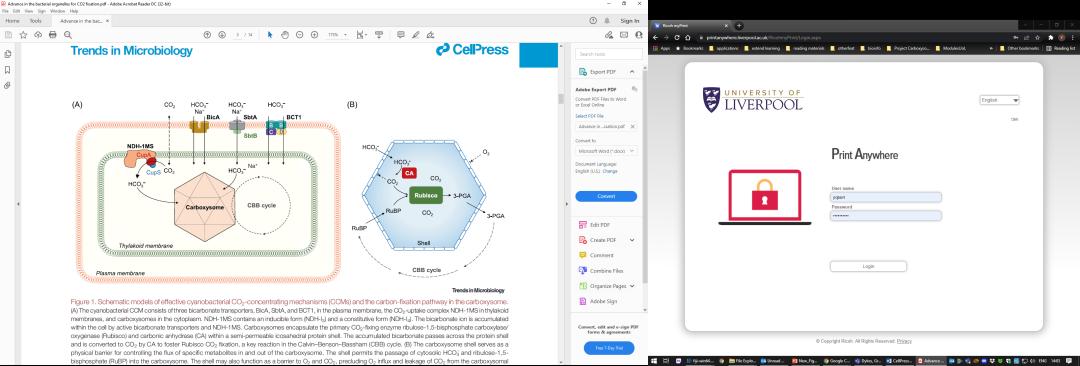
该综述以模式蓝细菌为例,首先介绍了以羧酶体为核心元件的CCM机制的组成和协同工作原理,阐述了近年来通过结构解析揭示的碳酸氢根转运跨膜运输的分子机制,以及NDH复合物中的二氧化碳转化模组CupA/S在碳转化富集过程中的工作机理。
羧酶体 (carboxysome)
羧酶体位于蓝藻细胞质中,是一种典型的细胞微室 (bacterial microcompartment),类似病毒结构,由几百个蛋白通过自聚集而形成。羧酶体外围是一个二十面体的蛋白外壳,由多种不同的外壳蛋白六聚体、五聚体和三聚体配装而成,每种外壳蛋白的中心都有一个孔洞。羧酶体外壳不仅可将Rubisco酶和碳酸酐酶(Carbonic anhydrase)保护并包裹在内腔中,促使固碳酶形成紧密有序的空间排布,而且还具有特异的选择通透性,可透过催化底物分子,比如HCO3-和RuBP(图1)。在羧酶体内腔里,碳酸酐酶将HCO3- 脱水生成CO2,并在Rubisco酶周围的微环境中富集大量的CO2。RuBP和CO2作为Rubisco的底物,驱动CO2固定。
该综述文章重点讨论了羧酶体在蓝细菌体内的结构组成、功能和生理调节等方面的新进展。首先,文章详细介绍了两种不同类型羧酶体(α型和β型)的分型原则以及基因和蛋白质组成(图2),继而介绍了单分子荧光显微镜技术对β型羧酶体蛋白计量的研究,并阐述了羧酶体蛋白组分在不同环境条件下的可塑性。
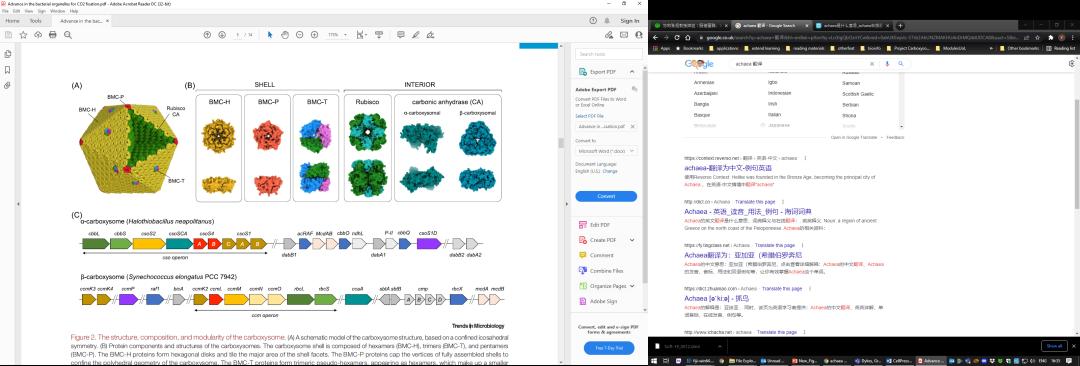
文章进而阐述了两种类型羧酶体中Rubisco酶的组装、激活和聚集形式,以及碳酸酐酶在羧酶体中的功能。Rubisco酶的组装需要一系列分子伴侣蛋白的辅助:在模式蓝细菌聚球藻Synechococcus 7942中,Raf1是必不可缺的重要辅助因子,而RbcX的缺失不会完全破坏Rubisco酶的组装。研究表明Raf1和RbcX都对羧酶体的组装产生影响,其中Raf1尤为重要。根据羧酶体的类型,Rubisco酶的激活需要CbbQO或Rca激酶。Rubisco酶的聚集受具有无序结构的CcmM或CsoS2连接蛋白的多价结合介导,通过液液相分离(liquid-liquid phase separation)形成Rubisco酶的液态聚合体。形成的核心酶聚合体再通过其他特殊的组成蛋白与外壳蛋白结合,最终完成外壳的封装。
蛋白外壳的选择通透性
随后,文章对羧酶体蛋白外壳的选择通透机理进行了阐述。当前研究表明,外壳蛋白的中心孔洞带正电荷,可允许带负电荷的碳酸根离子进入羧酶体腔内,同时阻隔无电荷性的二氧化碳和氧气分子通过(图3)。由于外壳蛋白六聚体和五聚体中心孔洞的孔径相对较小,RuBP和3-PGA等大分子代谢底物或产物被认为是通过具有更大孔径的外壳蛋白三聚体进出羧酶体的。另外,羧酶体外壳自身构象的柔性和可塑性也可能有助于对通透性进行调控。外壳蛋白对代谢底物和产物、质子和还原剂的选择通透性,为建立羧酶体腔内特殊的pH和氧化还原态的内环境至关重要。而这一特殊的内环境在Rubisco酶聚集以及调控碳酸酐酶活性和羧酶体功能中是必不可少的。
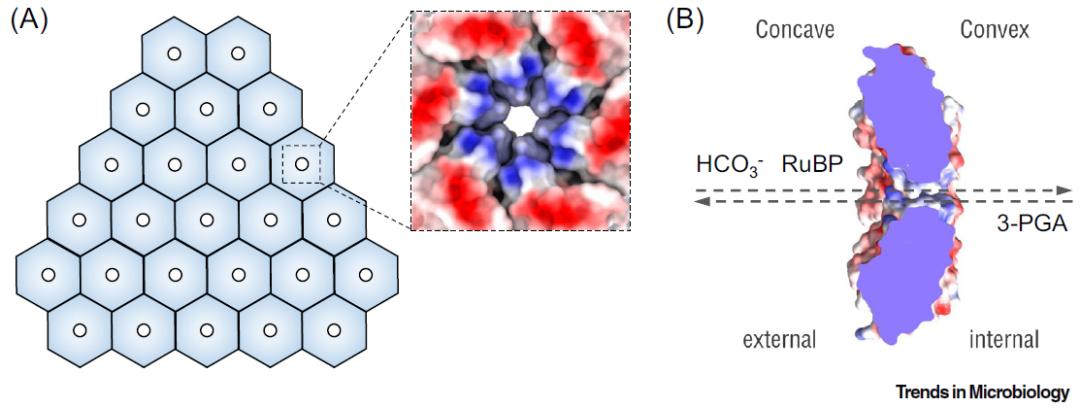
羧酶体天然合成和细胞内定位
文章比较性地分析了对两种类型羧酶体从核心酶的聚集、外壳蛋白的招募,直至最终形成羧酶体的天然过程的研究进展(图4),同时也阐述了目前对羧酶体细胞内定位调控机制的认识,以及外界生长环境(如光照强度和节律等)对羧酶体生物合成、结构、功能和亚细胞分布的影响,进一步证实了羧酶体结构和功能的可塑性和环境适应性。
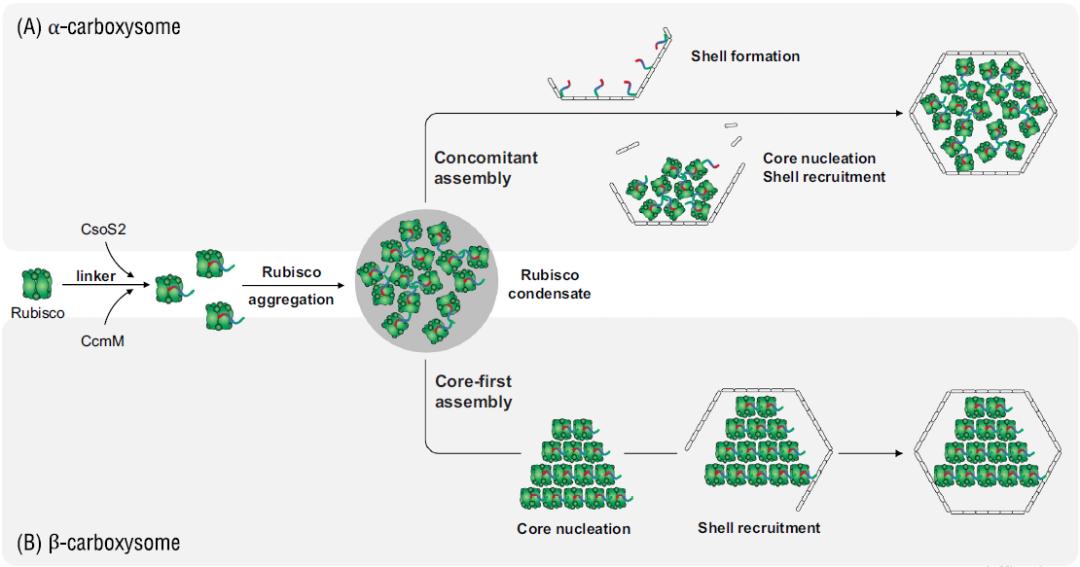
基于羧酶体的自聚集特性、可塑性以及对酶催化活性的促进功能,羧酶体被认为是一种理想的合成生物学模式系统。该综述文章列举了近期对羧酶体的人工改造和新功能开发的一系列工作,介绍了利用合成生物学方法人工构建羧酶体结构,并对其进行构象和功能的优化、改造、以及在生物产氢等方面的应用。文章也阐述了如何通过优化羧酶体的组成成份,进一步研究细菌微室的生物合成过程和分子机理,并为采用合成生物学方法改造和构建新的羧酶体功能复合物提供了科学依据和可能的方案。
总结
对微生物内羧酶体和二氧化碳浓缩机制的全面深入研究,不仅有助于进一步提高我们对自然和生物体的科学认识,而且有重大的社会和经济价值。最近,依靠提高光合作用中的固碳效率来提高农作物的产量受到了广泛的关注。与蓝细菌不同,绝大多数的农作物,例如水稻、小麦、大豆、棉花等,都是利用C3途径进行光合作用,在这些作物体内中没有有效的二氧化碳浓缩体系,因此影响了农作物的光合效率和产量。如果能通过基因工程技术,将蓝细菌的羧酶体和二氧化碳浓缩机制引入到植物体内,将有效的提高农作物碳能力和粮食产量。
本文参考文献(上线划动查看)
1.Chen, T. et al. Incorporation of Functional Rubisco Activases into Engineered Carboxysomes to Enhance Carbon Fixation. ACS Synthetic Biology 11, 154-161 (2022).
2.Liu, L. N., Yang, M., Sun, Y. & Yang, J. Protein stoichiometry, structural plasticity and regulation of bacterial microcompartments. Curr Opin Microbiol 63, 133-141 (2021).
3.Li, T. et al. Reprogramming bacterial protein organelles as a nanoreactor for hydrogen production. Nature Communications 11, 5448 (2020).
4.Huang, F. et al. Rubisco accumulation factor 1 (Raf1) plays essential roles in mediating Rubisco assembly and carboxysome biogenesis. PNAS 117, 17418-17428 (2020).
5.Faulkner, M. et al. Molecular simulations unravel the molecular principles that mediate selective permeability of carboxysome shell protein. Scientific Reports 10, 17501 (2020).
6.Sun, Y., Wollman, A. J. M., Huang, F., Leake, M. C. & Liu, L. N. Single-organelle quantification reveals the stoichiometric and structural variability of carboxysomes dependent on the environment. Plant Cell 31, 1648-1664 (2019).
7.Huang, F. et al. Roles of RbcX in carboxysome biosynthesis in the cyanobacterium Synechococcus elongatus PCC7942. Plant Physiology 179, 184-194 (2019).
8.Fang, Y. et al. Engineering and modulating functional cyanobacterial CO2-fixing organelles. Frontiers in Plant Sciences 9, 739 (2018).
9. Faulkner, M. et al. Direct characterization of the native structure and mechanics of cyanobacterial carboxysomes. Nanoscale 9, 10662-10673 (2017).
10. Sun, Y. et al. Light modulates the biosynthesis and organization of cyanobacterial carbon fixation machinery through photosynthetic electron flow. Plant Physiology 171, 530-541 (2016).


教授
刘鲁宁,英国利物浦大学教授,博士生导师,英国皇家科学院研究员。担任英国生物技术与生物科学研究委员会(BBSRC)评审、工程和物理科学研究委员会(EPSRC)评审、欧洲研究理事会(ERC)项目评审、国家自然科学基金委生命科学部重点项目评审。课题组对光合作用、二氧化碳固定、生物膜合成和结构、蛋白复合物自聚集等领域进行了广泛深入的研究。发表SCI期刊论文超过80篇,包括Nature Plants、Nature Communications、Science Advances、Nano Letters、PNAS、Molecular Plants、Plant Cell、eLife、Plant Physiology、Ann Rev Microbiol、Curr Opin Microbiol、Trends in Plant Sciences等国际知名杂志。
实验室网页:www.luningliu.org
相关论文信息
相关研究发表在Cell Press细胞出版社旗下期刊Trends in Microbiology,
点击“阅读原文”或扫描下方二维码查看论文
▌论文标题:
Advances in the bacterial organelles for CO2 fixation
▌论文网址:
https://www.cell.com/trends/microbi-ology/fulltext/S0966-842X(21)00259-6
▌DOI:
https://doi.org/10.1016/j.tim.2021.10.004
