
生物体内,遗传信息储存在DNA中,通过转录作用生成RNA也即转录本,其中一些转录本会直接翻译形成蛋白质发挥功能(编码RNA/转录本),也有很多转录本以RNA形式参与细胞内的调控功能(非编码RNA/转录本)。其中RNA上的化学修饰,被认为是很多RNA层面调控实现的基础。目前已发现的RNA化学修饰有200多种,其中N6-甲基腺嘌呤(m6A)是真核生物mRNA上丰度最高的修饰,被认为广泛参与RNA的剪接、转运、降解、翻译、相分离等过程的调控。RNA上m6A修饰的建立依赖于甲基转移酶蛋白复合物,包括METTL3、METTL14、METTL16、WTAP和KIAA1429等。研究发现这些蛋白如果缺乏会引发小鼠胚胎干细胞分化,卵子发生和早期胚胎发育等方面的异常。但是传统的m6A修饰的测序技术需要大量RNA作为原料,而小鼠早期胚胎材料十分稀少,所以对于小鼠等哺乳动物在早期胚胎发育过程中的m6A修饰组学动态检测一直缺乏,限制了相关机制研究的开展。
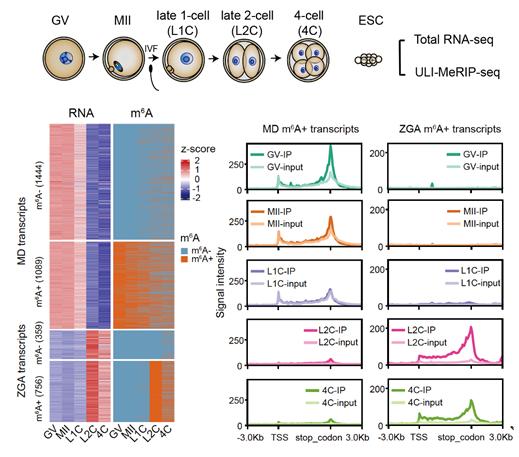
此项研究中,为揭示m6A在小鼠早期胚胎中的组学动态,研究人员首先优化了传统的m6A测序方法,建立了适用于50ng total RNA起始的ULI-MeRIP-seq方法,该方法能够精确检测RNA上m6A修饰分分布位置,并与RNA大量起始所获得的m6A修饰信息有高度的重叠。研究团队利用这一方法对GV 卵母细胞(减数分裂双线期后期)、MII卵母细胞(第二次减数分裂中期,成熟态卵母细胞)、受精卵以及卵裂早期胚胎(2-细胞和4-细胞胚胎)等母源-合子转变过程中涉及的卵母细胞与胚胎材料,进行了m6A修饰检测。结果显示,对于编码蛋白的转录本来说,约40%的母源性转录本上具有m6A修饰的富集,这些转录本在卵母细胞中表达量普遍高于未修饰RNA,并大多在受精后才被降解。而在受精后才激活的ZGA转录本中,约70%都富集m6A修饰,其中包括2-细胞特异性表达的RNA如Zscan4(图1)。值得注意的是很多发育阶段特异性的非编码转录本,如卵母细胞中高丰度的MTA(属于MaLR家族)以及2-细胞特异性表达的MERVL(属于ERVL家族),都高度富集了m6A修饰。
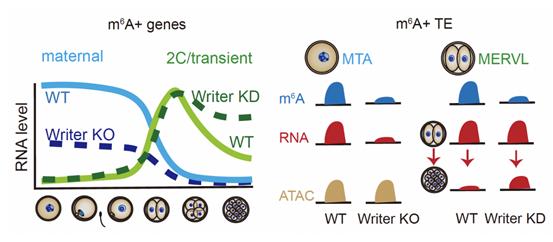
为了揭示m6A对于母源和子代转录本的调控作用,研究人员利用卵母细胞特异性敲除Kiaa1429(RNA甲基转移酶复合体成员之一)的小鼠模型以及甲基转移酶METTL3抑制剂STM2457,分别获取了m6A修饰建立缺陷的卵子以及胚胎样本。研究团队发现母源转录本,包括母源转座子MTA的转录本,缺乏m6A修饰后会呈现本身丰度的显著降低(图2);有趣的是抑制ZGA转录本上m6A的建立,会引发2-4-细胞时期短暂表达的转录本如Zscan4,逆转座子MERVL无法及时降解,进而分别引发了卵子与胚胎发育的阻滞。这些结果证明转录本上的m6A修饰调控了母源转录本的维持与子代转录本的有序降解,保证了生命早期母源-子代转变的顺利发生。
高绍荣介绍,团队利用高通量测序法首次绘制了小鼠早期胚胎发育过程中转录本上m6A修饰的动态图谱,并证实了母源的转座子MTA和2-细胞时期转座子MERVL具有高度的m6A修饰富集。研究进一步发现m6A修饰分别维持了卵母细胞中母源RNA的稳定性,以及受精后短暂表达的转录本的及时降解。m6A修饰在卵母细胞和合子基因激活阶段不同的调控功能体现了生命初始阶段调控的复杂性,并为进一步探究生命调控奥秘开辟了全新视域。
论文第一作者是同济大学博士后吴悠、徐小翠,以及南京医科大学齐美杰博士,高绍荣、高亚威、沈彬是本文的共同通讯作者。浙江大学附属妇产科医院的陈川博士、北京大学伊成器教授、芝加哥大学向俊鸿博士、山东大学生殖医学研究中心刘洪彬教授等也参与了此项工作。该研究得到了科技部、国家自然科学基金委以及上海市科委等项目的支持。
据悉,研究团队致力于解析小鼠早期胚胎及植入后胚胎发育以及胚胎干细胞中的m6A调控作用,近期还阐明了FTO基因通过调控LINE1 RNA的m6A修饰调控核表观与发育(2022年5月5日在《science》杂志在线发表),YTHDC1调控早期胚胎及胚胎干细胞中LINE1 RNA功能等多项重要机制。
高绍荣团队一直致力于解析小鼠早期胚胎发育与细胞重编程中的表观调控机制。今年4月28日,团队与生命科学与技术学院张勇团队合作在《自然·细胞生物学》(Nature Cell Biology)上在线发表了题为《等位基因特异性H3K9me3和DNA甲基化共同标记的富含双核甘酸(CPG)区域作为着床前胚胎中潜在的印迹控制区域》的论文,报道了小鼠植入前胚胎发育过程的一项研究成果。今年5月5日,团队与芝加哥大学何川团队合作在《科学》(Science)上在线发表题为《FTO在mESCs和小鼠发育中介导LINE1 m6A去甲基化和染色质调节》的论文,阐明了FTO基因通过调控LINE1 RNA的m6A修饰调控核表观与发育的分子机制。
原标题:《厉害了!同济这个团队一月内三发国际顶刊》
